Đề thi tham khảo ôn thi THPT Hóa học có đáp án - Đề tham khảo số 8
28 câu hỏi
Chất nào sau đây là chất béo?
C17H35COOC3H5.
(CH3COO)3C3H5.
(C15H31COO)3C3H5.
C17H35COOH.
Thành phần kim loại cơ bản trong hợp kim duralumin là
Mg.
Cu.
Fe.
Al.
Chất nào sau đây có thể tham gia phản ứng trùng hợp?
HO-CH2-COOH.
CH2=CH2.
CH3-CH3.
H2N-CH2-COOH.
Khi đun nóng, phản ứng giữa dung dịch NaOH với chất nào dưới đây gọi là phản ứng xà phòng hóa?
Phenol.
Acid.
Ester.
Amino acid.
Phát biểu nào sau đây đúng?
Cellulose và tinh bột đều là polysaccharide thiên nhiên.
Trong tinh bột và cellulose đều chứa liên kết α-glycoside.
Tinh bột được cấu tạo từ các gốc β-glucose.
Cellulose được cấu tạo từ các gốc α-glucose.
Các hợp chất của nguyên tố nào sau đây có trong cơ thể người giúp phát triển, ổn định xương và răng, ổn định chức năng tim mạch, thần kinh?
Fe.
K.
Mg.
Ca.
Phản ứng hạt nhân có nhiều ứng dụng trong cuộc sống. Dựa trên cơ sở sử dụng tia bức xạ có năng lượng cao (tia γ, β,…) từ phản ứng hạt nhân để tiêu diệt hoặc kìm hãm sự phát triển tế bào ung thư (phương pháp xạ trị). Tia bức xạ phá hủy DNA của tế bào ung thư.
Hạt α chính là hạt nhân 2 4 H e ; hạt β chính là electron − 1 0 e ; hạt γ là các photon 0 0 γ . Đồng vị 2 7 6 0 C o được dùng trong phương pháp trị xạ theo phương trình sau:
2 7 6 0 C o → Z A X + β + γ
Tất cả các phản ứng hạt nhân đều tuân theo định luật bảo toàn số khối và điện tích. Giá trị của A là
28.
60.
61.
59.
Tính chất vật lí nào sau đây được quan tâm khi tách hai chất lỏng tan vào nhau bằng phương pháp chưng cất?
Nhiệt độ nóng chảy của chất.
Tính tan của chất trong nước.
Nhiệt độ sôi của chất.
Màu sắc của chất.
Cho sơ đồ lưu hóa cao su:
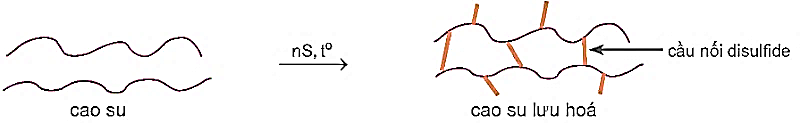
Quá trình lưu hoá cao su thuộc loại phản ứng
cắt mạch polymer.
phân huỷ polymer.
tăng mạch polymer.
giữ nguyên mạch polymer.
Benzene tác dụng với bromine khi có mặt xúc tác: C6H6+Br2→t0FeBr3C6H5-Br + HBr (*)
Phản ứng xảy ra các giai đoạn sau:
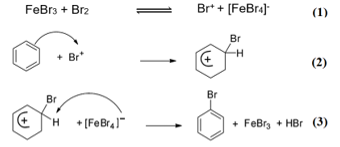
Phát biểu nào sau đây đúng?
Trong giai đoạn (2) có sự hình thành liên kết pi (π) giữa carbon và bromine.
Phản ứng (*) là phản ứng cộng bromine vào vòng benzene.
Trong gian đoạn (3) hình thành liên kết pi (π) giữa carbon và carbon.
Khối lượng FeBr3 trước phản ứng ít hơn sau phản ứng.
Cho các cặp oxi hóa khử: X2+/X; Y2+/Y; Z2+/Z. Pin X–Y có sức điện động chuẩn là 1,10 V. Pin Y–Z có sức điện động chuẩn là 0,82 V. Pin X–Z có sức điện động chuẩn là bao nhiêu volt (V)?
0,82.
1,92.
1,10.
0,28.
Trong các nguyên tố: Cr, Fe, Mn, Co, mỗi nguyên tố thể hiện nhiều số oxi hóa dương trong các hợp chất khác nhau. Nguyên nhân chính là do
nguyên tử bán kính nhỏ, nguyên tố có độ âm điện lớn.
nguyên tử bán kính lớn, nguyên tố có độ âm điện nhỏ.
nguyên tử có nhiều electron hóa trị, nguyên tố có độ âm điện lớn.
nguyên tử có nhiều electron hóa trị, nguyên tố có độ âm điện nhỏ.
Hợp kim là vật liệu kim loại có chứa một …(1)… cơ bản và một số …(1)… khác hoặc …(2)…. Nội dung phù hợp trong (1), (2) lần lượt là
phi kim; kim loại.
hợp chất; phi kim.
kim loại; phi kim.
hợp chất; kim loại.
Nhôm được ứng dụng để chế tạo dụng cụ nhà bếp như ấm đun nước, xoong chảo,.... Nguyên nhân chính là do nhôm có tính chất nào sau đây?
Tính khử mạnh.
Khối lượng riêng lớn.
Dẫn điện tốt.
Dẫn nhiệt tốt.
Cation Cu2+ đã nhận 6 cặp electron hóa trị của các phân tử H2O hình thành phức aqua có công thức là
[Cu(OH)6]2+.
[Cu(OH2)6]2+.
[Cu(OH2)6].
[Cu(OH)6]4-.
Thực hiện phản ứng: 2ICl(g) + H2(g)→ I2(g)+ 2HCl(g).
Nồng độ đầu của ICl và H2 được lấy đúng theo tỉ lệ hợp thức. Nghiên cứu sự thay đổi nồng độ các chất tham gia và chất tạo thành trong phản ứng theo thời gian, thu được đồ thị như hình bên.
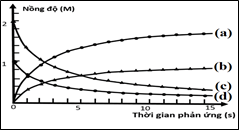
Dựa vào đồ thị, hãy cho biết đường nào ứng với sự biến đổi nồng độ của HCl trong phản ứng trên là
(d).
(a).
(c).
(b).
Phức chất [PtCl2(NH3)2] (vuông phẳng) có hai dạng đồng phân hình học (cis – trans) như hình bên.
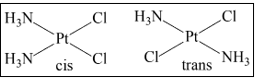
Khi hình thành phức, ion SCN− có thể tạo liên kết cho nhận với Pt2+ qua nguyên tử S hoặc N tạo ra các đồng phân liên kết, NH3 tạo liên kết cho nhận với Pt2+ qua nguyên tử N. Phức chất X (vuông phẳng) được tạo thành từ sự kết hợp của một Pt2+ với hai NH3 và hai SCN−. Tổng số lượng đồng phân liên kết và hình học của X là
6.
2.
4.
8.
Biết: EAg+/Ag0=0,80V; EFe3+/Fe2+0=0,77V; ECu2+/Cu0=0,34V; EFe2+/Fe0= - 0,44V . Trong các ion: Ag+, Fe3+, Cu2+, Fe2+, ion có tính oxi hóa mạnh nhất là
Ag+.
Cu2+.
Fe2+.
Fe3+.
Sulfur dioxide là một trong các tác nhân gây mưa acid, phát thải chủ yếu từ các quá trình đốt cháy nhiên liệu như than đá, xăng, dầu,…
Một nhà máy nhiệt điện than sử dụng hết 6000 tấn than đá/ngày, có thành phần chứa 0,8% sulfur về khối lượng để làm nhiên liệu. Giả thiết có 1% lượng khí SO2 tạo ra khuếch tán vào khí quyển rồi bị chuyển hóa thành sulfuric acid trong nước mưa theo sơ đồ:
SO2→xt+O2 SO3→+H2O H2SO4
Thể tích nước mưa bị nhiễm acid, giả thiết nồng độ sulfuric acid trong nước mưa là 1.10-5 M là x nghìn m3. Giá trị của x bằng bao nhiêu? Kết quả làm tròn đến hàng đơn vị.
Phân tử khối của peptide Ala-Glu-Gly-Ala-Lys-Glu là bao nhiêu?
Cellulose tác dụng với acetic anhydride thu được cellulose triacetate theo phương trình sau:
[C6H7O2(OH)3]n + 3n(CH3CO)2O→[C6H7O2(OCOCH3)3]n+3nCH3COOH
Khi sử dụng cellulose của bông thì hiệu suất phản ứng đạt 91,30% tính theo cellulose. Tính số kg tơ acetate chứa 92% khối lượng cellulose triacetate tạo thành từ 1,0 tấn bông chứa 99,0% cellulose (coi các tạp chất trong bông không sinh ra cellulose triacetate, làm tròn kết quả đến hàng đơn vị và chỉ làm tròn ở phép tính cuối cùng).
Trong phức chất: số liên kết σ của một phối tử với nguyên tử trung tâm được gọi là dung lượng phối trí của phối tử đó; tổng số liên kết σ giữa nguyên tử trung tâm với các phối tử được gọi là số phối trí của nguyên tử trung tâm đó. Trong nghiên cứu về xúc tác đồng thể, người ta tổng hợp được một phức chất có công thức [CoCl2(en)2]+ có tính ổn định cao và được sử dụng làm chất trung gian trong tổng hợp các hợp chất hữu cơ. Cho biết phối tử ethylenediamine (en) có dung lượng phối trí là 2. Phức chất [CoCl2(en)2]+ có số phối trí của nguyên tử trung tâm là bao nhiêu?
Một nhà máy nhiệt điện than sử dụng hết 6000 tấn than đá/ngày, có thành phần chứa 0,8% sulfur về khối lượng để làm nhiên liệu. Khí SO2 thải ra ngoài không khí sẽ chuyển hóa thành sulfuric acid theo sơ đồ: SO2 → SO3 → H2SO4. Biết rằng, hệ thống xử lí khí thải của nhà máy có thể giảm 99% lượng khí SO2 và đo đạc trong nước mưa xung quanh khu vực nhà máy cho thấy nồng độ sulfuric acid là 10-5 (M). Thể tích nước mưa (m³) trong ngày đã nhiễm acid là a.106. Giá trị của a là
Trong một nhà máy, người ta dùng than đá để cung cấp nhiệt cho quá trình sản xuất. Nhà máy sử dụng một loại than đá có 90,0% carbon, 2,0% sulfur về khối lượng, còn lại là tạp chất trơ không cháy. Trong điều kiện ở nhà máy, người ta xác định được nhiệt của các phản ứng như sau:
C(s) + O2(g)→CO2(g) ΔrH(1) = -393,5 kJS(s) + O2(g)→SO2(g) ΔrH(2) = -296,8 kJ
Để sản xuất 1 sản phẩm cần sử dụng năng lượng là 20000 kJ. Nếu có 20,0% nhiệt năng của quá trình đốt cháy bị thất thoát thì để sản xuất được 1000 sản phẩm thì cần bao nhiêu kg than đá nói trên? Làm tròn kết quả đến hàng đơn vị và chỉ làm tròn ở phép tính cuối cùng.
Trong công nghiệp sản xuất Na, quá trình điện phân được thực hiện trong bình điện phân Downs với hỗn hợp nóng chảy ở 600 – 650°C gồm NaCl và CaCl2 theo tỉ lệ khối lượng tương ứng khoảng 3 : 2. Hiệu điện thế trong bình điện phân được duy trì trong khoảng 6 – 7 V, thu được kim loại tinh khiết ở cathode. Cường độ dòng điện chạy qua chất điện li nóng chảy từ 20 – 40 kA. Cho nhiệt độ nóng chảy của NaCl và CaCl2 lần lượt là 801°C và 772°C.
. Nếu tăng diện tích bề mặt các điện cực và tăng cường độ dòng điện tương ứng sẽ giúp làm tăng sản lượng Na.
. Nếu sử dụng MgCl2 (có nhiệt độ nóng chảy là 714°C) thay thế cho CaCl2 trong quá trình trên sẽ đạt hiệu quả sản xuất tốt hơn.
. Một trong các vai trò của CaCl2 là giúp giảm nhiệt độ nóng chảy khi điện phân
. Quá trình sản xuất Na cũng đồng thời thu được khí Cl2 ở anode.
Điểm đẳng điện (pI) là giá trị pH tại đó một amino acid tồn tại chủ yếu dưới dạng ion lưỡng cực, tức là mang đồng thời điện tích dương và âm nhưng tổng điện tích bằng không.
Giá trị pH của dung dịch so với giá trị pI | nhỏ hơn | bằng | lớn hơn |
Dạng tồn tại của amino acid | cation | ion lưỡng cực | anion |
Tryptophan (pI = 5,88) là amino acid thiết yếu, cơ thể không thể tổng hợp được. Công thức cấu tạo của tryptophan như hình bên: 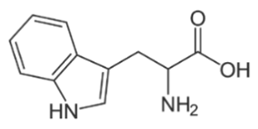
Một mol tryptophan tác dụng được với tối đa hai mol HCl trong dung dịch.
Cả tryptophan và aniline đều phản ứng với dung dịch HCl và NaNO2 khi đun nóng, giải phóng khí N2 do cùng chứa nhóm amino (-NH2) trong cấu trúc phân tử.
Trong dung dịch có pH = 7,55, tryptophan tồn tại chủ yếu ở dạng cation, di chuyển về phía cực âm khi đặt điện trường
Tryptophan có công thức phân tử là C11H14N2O2.
Thép thường hay thép carbon là hợp kim của Fe và C (≤ 2%), nguyên tố khác rất ít hoặc không có. Để xác định hàm lượng Fe trong mẫu thép chứa Fe, C và Si người ta thực hiện các thí nghiệm sau:
- Cân 10,00 gam mẫu thép rồi cho vào 200 mL dung dịch H2SO4 1M đến khi phản ứng xảy ra hoàn toàn thu được 200 mL dung dịch X.
- Lấy 10,0 mL dung dịch X vào trong cốc thuỷ tinh, thêm tiếp dung dịch H2SO4 1M (dư) rồi chuẩn độ bằng dung dịch KMnO4 0,1M. Kết quả chuẩn độ, thể tích (mL) dung dịch KMnO4 0,1M sử dụng qua 3 lần chuẩn độ như sau:
Lần chuẩn độ | Lần 1 | Lần 2 | Lần 3 |
Thể tích dung dịch KMnO4 0,1M | 17,6 | 17,4 | 17,5 |
Trong phản ứng chuẩn độ, chất khử là KMnO4.
Vai trò của C trong thép là bảo vệ Fe không bị ăn mòn điện hóa.
Điểm tương đương (kết thúc chuẩn độ) là khi dung dịch trong cốc bắt đầu chuyển màu tím.
Hàm lượng Fe trong thép là 98,0%.
Các muối carbonate của kim loại nhóm IIA khó tan trong nước và bị phân hủy theo phản ứng sau:
MCO3(s) → MO(s) + CO2(g) (1)
Cho bảng thông tin sau:
Muối MCO3 | MgCO3 | CaCO3 | SrCO3 | BaCO3 |
| ΔrH2980 (1) | 100,7 | 179,2 | 234,6 | 271,5 |
Độ tan (20°C, g/100g H2O) | 1,00.10-2 | 1,30.10-3 | 1,10.10-3 | 2,40.10-3 |
. Độ bền nhiệt của các muối có xu hướng tăng từ MgCO3 đến BaCO3.
. Phản ứng (1) minh họa cho quá trình đun sôi để làm giảm tính cứng của nước cứng tạm thời (với M là Ca2+, Mg2+).
. Để thu được cùng khối lượng các oxide kim loại thì phản ứng phân hủy BaCO3 cần năng lượng nhiều nhất.
. Tại 20°C thì 1,5 lít H2O (D = 1 g/mL) hòa tan được tối đa 19,5 mg CaCO3.








