Đề thi tham khảo ôn thi THPT Hóa học có đáp án - Đề tham khảo số 6
28 câu hỏi
Methyl acrylate là một chất kích thích mạnh, có thể gây chóng mặt, đau đầu, hoa mắt và khó thở khi tiếp xúc với da hoặc hít phải, ester này có công thức cấu tạo thu gọn là
CH3COOC2H5.
CH3COOCH3.
C2H5COOC2H3.
CH2=CHCOOCH3.
Chất nào sau đây thuộc loại monosaccharide?
Saccharose.
Glucose.
Tinh bột.
Cellulose.
Chất nào sau đây không tạo được liên kết hydrogen giữa các phân tử?
HF.
H2O.
NH3.
HI.
Kim loại nào sau đây điều chế được bằng phương pháp thủy luyện?
Al.
Au.
Na.
Mg.
Hydrate hóa alkene nào sau đây chỉ thu được một sản phẩm hữu cơ duy nhất?
Propene.
2-methyl but-2-en.
2-methyl but-1-ene.
But-2-ene.
Đun nước lâu ngày thấy xuất hiện lớp cặn bám vào đáy ấm đun nước. Để loại bỏ lớp cặn có thể dùng dung dịch nào sau đây?
Cồn.
Giấm ăn.
Nước vôi.
Muối ăn.
Hiện tượng phú dưỡng là một biểu hiện của môi trường ao, hồ bị ô nhiễm do dư thừa các chất dinh dưỡng, Sự dư thừa dinh dưỡng chủ yếu do hàm lượng các ion nào sau đây vượt quá mức cho phép?
Sodium, potassium.
Calcium, magnesium.
Nitrate, phosphate.
Chloride, sulfate.
Tên thay thế của amine CH3-NH-CH2-CH2-CH3 là
Methylpropylamine.
N-methylpropan-1-amine.
N-methylpropan-3-amine.
N-propylmethylamine.
Trong phản ứng với nước bromine, aniline thể hiện phản ứng nào sau đây?
Phản ứng cộng halogen vào nhóm –NH2.
Phản ứng thế hydrogen của nhóm –NH2.
Phản ứng cộng hợp halogen vào vòng benzene.
Phản ứng thế hydrogen trên vòng benzene.
Polymer nào sau đây thuộc loại polymer tổng hợp?
Tinh bột.
Tơ tằm.
Polyethylene.
Cao su thiên nhiên.
Các kim loại nhóm IA (nhóm kim loại kiềm) và hợp chất của chúng có nhiều ứng dụng như: sản xuất pin lithium, nước Javel, phân kali, tế bào quang điện, đồng hồ nguyên tử, ... Các nhận định sau đây nhận định nào sai?
Trong tự nhiên, các kim loại kiềm chỉ tồn tại ở dạng hợp chất.
Các kim loại kiềm có độ cứng thấp do có liên kết kim loại yếu.
Ở nhiệt độ thường, các ion kim loại nhóm IA đều có màu đặc trưng.
Trong các hợp chất, nguyên tố kim loại kiềm chỉ có số oxi hóa là +1.
Cho các cặp oxi hoá - khử của các kim loại và thế điện cực chuẩn tương ứng:
| Cặp oxi hóa – khử | Li+/Li | Mg2+/Mg | Zn2+/Zn | Ag+/Ag |
| Thế điện cực chuẩn, V | -3,040 | -2,356 | -0,762 | +0,799 |
Nhận xét nào sau đây đúng?
Tính khử của Mg lớn hơn tính khử của Li.
Thế điện cực chuẩn của pin Galvani Zn-Ag có giá trị 1,1V.
Trong dung dịch Mg oxi hóa được ion Zn2+ thành Zn.
Trong dung dịch Ag+ oxi hóa được Zn thành Zn2+.
Dãy gồm các kim loại phản ứng với nước ở nhiệt độ thường là
Na, Fe, K.
Na, Cr, K.
Be, Na, Ca.
Na, Ba, K.
Phát biểu nào sau đây về thứ tự điện phân trong dung dịch của các ion kim loại ở điện cực là đúng?
Ion kim loại ứng với thế điện cực chuẩn lớn hơn sẽ được điện phân trước ở cực âm.
Ion kim loại ứng với thế điện cực chuẩn âm hơn sẽ được điện phân trước ở cực âm.
Ion kim loại ứng với thế điện cực chuẩn dương hơn sẽ được điện phân trước ở cực dương.
Ion kim loại ứng với thế điện cực chuẩn âm hơn sẽ được điện phân trước ở cực dương.
Có 4 ester no, đơn chức, mạch hở được kí hiệu ngẫu nhiên lần lượt là X, Y, Z, T. Phân tử ester của mỗi chất nêu trên đều tạo bởi các carboxylic acid mạch không phân nhánh và ethyl alcohol. Độ tan của 4 ester được cho ở bảng sau:
| Ester | X | Y | Z | T |
| Độ tan (g/100 g nước, ở 25oC) | 8,7 | 10,5 | 2,2 | 4,9 |
Trong số 4 ester trên, ester có nhiều nguyên tử carbon nhất trong phân tử là
Y.
T.
X.
Z.
Cho các phát biểu sau:
a). Oleic acid và linoleic acid đều thuộc loại acid béo omega-6.
b). Cellulose và tinh bột đều tan trong nước Schweizer.
c). Trong môi trường có pH =12, glycine và lysine đều di chuyển về cực dương của điện trường.
d). Polymer khâu mạch (tăng mạch) khó nóng chảy và khó hoà tan hơn polymer chưa khâu mạch.
e). Trong quá trình điện phân ở cực âm (cathode) luôn xảy ra sự khử.
Tổng số phát biểu đúng là
2.
3.
4.
5.
Biết độ tan trong nước của monosodium glutamate (mì chính hay bột ngọt) ở 60 oC là 112 g/100 g nước; ở 25 oC là 74 g/ 100 g nước. Có bao nhiêu gam monosodium glutamate kết tinh khi làm nguội 1000 g dung dịch monosodium glutamate bão hoà ở 60 oC xuống 25 oC? (giả thiết lượng nước bay hơi không đáng kể)
38 gam.
103,1 gam.
179,24 gam.
145,67 gam.
Tiến hành chuẩn độ dung dịch NaOH chưa biết nồng độ bẳng dung dịch chuẩn HCl 0,1M với chất chỉ thị phenolphthalein như sau:
Bước 1: Dùng pipette lấy 10 mL dung dịch HCl 0,1M vào bình tam giác, thêm 1-2 giọt chất chỉ thị phenolphthalein.
Bước 2: Cho dung dịch NaOH vào burette, điều chỉnh dung dịch trong burette về mức 0.
Bước 3: Mở khóa burette, nhỏ từng giọt dung dịch NaOH xuống bình tam giác (lắc đều trong quá trình chuẩn độ) cho đến khi dung dịch xuất hiện màu hồng nhạt (bền trong khoảng 10 giây) thì dừng chuẩn độ.
Bước 4: Ghi lại thể tích dung dịch NaOH đã dùng.
Nếu thể tích dung dịch NaOH đã dùng là 12,0 mL thì nồng độ mol/L của dung dịch NaOH ban đầu là bao nhiêu? (Làm tròn kết quả đến hàng phần trăm)
Bradykinin là một peptide được sản sinh từ huyết thanh trong máu, là chất làm giãn mạch mạnh và gây co cơ trơn, chất trung gian gây ra tình trạng viêm.
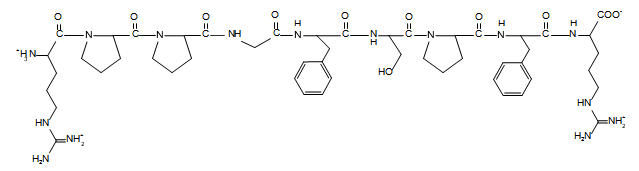
Công thức cấu tạo của Bradykinin
Trong Bradykinin có a đơn vị amino acid khác nhau và b liên kết peptide. Giá trị a và b viết liền là?
Vôi sống có nhiều ứng dụng như: sản xuất vật liệu xây dựng, vật liệu chịu nhiệt, khử chua đất trồng, tẩy uế, sát trùng, xử lí nước thải,... Hiện nay, nhiều lò nung vôi thủ công hoạt động tự phát, gây ảnh hưởng xấu đến môi trường xung quanh. Ở các lò nung vôi công nghiệp, quá trình kiểm soát phát thải ô nhiễm được thực hiện chặt chẽ hơn.
Xét một lò nung vôi công nghiệp sử dụng than đá làm nhiên liệu. Giả thiết đá vôi chỉ chứa CaCO3 và để phân hủy 1 kg đá vôi cần cung cấp một lượng nhiệt là 1800 kJ. Đốt cháy 1 kg than đá giải phóng ra một lượng nhiệt là 27000 kJ và có 50% lượng nhiệt này được hấp thụ ở quá trình phân hủy đá vôi. Công suất của lò nung vôi là 420 tấn vôi sống/ngày.
Tổng khối lượng (tấn) đá vôi và than đá mà lò nung vôi trên sử dụng mỗi ngày là bao nhiêu?
Để mạ đồng một vật dụng kim loại có diện tích bề mặt là 10 cm², người ta tiến hành điện phân dung dịch CuSO₄ với cực âm là vật dụng cần mạ và cực dương là lá đồng thỏi. Biết cường độ dòng điện không đổi là 2 A, hiệu suất điện phân là 90%, khối lượng riêng của tinh thể đồng là 8,94 g/cm³ và hằng số Faraday F = 96485 C/mol. Thời gian điện phân để lớp mạ có độ dày đồng nhất 0,1 mm là bao nhiêu phút? (làm tròn đến hàng đơn vị).
Copolymer được tạo thành từ 2 monomer khác nhau. Khi thực hiện phản ứng trùng hợp gồm ethylene và styrene thu được copolymer X. Phân tích thành phần nguyên tố của X thấy phần trăm khối lượng của carbon bằng 90,91%. Trong thành phần của X, cứ 1,0 mol styrene thì có bao nhiêu mol ethylene?
Chất nào sau đây không thuộc nhóm hợp chất carbohydrate?
Tinh bột.
Glucosamine.
Fructose.
Glucose.
Một vết nứt trên đường ray tàu hỏa có thể tích 3,36 cm3. Dùng hỗn hợp tecmite (Al và Fe2O3 theo tỉ lệ mol tương ứng 3 : 1) để hàn vết nứt trên. Biết: lượng Fe cần hàn cho vết nứt bằng 79% lượng Fe sinh ra; khối lượng riêng của sắt là 7,9 gam/cm3; chỉ xảy ra phản ứng khử Fe2O3 thành Fe với hiệu suất của phản ứng bằng 80%. Khối lượng của hỗn hợp tecmite tối thiểu cần dùng là bao nhiêu gam? Kết quả làm tròn đến hàng đơn vị.
Một trong những phương pháp điều chế ester là đun hồi lưu hỗn hợp ethanol, acetic acid và H2SO4 đặc trong bình cầu 1 có chứa đá bọt trong một khoảng thời gian nhất định. Sau đó chưng cất để thu được ester ở nhiệt độ thích hợp như hình bên:
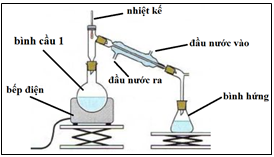
Nếu tiến hành thí nghiệm với 46,0 gam ethanol và 60,0 gam acetic acid, sau một thời gian thu được 22,0 gam chất lỏng ở bình hứng, thì kết luận rằng hiệu suất phản ứng ester hóa đúng bằng 25% (không làm tròn) là hoàn toàn chính xác.
Phản ứng giữa ethanol và acetic acid khi có mặt xúc tác H2SO4 gọi là phản ứng ester hóa.
Ngoài sản phẩm ester và nước thì trong quá trình thí nghiệm còn sinh ra một số sản phẩm phụ
Ethyl acetate hoặc ethyl ethanoate đều là tên gọi đúng của ester sinh ra trong thí nghiệm trên.
Tiến hành thí nghiệm sau:
Bước 1: Rót vào ống nghiệm 1 và 2, mỗi ống khoảng 3 ml dung dịch H2SO4 loãng và cho vào mỗi ống một mẩu Zn giống nhau. Quan sát bọt khí thoát ra.
Bước 2: Nhỏ thêm 2 - 3 giọt dung dịch CuSO4 vào ống 2. So sánh lượng bọt khí thoát ra ở 2 ống.
Ống 1 chỉ xảy ra ăn mòn hoá học còn ống 2 chỉ xảy ra ăn mòn điện hoá học.
Tốc độ bọt khí thoát ra ở hai ống là như nhau.
. Ở cả hai ống nghiệm, Zn đều bị oxi hoá thành Zn2+.
. Ở ống 2, thay dung dịch CuSO4 bằng dung dịch MgSO4 vẫn xuất hiện pin điện hóa.
Thành phần dịch vị dạ dày gồm 95% là nước, enzyme và hydrochloric acid. Sự có mặt của hydrochloric acid làm cho pH của dịch vị trong khoảng từ 2 – 3. Khi độ acid trong dịch vị dạ dày tăng thì dễ bị ợ chua, ợ hơi, ói mửa, buồn nôn, loét dạ dày, tá tràng. Để làm giảm bớt lượng acid dư trong dịch vị dạ dày người ta thường uống thuốc muối dạ dày “Nabica” từng lượng nhỏ và cách quãng.
Công thức hoá học của thuốc muối “Nabica” là NaHCO3.
Khi uống từng lượng nhỏ và cách quãng thuốc muối “Nabica” thì pH của dịch vị dạ dày sẽ tăng từ từ.
Khi uống thuốc muối “Nabica” thì sẽ sinh ra khí carbon dioxide.
Nếu có 10 mL dịch vị dạ dày và coi pH của dạ dày hoàn toàn do hydrochloric acid gây ra, để nâng pH của dạ dày từ pH = 1 lên pH = 2 ta cần dùng hết 0,0756 gam thuốc muối Nabica (với giả thiết Nabica là nguyên chất).
Cho các quá trình tạo phức chất bát diện sau:
Fe3+(aq) + 6H2O(l) [Fe(OH2)6]3+ (aq) (I)
[Fe(OH2)6]3+ (aq) + SCN− (aq) [Fe(OH2)5(SCN)]2+ (aq) + H2O(l) KC=1,4.102 (II)
[Fe(OH2)6]3+(aq) + F−(l) [Fe(OH2)5F]2+(aq) + H2O(l) KC=2,0.105 (III)
Biết dung dịch[Fe(OH2)6]3+ có màu vàng nâu, dung dịch [Fe(OH2)5(SCN)]2+ có màu đỏ, dung dịch [Fe(OH2)5F]2+ và các anion SCN−, F− đều không có màu.
Cho các phát biểu:
. Quá trình (I) xảy ra khi hoà tan iron(III) chloride trong nước. Kết thúc quá trình này thu được dung dịch có chứa lượng lớn cation Fe3+ và phức chất aqua [Fe(OH2)6]3+.
. So với anion F−, anion SCN− dễ thay thế phối tử H2O trong [Fe(OH)6]3+ hơn.
. Khi cho từ từ dung dịch KSCN vào dung dịch ở quá trình (III) thì dung dịch này sẽ có màu.
. Trong các quá trình (I), (II) và (III), mỗi phân tử H2O hoặc anion SCN− hay anion F− đều sử dụng số cặp electron hoá trị riêng như nhau để cho vào orbital trống của cation Fe3+.








