Đề thi tham khảo ôn thi THPT Hóa học có đáp án - Đề tham khảo số 4
28 câu hỏi
Chất nào sau đây là chất khí ở điều kiện thường?
Ethyl acetate.
Acetic acid.
Alanine.
Methylamine.
Fructose là hợp chất hữu cơ có nhiều trong mật ong, làm cho mật ong có vị ngọt sắc. Công thức phân tử của fructose là C6H12O6. Công thức đơn giản nhất của fructose là
C1,5H3O1,5.
CH2O.
C3H4O3.
CHO2.
Khí X làm đục nước vôi trong và được dùng làm chất tẩy trắng bột gỗ trong công nghiệp giấy. Chất khí X là
C O 2 .
S O 2 .
N H 3 .
O 3 .
Cho các phản ứng:
H2N–CH2–COOH + HCl → Cl–H3N+–CH2–COOH
H2N–CH2–COOH + NaOH → H2N–CH2–COONa + H2O.
Hai phản ứng trên chứng tỏ aminoacetic acid
chỉ có tính base.
chỉ có tính acid.
có tính oxi hoá và tính khử.
có tính chất lưỡng tính.
"Điện phân là quá trình oxi hóa khử xảy ra trên bề mặt các điện cực dưới tác dụng của...(1)... đi qua dung dịch chất điện li hoặc chất điện li …(2)…". Nội dung phù hợp trong ô trống (1), (2) lần lượt là
dòng điện xoay chiều, ở dạng khí.
dòng điện một chiều, nóng chảy.
dòng điện xoay chiều, nóng chảy.
dòng điện một chiều, ở dạng khí.
Nhận xét nào sau đây về phức chất là không đúng?
Nguyên tử trung tâm chỉ có thể là cation kim loại.
Thành phần của phức chất có nguyên tử trung tâm và phối tử.
Phối tử còn cặp electron chưa liên kết, có khả năng cho nguyên tử trung tâm.
Liên kết giữa phối tử và nguyên tử trung tâm là liên kết cho – nhận.
Trong dãy kim loại chuyển tiếp thứ nhất, hai kim loại nào sau đây đều là kim loại nhẹ ( D < 5g/cm3 ) ?
Cr, Mn.
Fe, Co.
Sc, Ti.
Ni, Cu.
Hemoglobin (huyết cầu tố) có phân tử khối là 14000. Mỗi phân tử hemoglobin chỉ chứa 1 nguyên tử sắt. Phần trăm về khối lượng của sắt trong hemoglobin là
0,80%.
0,40%.
4,00%.
0,25%.
Linoleic acid là acid béo thiết yếu cần thiết nhất trong cơ thể người do có thể bị chuyển hoá tạo ra nhiều acid béo omega-6 khác như arachidonic acid, docosatetraenoic acid. Arachidonic acid chiếm khoảng 10 – 20% hàm lượng acid béo phospholipid trong cơ xương và có cấu tạo như sau:
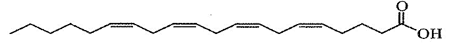
Số nguyên tử hydrogen trong một phân tử arachidonic acid là
20.
34.
30.
32.
Phát biểu nào sau đây về xà phòng là đúng?
Là chất giặt rửa tự nhiên.
Làm giảm chất lượng của sợi vải.
Dùng được với nước cứng (nước chứa nhiều ion Ca2+ và Mg2+).
Có thể sản xuất từ chất béo hoặc từ dầu mỏ.
Cho các cặp oxi hoá - khử của các kim loại và thế điện cực chuẩn tương ứng:
| Cặp oxi hoá-khử | F e 2 + / F e | S n 2 + / S n | Z n 2 + / Z n | N i 2 + / N i |
| Thế điện cực chuẩn (V) | -0,440 | -0,138 | -0,763 | -0,257 |
Trong số các kim loại trên, kim loại có tính khử yếu nhất là
Fe.
Sn.
Ni.
Zn.
Xăng E5 chứa 5% thể tích ethanol hiện đang được sử dụng phổ biến ở nước ta để thay thế một phần xăng thông thường. Một người đi xe máy mua 3 lít xăng E5 để đổ vào bình chứa nhiên liệu. Thể tích ethanol có trong 3 lít xăng trên là
150 mL.
138 mL.
100 mL.
75 mL.
Cho một mẩu Na vào dung dịch M g S O 4 dư, thu được kết tủa X và chất khí Y. Hai chất X, Y lần lượt là
Mg, O2.
Mg, H2.
Mg(OH)2, H2.
Mg(OH)2, O2.
Cho phản ứng oxi hoá - khử sau: X(s) + Y2+ (aq) → X2+(aq) + Y(s). Dựa vào phản ứng đã cho, hãy cho biết phát biểu nào sau đây đúng.
Chất X có tính khử mạnh hơn chất Y.
Ion Y2+ có tính khử mạnh hơn ion X2+.
Chất X có tính oxi hoá mạnh hơn chất Y.
Ion X2+ có tính oxi hoá manh hơn ion Y2+.
Một mẫu nước cam có khối lượng riêng 1,05 g/mL, chứa 2,5% fructose và 2,0% glucose về khối lượng. Khối lượng fructose trong 500 mL mẫu nước cam trên là
10,500 gam.
23,625 gam.
13,125 gam.
26,325 gam.
Pin Mặt Trời (pin quang điện) bao gồm nhiều tế bào quang điện làm biến đổi năng lượng ánh sáng thành năng lượng điện. Pin Mặt Trời mang đến rất nhiều lợi ích, nó được ứng dụng khá rộng rãi trong đời sống hiện nay. Phát biểu nào sau đây không đúng của việc sử dụng pin Mặt Trời?
Sử dụng nguồn năng lượng vô tận là ánh sáng mặt trời.
Tạo ra được nguồn năng lượng sạch.
Pin mặt trời tạo ra dòng điện nhờ phản ứng oxi hóa hydrogen.
Công suất sản sinh dòng điện phụ thuộc vào cường độ ánh sáng.
Các dung dịch muối ăn, phèn chua, nước vôi trong được kí hiệu ngẫu nhiên là X, Y, Z. Một số kết quả thí nghiệm được ghi ở bảng dưới đây.
| Mẫu thử | Thuốc thử | Hiện tượng |
| X | Dung dịch phenolphthalein | Chuyển màu hồng |
| Z | Dung dịch B a C l 2 | Có kết tủa trắng |
Các dung dịch ban đầu tương ứng với các kí hiệu là
Y, Z, X.
Z, X, Y.
X, Y, Z.
Y, X, Z.
Cho các polymer sau: PE, PVC, cao su buna, poly(methyl methacrylate), tơ olon, tơ nylon-6,6. Số polymer được điều chế bằng phản ứng trùng hợp là
2.
3.
5.
4.
Phân tích nguyên tố hợp chất hữu cơ mạch hở E cho kết quả phần trăm khối lượng carbon, hydrogen, oxygen lần lượt là 40,68%; 5,08%; 54,24%. Phương pháp phân tích phổ khối lượng (MS) cho biết E có phân tử khối bằng 118. Từ E thực hiện sơ đồ các phản ứng sau theo đúng tỉ lệ mol:
( 1 ) E + 2 N a O H → t o X + Y + Z ( 2 ) X + H C l → F + N a C l ( 3 ) Y + H C l → T + N a C l
Biết Z là alcohol đơn chức; F và T là các hợp chất hữu cơ; MF < MT.
Trong các phát biểu sau:
(1) Trong Y, số nguyên tử hydrogen bằng số nguyên tử oxygen.
(2) Chất F không có khả năng tham gia phản ứng tráng gương.
(3) Nhiệt độ sôi của Z thấp hơn nhiệt độ sôi của ethanol.
(4) Chất T thuộc loại hợp chất hữu cơ đa chức.
Có bao nhiêu số phát biểu đúng?
Saccharin \[\left( {{C_7}{H_5}{O_3}NS} \right)\] được biết đến là một loại đường hóa học, công dụng chính của saccharin là chất làm ngọt không chứa calo. Để so sánh độ ngọt của các chất tạo ngọt với một số loại đường, người ta chọn độ ngọt của saccharose làm đơn vị.
Chất ngọt | Glucose | Fructose | Saccharose | Saccharin |
Độ ngọt | 0,75 | 1,75 | 1,00 | 350 |
Để pha chế một loại nước giải khát, người ta dùng 30 g saccharose cho 1 lít nước. Nếu dùng 15 g saccharin thì sẽ pha được khoảng bao nhiêu lít nước có độ ngọt tương đối với loại nước giải khát đã nêu?
Hiện nay mạ điện được sử dụng rộng rãi trong thực tế, mạ điện là quá trình phủ một lớp kim loại lên bề mặt kim loại khác bằng phương pháp điện phân. Giả sử người ta cần mạ Ag lên một mặt của một chiếc đĩa kim loại hình tròn có bán kính 20cm, độ dày lớp mạ là 0,01 mm. Nếu được cung cấp nguồn điện một chiều có cường độ dòng điện I = 2A thì thời gian cần dùng là t giờ. Biết rằng khối lượng riêng của A g là 10,5 g/cm3; π =3,14; hằng số Faraday (F = 96 500 C/mol); hiệu suất điện phân là 100%. Giá trị của t là bao nhiêu? (Làm tròn kết quả đến hàng phần trăm)
Insulin là hormon có tác dụng điều tiết lượng đường trong máu. Thủy phân một phần insulin thu được heptapeptide X mạch hở. Khi thủy phân không hoàn toàn X, thu được hỗn hợp có chứa các peptide: Glu-Gln-Cys, Gly-Ile-Val, Gln-Cys-Cys, Val-Glu-Gln. Nếu đánh số thứ tự amino acid đầu N là số 1 thì amino acid Val ở vị trí số mấy?
Sulfuric acid có thể được điều chế từ quặng pyrite theo sơ đồ:
F e S 2 → S O 2 → S O 3 → H 2 S O 4
Thể tích (lít) của dung dịch H2SO498% (D = 1,82 g/mL) thu được từ 100kg quặng pyrite (chứa 80% F e S 2 ) . Biết hiệu suất của cả quá trình là 90%, các tạp chất trong quặng không chứa sulfur. (Làm tròn kết quả đến hàng đơn vị).
Để điều chế isoamyl acetate trong phòng thí nghiệm, một học sinh đã đun nóng 4 mL acetic acid CH3COOH (D = 1,05 g.mL-1) với 8 mL isoamyl alcohol (CH3)2CHCH2CH2OH (D = 0,81 g.mL-1), có dung dịch H2SO4 đặc làm xúc tác, thu được 6 mL isoamyl acetate (D = 0,88 g.mL-1). Tính hiệu suất của phản ứng (Làm tròn kết quả đến hàng phần trăm).
Tiến hành thí nghiệm theo các bước sau:
Bước 1: Cho 1 mL dung dịch AgNO3 1% vào ống nghiệm sạch.
Bước 2: Thêm từ từ từng giọt dung dịch NH3, lắc đều cho đến khi kết tủa tan hết.
Bước 3: Thêm tiếp khoảng 1 mL dung dịch glucose 1% vào ống nghiệm; đun nóng nhẹ.
. Sản phẩm hữu cơ thu được sau bước 3 là ammonium gluconate.
. Thí nghiệm trên chứng minh glucose có tính chất của polyalcohol.
. Sau bước 3, có lớp bạc kim loại bám trên thành ống nghiệm.
. Trong phản ứng ở bước 3, glucose đóng vai trò là chất khử.
Giá trị biến thiên enthalpy chuẩn của phản ứng nhiệt phân muối nitrate của kim loại nhóm IIA (R) (R(NO3)2(s) →to RO(s) + 2NO2(g) + O2(g)) theo bảng sau:
Muối R(NO3)2(s) | Mg(NO3)2 | Ca(NO3)2 | Sr(NO3)2 | Ba(NO3)2 |
| ΔrH298o(kJ) | 255,2 | 369,5 | 452,4 | 506,2 |
. Độ bền nhiệt của các muối nitrate của kim loại nhóm IIA có xu hướng tăng dần từ \[Mg{\left( {N{O_3}} \right)_2}\]tới\[Ba{\left( {N{O_3}} \right)_2}.\]
. Dựa vào bảng giá trị biến thiên enthalpy chuẩn ở trên có thể dự đoán xu hướng biến đổi độ bền nhiệt của\[R{\left( {N{O_3}} \right)_2}.\]
. Phản ứng nhiệt phân muối nitrate của kim loại nhóm IIA \[\left( {R{{\left( {N{O_3}} \right)}_2}} \right)\] là phản ứng oxi hoá – khử, trong đó vai trò chất oxi hoá là\[{R^{2 + }}.\;\]
. Nhiệt độ phân huỷ theo thứ tự sau: \[Mg{\left( {N{O_3}} \right)_2} < {\rm{ }}Ca{\left( {N{O_3}} \right)_2} < {\rm{ }}Sr{\left( {N{O_3}} \right)_2} < {\rm{ }}Ba{\left( {N{O_3}} \right)_2}.\;\]
Điện phân dung dịch NaCl có màng bán thấm ngăn giữa anode với cathode (các điện cực đều là các điện cực trơ). Màng bán thấm chỉ cho ion \[N{a^ + }\]đi qua. Sơ đồ bình điện phân như hình sau:
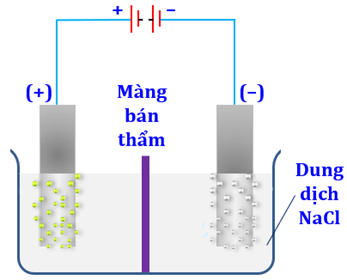
Tại cực âm (anode) xảy ra quá trình khử \[{H_2}O\]thành khí \[{H_2}\]và \[O{H^ - }.\]
Tại cực dương xảy ra quá trình oxi hóa \[C{l^ - }\](aq) thành khí \[C{l_2}.\]
Lượng (số mol) Na+ trong dung dịch giảm dần trong quá trình điện phân.
Phản ứng chung trong bình điện phân là: 2NaCl+2H2O →cmn®pdd 2NaOH+H2+Cl2.
Khi cho dung dịch ammonia dư vào dung dịch chứa phức chất \[{\left[ {Ni{{\left( {O{H_2}} \right)}_6}} \right]^{2 + }}\]và anion \[C{l^ - }\]thì có phản ứng sau:
[Ni(OH2)6]2+(aq) + 6NH3(aq) ® [Ni(NH3)6]2+(aq) + 6H2O (l) (*)
Trong điều kiện của phản ứng (*), phức chất \[{\left[ {Ni{{\left( {N{H_3}} \right)}_6}} \right]^{2 + }}\](aq) kém bền hơn phức chất \[{\left[ {Ni{{\left( {O{H_2}} \right)}_6}} \right]^{2 + }}\](aq).
Phản ứng (*) là phản ứng thế phối tử.
Dung dịch sau phản ứng có pH > 7.
Trong phản ứng không có sự thay đổi số oxi hoá của các nguyên tố.








