Đề thi tham khảo ôn thi THPT Hóa học có đáp án - Đề tham khảo số 10
27 câu hỏi
Trong các phản ứng hữu cơ thường có sự tạo thành các tiểu phân trung gian hoạt động như gốc tự do, carbanion, carbocation. Carbocation là ion mang điện tích dương trên nguyên tử carbon. Có bao nhiêu carbocation trong số các tiểu phân ( C H 3 ) 3 C + , ( C H 3 ) 2 C − H , C • H 3 và ( C H 3 ) 2 C + H ?
3.
2.
1.
4.
Cho một ống nghiệm chứa đầy khí NO2, đậy nút kín, ở nhiệt độ phòng (khoảng 25°C). Biết NO2 có thể chuyển hoá thành N2O4 và ngược lại N2O4 có thể chuyển lại thành NO2 theo phản ứng thuận nghịch sau:
2NO2(g, màu nâu đỏ) ⇌ N2O4(g, không màu) Δ r H 2 9 8 o = − 5 8 k J .
Nhận định nào sau đây đúng?
Nếu ngâm ống nghiệm vào cốc nước đá thì thấy màu của hỗn hợp khí đậm hơn.
Nếu ngâm ống nghiệm vào cốc nước đá thì thấy màu của hỗn hợp khí không thay đổi.
Nếu ngâm ống nghiệm vào cốc nước nóng (khoảng 70-80°C) thì thấy hỗn khí có màu đậm hơn.
Phản ứng thuận chuyển hoá NO2 thành N2O4 là phản ứng thu nhiệt.
Trong chế biến một số món ăn, đồ uống, người nội trợ thường cho các loại rau thơm (như rau húng quế, rau răm, …) vào sau khi thực phẩm đã được nấu chín. Nguyên nhân chính của việc làm này là
nếu cho vào lúc nấu sẽ sinh ra chất độc hại, ảnh hưởng đến sức khoẻ.
hạn chế sinh ra acid, gây ngộ độc cho người ăn.
các loại rau thơm thường chứa tinh dầu dễ bay hơi hoặc bị phân hủy ở nhiệt độ cao.
để rau ngấm gia vị làm tăng hương vị món ăn.
Đun hỗn hợp acetic acid và methyl alcohol với dung dịch sulfuric acid đặc xúc tác xảy ra phản ứng
trung hòa.
thủy phân.
xà phòng hóa.
ester hóa.
Phổ khối lượng (MS) là phương pháp hiện đại để xác định phân tử khối của các hợp chất hữu cơ. Kết quả phân tích phổ khối lượng cho thấy phân tử khối của hợp chất hữu cơ X là 60. Chất X có thể là
methanol.
ethyl acetate.
acetic acid.
ethanal.
Phản ứng xảy ra trong thí nghiệm nào sau đây thuộc loại phản ứng cộng?
Cho benzene tác dụng với bromine, có mặt FeBr3, đun nóng.
Cho toluene tác dụng với HNO3 đặc, có mặt H2SO4 đặc, đun nóng.
Cho toluene vào dung dịch KMnO4, đun nóng.
Cho benzene vào bình chứa khí chlorine, chiếu sáng.
Poly(vinyl chloride) (PVC) có công thức là
[ C H 2 − C H = C H − C H 2 ] n .
[ H N ( C H 2 ) 5 C O ] n .
[ C H 2 − C | H ] n C l .
[ C H 2 − C H 2 ] n .
Electron tự do trong mạng tinh thể kim loại phản xạ ánh sáng trong vùng nhìn thấy. Điều này giải thích tính chất vật lí nào sau đây của kim loại?
Tính dẫn nhiệt.
Tính dẫn điện.
Tính dẻo.
Tính ánh kim.
Đá vôi có thành phần chính là CaCO3. Tên của hợp chất này là
calcium oxide.
calcium hydroxide.
calcium sulfate.
calcium carbonate.
Thí nghiệm nào sau đây chỉ xảy ra sự ăn mòn hóa học ?
Nhúng thanh Zn vào dung dịch CuSO4.
Nhúng thanh Fe vào dung dịch CuSO4 và H2SO4 loãng.
Nhúng thanh Cu vào dung dịch AgNO3.
Nhúng thanh Cu vào dung dịch Fe2(SO4)3.
Trong pin Galvani Zn–Cu có phản ứng: Zn(s) + Cu2+(aq) → Cu(s) + Zn2+(aq). Quá trình xảy ra tại anode (cực âm) của pin là
Zn(s) → Zn2+(aq) + 2e.
Cu(s) → Cu2+(aq) + 2e.
Zn2+(aq) + 2e → Zn(s).
Cu2+(aq) + 2e → Cu(s).
Ở 20°C, hydroxide của kim loại nhóm IIA nào sau đây có độ tan lớn nhất ?
Sr(OH)2.
Ca(OH)2.
Mg(OH)2.
Ba(OH)2.
Cho các cặp oxi hóa - khử của các kim loại và thế điện cực chuẩn tương ứng:
| Cặp oxi hóa - khử | Li+/Li | Mg2+/Mg | Zn2+/Zn | Ag+/Ag |
| Thế điện cực chuẩn (V) | –3,040 | –2,356 | –0,762 | +0,799 |
Trong các kim loại trên, ở điều kiện chuẩn kim loại có tính khử mạnh nhất là
Li.
Zn.
Ag.
Mg.
Cho một số biện pháp sau:
(a) Đưa thêm hợp chất chứa chì vào xăng để làm tăng chỉ số octane của xăng.
(b) Đưa thêm chất xúc tác vào ống xả động cơ để chuyển hoá các khí thải độc hại.
(c) Sử dụng điện mặt trời, điện gió, thủy điện… thay cho nhiên liệu hóa thạch.
(d) Sử dụng tiết kiệm điện, nước, xăng dầu trong sinh hoạt và sản xuất.
(e) Tăng cường sử dụng các phương tiện cá nhân khi tham gia giao thông.
Số biện pháp góp phần làm giảm ô nhiễm môi trường gây ra do sử dụng nhiên liệu từ dầu mỏ là
4.
2.
3.
5.
Kim loại nhóm IA có khối lượng riêng nhỏ là do
bán kính nguyên tử nhỏ, cấu trúc mạng tinh thể kém đặc khít.
bán kính nguyên tử lớn, cấu trúc mạng tinh thể kém đặc khít.
bán kính nguyên tử nhỏ, cấu trúc mạng tinh thể đặc khít.
bán kính nguyên tử lớn, cấu trúc mạng tinh thể đặc khít.
Hợp chất nào dưới đây là α-amino acid?
CH3NH2.
CH3CH2COOH.
NH2CH2CH2COOH.
NH2CH2COOH.
Glutamic acid là một amino acid thiên nhiên có trong nhiều loại thực phẩm. Trong dung dịch, glutamic acid có thể tồn tại dưới dạng ion khác nhau phụ thuộc vào pH môi trường. Glutamic acid có cấu trúc gồm một nhóm amino (–NH2) và hai nhóm carboxyl (–COOH). Điểm đẳng điện (pI) của glutamic acid là 3,08 (pI là giá trị pH mà khi đó amino acid có nồng độ ion lưỡng cực là cực đại). Khi pH < pI thì amino acid tồn tại chủ yếu ở dạng cation, còn khi pH > pI thì amino acid tồn tại chủ yếu ở dạng anion.
Cho các nhận định sau:
(a) Glutamic acid thuộc loại hợp chất hữu cơ đa chức, trong phân tử chứa hai loại nhóm chức.
(b) Ở pH = 3,08 thì glutamic acid tồn tại chủ yếu ở dạng anion.
(c) Khi đặt trong một điện trường ở pH = 7,0 thì glutamic acid di chuyển về phía cực dương.
(d) Trong dung dịch pH = 6,0 có thể tách hỗn hợp gồm glutamic acid và lysine (pI = 9,74) bằng phương pháp điện di.
Các nhận định đúng là
(a), (b).
(a), (c).
(b), (d).
(c), (d).
Xà phòng hóa hoàn toàn triglyceride X trong dung dịch NaOH dư, thu được glycerol, sodium stearate (C17H35COONa). Phân tử khối của X là bao nhiêu?
Xăng E5 là một loại xăng sinh học, trong đó có pha 5,0% ethanol (cồn sinh học) và 95,0% xăng truyền thống từ dầu mỏ. Lên men 1,2 tấn gạo chứa 62,6% khối lượng là tinh bột thành ethanol, phần còn lại là các chất không lên men thành ethanol với hiệu suất 81,0% cho toàn quá trình. Dùng toàn bộ lượng ethanol thu được để sản xuất xăng E5. Biết khối lượng riêng của ethanol là 0,8 kg/L. Tính thể tích (L) xăng E5 thu được (làm tròn kết quả đến hàng đơn vị).
Máy tạo oxygen y tế sử dụng phương pháp điện phân nước (trong môi trường acid) để cung cấp oxygen. Quá trình điện phân nước được biểu diễn bằng các bán phản ứng như sau:
(-) Cathode: 2H+ + 2e → H2
(+) Anode: 2H2O → O2 + 4H+ + 4e
Biết chỉ thêm đúng dịch nước (trong môi trường acid) vào máy ban đầu, trong quá trình hoạt động không bổ sung thêm nước. Biết một máy tạo được 1 lít oxygen (đkc) mỗi phút; máy hoạt động 30 lần mỗi ngày với mỗi lần 15 phút. Nước sử dụng có khối lượng riêng là 1 g/mL. Cứ trung bình 10 lần hoạt động, lượng nước trong máy chỉ còn 20% so với ban đầu, nên cần đổ thêm nước đầy về mức ban đầu. Giả thiết hiệu suất điện phân nước là 100% thì tổng lượng nước cần sử dụng để vận hành máy tạo oxygen trong một ngày là bao nhiêu mL (làm tròn đến hàng đơn vị).
Để kiểm nghiệm hàm lượng sắt trong viên thuốc (chứa nguyên tố sắt ở dạng muối Fe(II) cùng một số chất khác - tá dược), học sinh tiến hành hoà tan 5 viên thuốc có tổng khối lượng 1,20 gam trong dung dịch sulfuric acid 1,0 M rồi tiếp tục pha thành 250,0 mL dung dịch X. Chuẩn độ lượng Fe(II) trong 25,00 mL dung dịch X bằng dung dịch KMnO4 0,015 M đến khi xuất hiện màu hồng nhạt thì dừng. Lặp lại thí nghiệm chuẩn độ thêm 2 lần nữa. Thể tích trung bình của dung dịch KMnO4 sau 3 lần chuẩn độ là 5,75 mL. Tính khối lượng nguyên tố sắt trong mỗi viên thuốc (theo mg, làm tròn kết quả đến hàng phần mười).
Công thức cấu tạo thu gọn của ethylmethylamine là
CH3NH2.
CH3CH2NH2.
CH3CH2CH2NH2.
CH3NHCH2CH3.
Vôi sống có nhiều ứng dụng như sản xuất vật liệu xây dựng, vật liệu chịu nhiệt, khử chua đất trồng, tẩy uế, sát trùng, xử lí nước thải, … Một lò nung vôi có công suất 201,60 tấn CaO/ngày theo phương trình nhiệt hoá học sau:
CaCO3(s) → CaO(s) + CO2(g) ΔrH298o=179,20 kJ
Lò nung sử dụng nhiệt lượng từ đốt cháy than đá (giả sử chỉ chứa carbon và tạp chất trơ, sản phẩm cháy chỉ có CO2 với ΔfH298o= –393,50 kJ/mol) và chỉ có 71,68% lượng nhiệt đốt cháy than sử dụng cho phản ứng nung vôi. Lượng khí CO2 (đkc) đã thải ra trong một ngày của lò nung vôi trên là a triệu L. Tính giá trị của a (làm tròn kết quả đến hàng đơn vị).
Rutin có nhiều trong hoa hoè còn được gọi là vitamin P. Rutin có công thức cấu tạo như hình bên dưới: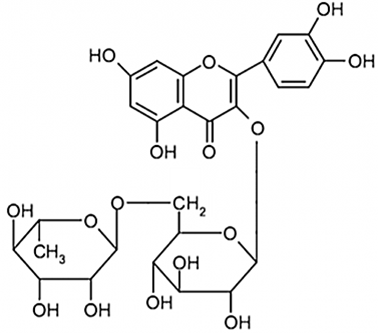
.Rutin có chứa 27 nguyên tử C.
. Trong phân tử rutin có một gốc α-fructose.
. Một mol rutin tác dụng được với tối đa 6 mol NaOH trong dung dịch.
. Khối lượng rutin thành phẩm có độ tinh khiết 94,10% thu được bằng phương pháp chiết dùng nước nóng từ 300 kg nụ hoa hòe khô (có 28,9% rutin về khối lượng), với hiệu suất của quá trình chiết đạt 11,29% là 10,4 kg (kết quả làm tròn đến hàng phần mười).
Một nhóm học sinh tìm hiểu về đặc điểm và tính chất giặt rửa của xà phòng. Giả thuyết của nhóm học sinh là “xà phòng làm tăng khả năng hoà tan các vết bẩn trong mọi loại nước”. Để kiểm tra giả thuyết trên, nhóm học sinh đã thực hiện thí nghiệm như sau:
- Lấy 3 ống nghiệm được đánh số thứ tự từ 1 đến 3.
- Ống nghiệm (1): cho 3 mL nước cất và vài giọt dầu ô-liu (RCOO)3C3H5 vào, lắc mạnh, để yên thấy dầu ô-liu không tan, nổi lên trên mặt nước.
- Ống nghiệm (2): cho 3 mL dung dịch xà phòng sodium RCOONa và vài giọt dầu ô-liu (RCOO)3C3H5 vào, lắc mạnh, để yên thấy hỗn hợp chuyển thành nhũ tương bền màu trắng như sữa.
- Ống nghiệm (3): cho 3 mL dung dịch xà phòng sodium RCOONa và 1 mL dung dịch CaCl2 5%, thấy xuất hiện hợp chất không tan trong nước, nổi trên mặt dung dịch.
. Xà phòng có khả năng làm tăng sức căng bề mặt của các giọt dầu ô-liu.
. Dầu ô-liu không rửa sạch được bằng nước mà cần chất giặt rửa có hoạt tính bề mặt.
. Hợp chất không tan trong nước, nổi trên mặt dung dịch là (RCOO)2Ca (s), theo phương trình:
2RCOONa(aq) + CaCl2(aq) → (RCOO)2Ca(s) + 2NaCl(aq).
. Không nên dùng xà phòng để giặt rửa với nước cứng.
Thực hiện thí nghiệm theo các bước sau:
• Bước 1: Hoà tan hoàn toàn một lượng muối CuSO4 khan màu trắng vào nước, thu được dung dịch X có màu xanh do hình thành phức bát diện [Cu(OH2)6]SO4(aq).
• Bước 2: Thêm tiếp dung dịch NH3 vào dung dịch X, thu được kết tủa màu xanh nhạt [Cu(OH)2(OH2)4](s).
• Bước 3: Tiếp tục thêm dung dịch NH3 đặc đến dư vào đến khi kết tủa bị hoà tan hoàn toàn, thu được dung dịch Y có màu xanh lam [Cu(NH3)4(OH2)2](OH)2(aq).
Màu xanh của kết tủa và dung dịch được lí giải là do sự hình thành các ion phức trong hợp chất phức gây ra.
. Trong quá trình hình thành phức chất [Cu(OH2)6]SO4(aq), mỗi phân tử H2O cho một electron chưa liên kết trở thành phối tử.
. Số oxi hoá của nguyên tử trung tâm trong [Cu(OH2)6]SO4 là +2.
.Ở bước (2) và bước (3) các phản ứng xảy ra đều có sự thay thế một phần phối tử trong phức chất.
. Trong hợp chất phức [Cu(NH3)4(OH2)2](OH)2, phối tử tạo phức là NH3, H2O và OH–.
Cho các phản ứng xảy ra theo sơ đồ sau (theo đúng tỉ lệ mol):
2X + 2H2O (đpdd có màng ngăn) → 2X1 + Cl2↑ + X2↑ (1)
X1 + X3 → CaCO3 + X4 + H2O (2)
KHSO4 + X4 → X5 + X6↑ + H2O (3)
. Nước chứa nhiều X3 thì có tính cứng tạm thời.
. Đốt cháy X trên ngọn lửa đèn khí không màu, thấy ngọn lửa có màu tím.
. Thực hiện phản ứng (1) không có màng ngăn thu được nước Javel.
. X4 còn được gọi là baking soda.








