Đề thi tham khảo ôn thi THPT Hóa học có đáp án - Đề tham khảo số 2
28 câu hỏi
Tên gọi của C H 3 C O O C H 2 C H 3 là
ethyl acetate.
methyl propionate.
propyl acetate.
methyl acetate.
Mùi tanh của cá là do hỗn hợp một số amine (nhiều nhất là trimethylamine) và một số chất khác gây nên. Công thức của trimethylamine là
C 2 H 5 N H 2 .
C H 3 N H 3 .
( C H 3 ) 3 N .
( C H 3 ) 2 N H .
Cách làm nào sau đây là đúng trong việc khử chua bằng vôi và bón phân đạm (urea hoặc ammonium) cho lúa?
Bón đạm và vôi cùng lúc.
Bón đạm trước rồi vài ngày sau mới bón vôi khử chua.
Bón vôi khử chua trước rồi vài ngày sau mới bón đạm.
Bón vôi khử chua trước rồi bón đạm ngay sau khi bón vôi.
Phổ khối lượng (MS) là phương pháp hiện đại để xác định phân tử khối của các hợp chất hữu cơ. Kết quả phân tích phổ khối lượng cho thấy phân tử khối của hợp chất hữu cơ X là 60. Chất X có thể là
acetic acid.
methyl acetate.
acetone.
triethylamine.
Trong nước, thế điện cực chuẩn của kim loại M n + / M càng lớn thì dạng khử có tính khử ...(1)... và dạng oxi hoá có tính oxi hoá ...(2)... Cụm từ cần điền vào (1) và (2) lần lượt là
càng mạnh và càng yếu.
càng mạnh và càng mạnh.
càng yếu và càng yếu.
càng yếu và càng mạnh.
Khi so sánh kim loại Fe với Ca, nhận định nào sau đây không đúng?
Fe có khối lượng riêng lớn hơn.
Fe có độ cứng cao hơn.
Ca có tính khử mạnh hơn.
Ca có nhiệt độ nóng chảy cao hơn.
Các động vật ăn cỏ như trâu, bò, dê, cừu,... có thể chuyển hoá cellulose trong thức ăn thành glucose bằng enzyme cellulase để cung cấp năng lượng cho cơ thể. Phản ứng chuyển hoá cellulose thành glucose thuộc loại phản ứng nào sau đây?
Cắt mạch polymer.
Giữ nguyên mạch polymer.
Tăng mạch polymer
Trùng ngưng.
Cho thế điện cực chuẩn của một số cặp oxi hóa khử như sau:
Cặp oxi hóa khử | \[F{e^{3 + }}/F{e^{2 + }}\] | \[C{u^{2 + }}/Cu\] | \[Z{n^{2 + }}/Zn\] |
Thế điện cực chuẩn (Eo, V) | 0,771 | 0,34 | -0,762 |
Nhận xét nào sau đây đúng?
Ở điều kiện chuẩn tính oxi hóa của ion C u 2 + lớn hơn Z n 2 + nhưng yếu hơn F e 3 + .
Trong dung dịch kim loại Cu khử được ion Z n 2 + và ion F e 3 + .
Sức điện động của pin Zn-Cu có giá trị là 0,42V.
Trong pin điện Zn-Cu, kim loại Zn đóng vai trò là cực âm (cathode).
Xét quá trình điện phân dung dịch NaCl bão hoà không có màng ngăn. Phát biểu nào sau đây đúng?
Quá trình xảy ra tại cathode là Na++1e →Na.
Quá trình xảy ra tại anode là 2H2O+2e→H2+ 2OH−.
Dung dịch thu được sau phản ứng là dung dịch NaOH.
Cho mẩu giấy màu vào dung dịch sau phản ứng thấy mẩu giấy mất màu.
Trong cơ thể người, ion M g 2 + ( Z = 1 2 ) tham gia cấu trúc tế bào, tổng hợp protein và chất sinh năng lượng ATP. Tổng số hạt proton và electron của ion M g 2 + là
26.
24.
22.
12.
Khi nhiệt kế thuỷ ngân vỡ, rắc chất bột nào sau đây lên thuỷ ngân rơi vãi sẽ chuyển hoá chúng thành hợp chất bền, ít độc hại?
Than đá.
Đá vôi.
Muối ăn.
Sulfur.
Ô nhiễm môi trường do chất dẻo và rác thải nhựa đang là vấn đề được quan tâm hàng đầu. Cho các phát biểu sau:
(a) Các loại nhựa được tạo ra từ chất dẻo khi thải ra môi trường mất nhiều thời gian để phân hủy.
(b) Rác thải nhựa sau thu gom nên đốt hoặc chôn lấp để giảm thiểu lượng rác thải.
(c) Sử dụng vật liệu phân hủy sinh học để thay thế một số loại chất dẻo.
(d) Nên phân loại rác thải tại các nguồn để đưa ra cách xử lí.
Số phát biểu đúng là
1.
4.
2.
3.
Phức Ethylenediaminetetraacetic acid copper(II) disodium complex ( E D T A − C u N a 2 ) thường được sử dụng trong nông nghiệp để cung cấp đồng cho đất trồng có công thức như sau:
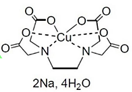
Nguyên tử trung tâm của phức này là
N O 3 − .
N a + .
C u 2 + .
EDTA.
Nhỏ vài giọt dung dịch NaCl vào ống nghiệm chứa dung dịch A g N O 3 , thu được kết tủa trắng. Tiếp tục nhỏ vào ống nghiệm dung dịch N H 3 đến dư thấy kết tủa tan, phức chất được tạo thành có công thức?
[ A g ( N H 3 ) 2 ] + .
[ A g ( N H 3 ) 6 ] + .
[ A g ( N H 3 ) 2 ] 2 + .
[ A g ( N H 3 ) 2 ] 4 + .
Insulin là hoocmon của cơ thể có tác dụng điều tiết lượng đường trong máu. Thủy phân một phần insulin thu được heptapeptide (X). Khi thủy phân không hoàn toàn X thu được hỗn hợp các peptide trong đó có các peptide sau: Ser-His-Leu; Val-Glu-Ala; His-Leu-Val; Gly-Ser-His. Nếu đánh số amino acid đầu N trong X là số 1 thì amino acid ở vị trí số 1 và số 5 lần lượt là
Ser và Glu.
Gly và Val.
Val và His.
Glu và Leu.
Trong dung dịch, tồn tại cân bằng hóa học giữa ion lưỡng cực với các dạng ion của amino acid đó. Ví dụ:
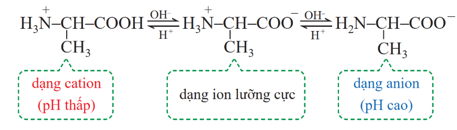
Các amino acid có khả năng di chuyển khác nhau trong điện trường tùy thuộc vào pH của môi trường (tính chất điện di). Cho các nhận định sau:
(a) Trong môi trường acid mạnh (pH khoảng 1 – 2), glycine tồn tại chủ yếu ở dạng cation, bị di chuyển về phía điện cực âm của điện trường.
(b) Ở pH khoảng 6, glycine tồn tại chủ yếu ở dạng ion lưỡng cực, không bị di chuyển trong điện trường.
(c) Ở pH lớn hơn 10, glycine tồn tại chủ yếu ở dạng anion, bị di chuyển về phía điện cực dương của điện trường.
(d) Ở pH = 6, ion tồn tại chủ yếu đối với Ala là cation. Vì vậy, khi đặt trong điện trường sẽ di chuyển về cực âm.
Các nhận định đúng là
(a), (b), (c).
(a), (c), (d).
(b), (c), (d).
(a), (b), (d).
Thực hiện bốn phản ứng hoá học theo sơ đồ:
NaOH → + CO2 X → + NaOH Y → + Ca(OH)2 Z → t o T
Biết X, Y, Z, T là các hợp chất của kim loại. Công thức hoá học của T là
N a O H .
C a C O 3 .
N a 2 C O 3 .
CaO.
Để sản xuất m tấn xà phòng (có chứa 75% muối sodium của acid béo, còn lại là chất độn), người ta xà phòng hóa hoàn toàn 1 tấn chất béo trung tính bằng dung dịch chứa 150 kg NaOH vừa đủ. Xác định giá trị m (Làm tròn kết quả đến phần trăm).
Người ta mạ nickel lên mặt vật kim loại bằng phương pháp mạ điện, dung dịch điện phân chứa N i S O 4 , cực dương là Ni kim loại, cực âm là vật kim loại cần mạ. Nếu dòng điện có cường độ 1,5 A chạy qua dung dịch trong 2 giờ thì khối lượng nickel được mạ lên vật là bao nhiêu? (Cho biết khối lượng mol của Ni = 58,7 g/mol, hằng số Faraday F = 96500 C/mol, hiệu suất quá trình điện phân là 100%). (Làm tròn kết quả đến hàng phần mười)
Nguyên liệu nào sau đây dùng để điều chế chất giặt rửa tổng hợp?
Dầu mỏ.
Mỡ động vật.
Mật ong.
Tinh bột.
Cho phản ứng:
C4H10(g) + 6,5O2(g) →4CO2(g) + 5H2O (l) (1)
Dựa vào bảng số liệu sau:
Liên kết | C−H | C−C | O=O | C=O | H-O |
EbkJ.mol−1 | 418 | 346 | 494 | 732 | 459 |
Một bình gas chứa 12 kg khí trong đó butane (C4H10) chiếm 96,67% về khối lượng còn lại là tạp chất không cháy. Một hộ gia đình cần đốt gas để cung cấp 10 000 kJ nhiệt trong mỗi ngày. Biết hiệu suất hấp thụ nhiệt là 80%. Sau bao nhiêu ngày thì hộ gia đình trên dùng hết bình gas 12 kg? ((làm tròn đến hàng đơn vị).
Cho các phát biểu sau:
(1) Oxi hóa glucose bằng thuốc thử Tollens thu được sản phẩm cuối cùng là gluconic acid.
(2) Dung dịch saccharose có thể hòa tan trong môi trường kiềm ở điều kiện thường.
(3) Cellulose trinitrate là nguyên liệu để sản xuất thuốc súng không khói.
(4) Trong amilopectin, các gốc α-glucose chỉ liên kết với nhau bằng liên kết α-1,4-glycoside.
(5) Glucose và fructose có thể chuyển hóa lẫn nhau trong môi trường kiềm.
(6) Glucose là hợp chất hữu cơ đa chức có công thức dạng
Gắn số thứ tự theo chiều tăng dần các phát biểu đúng (ví dụ 123; 146; 2356;…).
Muối Mohr là một muối kép ngậm nước được tạo thành từ hỗn hợp cùng số mol F e S O 4 . 7 H 2 O và ( N H 4 ) 2 S O 4 khan:
FeSO4.7H2O + (NH4)2SO4→ FeSO4.(NH4)2SO4.6H2O + H2O
Cho độ tan của muối Mohr ở 2 0 ° C là 26,9 gam/100 gam H2O và ở 8 0 o C là 73,0 gam/100 gam H2O. Tính khối lượng (đơn vị gam) của muối F e S O 4 . 7 H 2 O cần thiết để tạo thành dung dịch muối Mohr bão hòa 8 0 o C , sau khi làm nguội dung dịch này xuống 2 0 ° C để thu được 60 gam muối Mohr tinh thể và dung dịch bão hòa. Giả thiết trong quá trình kết tinh nước bay hơi không đáng kể (làm tròn đến hàng phần mười).
Một nhà máy sản xuất túi nilon tử PE cần sản xuất túi đựng hình chữ nhật có kích thước là 20 × 30 cm (hình dưới), bề dày của lớp nylon là 0,02 cm. Biết hiệu suất phản ứng trùng hợp ethylene để điều chế PE là 60%, quá trình chuyển nhựa thành túi có hiệu suất là 95% và biết khối lượng riêng của nhựa PE là \(0,95g/c{m^3}\). Tính khối lượng nguyên liệu ethylene dùng để sản xuất đơn hàng 100 000 túi trên (đơn vị: tấn).

Trong thực tiễn, độ cứng của nước thường được tính theo CaCO3, tức là coi nồng độ mol Ca2+ và Mg2+ thành nồng độ mol của Ca2+, tiếp đó quy đổi nồng độ mol của Ca2+ thành số mg CaCO3 trong 1 lít nước.
Mức độ cứng | Nồng độ CaCO3 (mg/L) | Đặc điểm |
Nước mềm | 0 – 60 | Ít khoáng chất, tạo nhiều bọt khi dùng xà phòng. |
Nước hơi cứng | 61 – 120 | Bắt đầu có dấu hiệu của độ cứng. |
Nước cứng trung bình | 121 – 180 | Xuất hiện cặn vôi khi đun nóng, giảm hiệu quả của xà phòng. |
Nước cứng | 181 – 300 | Tạo nhiều cặn vôi, ảnh hưởng đến sinh hoạt và công nghiệp. |
Nước rất cứng | > 300 | Rất nhiều cặn vôi, gây nhiều vấn đề nghiêm trọng cho thiết bị và sức khỏe. |
Khi phân tích một loại nước tự nhiên thấy đồng thời các muối với khối lượng tương ứng như bảng sau:
Muối | Ca(HCO3)2 | MgSO4 | NaHCO3 |
Khối lượng (mg/L) | 300,8 | 42,6 | 80,5 |
. Tổng khối lượng của ion Ca2+ và Mg2+ có trong loại nước tự nhiên trên là 78,6 mg/L.
. Nước tự nhiên trên thuộc loại nước cứng trung bình.
. Có thể làm mềm loại nước trên bằng phương pháp trao đổi ion.
. Có thể làm mềm loại nước trên bằng cách đun sôi.
Melamine là hợp chất hữu cơ tan ít trong nước, kết dính tốt được dùng trong chế tạo keo dính, nội thất. Một số cơ sở sản xuất sữa thường thêm melamine vào sản phẩm để tạo hàm lượng đạm giả trong sữa, gây nguy hại đến sức khỏe. Bê bối sữa nghiêm trọng năm 2008 đã xảy ra với người tiêu dùng Trung Quốc, khoảng 300.000 trẻ em bị đầu độc khi các nhà cung cấp bổ sung melamine vào sữa bột để tăng chỉ số hàm lượng protein trong các cuộc kiểm tra. Melamine có công thức cấu tạo như hình bên.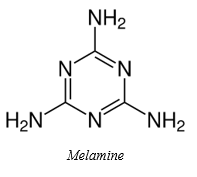
Melamine thuộc loại arylamine và có tính base.
Một phân tử melamine có công thức đơn giản nhất là và có 15 liên kết sigma (σ).
Melanine được dùng như một loại keo để sản xuất giấy trang trí phủ melamine (một loại vật liệu quan trọng trong ngành gỗ công nghiệp với ưu điểm màu sắc phong phú, bền màu, chống thấm nước,…).
Muốn tăng 1 độ đạm (1 g nitrogen) cho sữa tươi thì phải thêm vào 1 lít sữa khoảng 1500 mg melamine.
Trong phòng thí nghiệm, một nhóm học sinh tìm hiểu ảnh hưởng của thời gian lưu giữ tới nồng độ FeSO₄ trong dung dịch. Giả thuyết của nhóm học sinh là: “Khi để lâu, nồng độ FeSO4 trong dung dịch giảm.” Nhóm học sinh chuẩn bị 250,0 mL dung dịch FeSO4 (nồng độ khoảng 0,1 M) đựng trong bình kín (dán nhãn bình là Y) và tiến hành các thí nghiệm ở hai thời điểm khác nhau như sau:
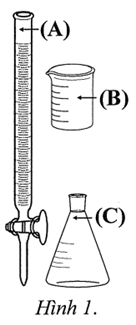
- Ngày thứ nhất:
Bước 1: Lấy 10,00 mL dung dịch trong bình Y cho vào bình tam giác rồi thêm tiếp 5 mL dung dịch H2SO4 2 M.
Bước 2: Chuẩn độ dung dịch trong bình tam giác bằng dung dịch KMnO4 2,20×10⁻2 M đến khi xuất hiện màu hồng nhạt (bền trong khoảng 20 giây) thì dừng. Ghi lại thể tích dung dịch KMnO4 đã dùng.
Lặp lại thí nghiệm chuẩn độ thêm 2 lần. Thể tích trung bình của dung dịch KMnO4 sau 3 lần chuẩn độ là 10,70 mL. Nồng độ của Fe(II) xác định được là C1 M.
- Ngày thứ tám:
Xác định lại hàm lượng Fe(II) của dung dịch chứa trong bình Y theo các bước tương tự như ngày thứ nhất. Thể tích trung bình của dung dịch KMnO4 sau 3 lần chuẩn độ là 9,92 mL. Nồng độ của Fe(II) xác định được là C2 M.
Nồng độ dung dịch KMnO4 như nhau trong các thí nghiệm chuẩn độ. Sự thay đổi nồng độ của Fe(II) (q%) được tính theo công thức:
\[{\rm{q\% }} = \frac{{{{\rm{C}}_{\rm{1}}} - {{\rm{C}}_2}}}{{{{\rm{C}}_1}}} \times 100{\rm{\% }}\]
Khi chuẩn độ, dung dịch KMnO₄ được nhỏ trực tiếp vào bình tam giác từ dụng cụ kí hiệu là (B) được minh họa ở Hình 1.
Giá trị của q là 7,9. (Kết quả các phép tính trung gian không được làm tròn, chỉ kết quả cuối cùng được làm tròn đến hàng phần mười.)
Giá trị của C2 là 0,109. (Kết quả các phép tính trung gian không được làm tròn, chỉ kết quả cuối cùng được làm tròn đến hàng phần nghìn.)
Kết quả thu được từ các thí nghiệm phù hợp với giả thuyết ban đầu của nhóm học sinh.
Phức chất có vai trò quan trọng làm xúc tác trong tổng hợp hữu cơ. Minh chứng cho vai trò to lớn đó là giải Nobel được trao cho ba nhà khoa học R. F. Heck, E. Negishi và A. Suzuki năm 2010 về phản ứng ghép mạch C=C sử dụng xúc tác là phức chất \[\left[ {Pd{{\left( {P{{\left( {{C_6}{H_5}} \right)}_3}} \right)}_4}} \right],\]còn được gọi là Tetrakis.
Phức chất Tetrakis có 4 phối tử triphenylphosphine \[\left( {P{{\left( {{C_6}{H_5}} \right)}_3}} \right).\]
Phức chất Tetrakis có dạng hình học bát diện.
Trong phức chất Tetrakis, nguyên tử trung tâm Pd đã nhận 4 cặp electron của các phối tử.
Nguyên tử trung tâm trong phức chất Tetrakis là \[P{d^{2 + }}.\]








