Đề thi tham khảo ôn thi THPT Hóa học có đáp án - Đề tham khảo số 7
28 câu hỏi
Chất nào sau đây không làm mất màu nước bromine?
Stearic acid.
Acetaldehyde.
Phenol.
Triolein.
Trong quá trình điện phân dung dịch CuSO4 với anode được làm bằng điện cực trơ, ở anode xảy ra quá trình
2H2O → 4H+ + O2 + 4e.
Cu → Cu2+ + 2e.
Cu2+ + 2e → Cu.
2H2O + 2e → 2OH- +H2.
Peptide nào sau đây không có phản ứng màu biuret?
Val-Ala-Gly-Gly.
Ala-Gly-Val.
Gly-Ala-Gly.
Ala-Gly.
Polystyrene (PS) là chất nhiệt dẻo thường được sử dụng để sản xuất đồ nhựa như: cốc, chén dùng một lần hoặc hộp đựng thức ăn mang về tại các cửa hàng. Monomer được dùng để điều chế PS là
CH2=CH2.
CH2=CH-CH=CH2.
C6H5CH=CH2.
CH2=CH-CH3.
Bước nào sau đây không đúng trong quá trình tái chế kim loại?
Đúc khuôn và xử lý thành phẩm sau khi tinh luyện.
Trộn thêm rác thải nhựa và giấy vào phế liệu để tăng thể tích nung chảy.
Nung chảy phế liệu ở nhiệt độ thích hợp.
Phân loại và thu gom kim loại phế liệu.
Chất X có công thức cấu tạo CH3NHC2H5. Tên gọi của X là
dimethylamine.
methylamine.
propylamine.
ethylmethylamine.
Dạng tồn tại chủ yếu của alanine trong môi trường acid mạnh (pH = 2) là
H2N-CH(CH3)-COO−.
H2NCH(CH3)COOH.
H2N-CH2-COO−.
+H3NCH(CH3)COOH.
Chọn phát biểu đúng về điều chế kim loại:
Dùng CO khử oxide kim loại có thể điều chế được các kim loại Fe, Ca, Cu.
Trong công nghiệp, nhôm được sản xuất bằng cách điện phân dung dịch AlCl3.
Các kim loại Mg, Zn, Ag có thể điều chế bằng phương pháp thủy luyện hay nhiệt luyện.
Trong quá trình điện phân nóng chảy MgCl2 để điều chế Mg, ở cathode xảy ra quá trình khử ion Mg2+.
Cho biết số thứ tự của K trong bảng tuần hoàn là 19. Số electron ở lớp ngoài cùng của nguyên tử K là
4.
3.
2.
1.
Nguyên tắc tách kim loại là
oxi hóa nguyên tử kim loại thành ion.
khử nguyên tử kim loại thành ion.
khử ion kim loại thành nguyên tử.
oxi hóa kim loại thành nguyên tử.
Cho bảng giá trị thế điện cực chuẩn của các cặp oxi hóa – khử như sau:
| Cặp oxi hóa – khử | Al3+/Al | Zn2+/Zn | Fe2+/Fe | Cu2+/Cu | Ag+/Ag |
| Thế điện cực chuẩn (V) | -1,676 | -0,763 | -0,440 | +0,340 | +0,799 |
Pin Galvani X được thiết lập từ hai trong số các cặp oxi hóa – khử trên có sức điện động chuẩn là 2,475 V. Pin Galvani X là pin
Fe – Ag.
Fe – Cu.
Al – Zn.
Al – Ag.
Trong pin điện hóa, quá trình oxi hóa
chỉ xảy ra ở cực dương.
chỉ xảy ra ở cực âm.
xảy ra ở cả hai cực.
không xảy ra ở cả hai cực.
Phức chất X có nguyên tử trung tâm Pt2+ và chỉ có phối tử CN-. Biết X có dạng hình học vuông phẳng, công thức của phức chất X là
[Pt(CN)2]2+.
[Pt(CN))4]2+.
[Pt(CN)6]4-.
[Pt(CN)4]2-.
Phương pháp nào dưới đây được dùng để sản xuất bơ nhân tạo?
Hydrogen hóa acid béo không no.
Xà phòng hóa chất béo lỏng.
Trung hòa acid béo không no.
Hydrogen hóa chất béo lỏng.
Ở nhiệt độ cao, CO khử được oxide nào sau đây?
K2O.
BaO.
Li2O.
Fe2O3.
Cho bảng giá trị thế điện cực chuẩn của các cặp oxi hóa – khử như sau:
| Cặp oxi hóa – khử | Al3+/Al | Fe2+/Fe | Cu2+/Cu | Ag+/Ag |
| Thế điện cực chuẩn (V) | -1,676 | -0,440 | +0,340 | +0,799 |
Dựa vào bảng thế điện cực chuẩn ở trên, kim loại có tính khử mạnh nhất là
Fe.
Al.
Cu.
Ag.
Chất béo là nguồn cung cấp năng lượng đáng kể cho cơ thể. Trung bình 1 gam chất béo cung cấp 37,7 kJ. Mỗi ngày, một học sinh trung học phổ thông cần cung cấp 10000 kJ (trong đó năng lượng từ chất béo đóng góp 20%) thì học sinh đó phải ăn bao nhiêu gam chất béo cho phù hợp? (Kết quả làm tròn đến hàng đơn vị)
Một mẫu nước thải của nhà máy sản xuất có pH = 3. Để thải ra ngoài môi trường thì cần phải tăng pH lên từ 5,8 đến 8,6 (theo đúng qui định), nhà máy phải dùng vôi sống thả vào nước thải. Để nâng pH của 4 m³ nước thải từ 3 lên 7 cần dùng m gam vôi sống. Tính giá trị m. (Bỏ qua sự thủy phân của các muối, kết quả làm tròn đến hàng đơn vị).
Trong phân tử peptide cho dưới đây có bao nhiêu liên kết peptide?
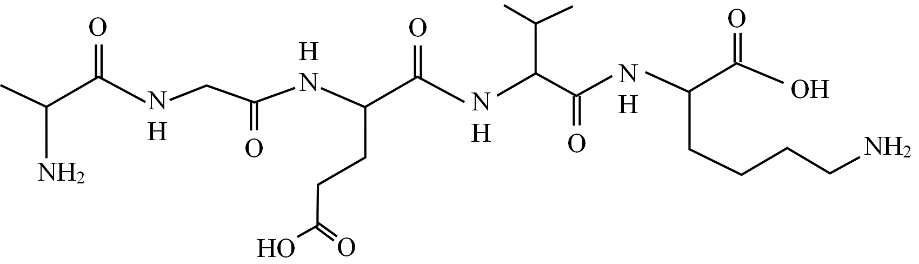
Ở 20oC, độ tan của NaCl trong nước là 35,9 g trong 100 g nước. Ở nhiệt độ này, dung dịch NaCl bão hòa có nồng độ a%. Giá trị của a là bao nhiêu? (Làm tròn kết quả đến hàng phần mười).
Chất nào sau đây được dùng làm chất giặt rửa tổng hợp?
C17H35COOK.
CH3[CH2]11C6H4SO3K.
CH3C6H4ONa.
C15H31COONa.
Quặng sắt là khoáng vật chứa các hợp chất của sắt chủ yếu ở dạng các oxide. Hematite là một loại quặng chứa hàm lượng sắt cao và được dùng để sản xuất gang bằng cách nạp trực tiếp vào lò cao. Từ 100 tấn quặng hematite có thể sản xuất được bao nhiêu tấn gang chứa 96% Fe về khối lượng? Giả thiết quặng hematite chứa 69,9% Fe về khối lượng và có 90% lượng Fe trong quặng chuyển vào gang. (Kết quả làm tròn đến hàng phần mười)
Phản ứng chứng tỏ glucose có dạng mạch vòng là phản ứng của glucose với
Cu(OH)2.
thuốc thử Tollens.
nước bromine.
CH3OH (xúc tác HCl).
Cho các phản ứng sau :
(1) Mg2+(aq) + Pb(s) → Pb2+(aq) + Mg(s)
(2) 2H+(aq) + Zn(s) → Zn2+(aq) + H2(g)
(3) Ni(s) + Pb2+(aq) → Ni2+(aq) + Pb(s)
(4) Fe(s) + Mn2+(aq) → Fe2+(aq) + Mn(s)
Biết: E°Mg2+/Mg=−2,356V; E°Mn2+/Mn=−1,180V; E°Zn2+/Zn=−0,763V; E ° N i 2 + / N i = − 0 , 2 5 7 V ; E ° F e 2 + / F e = − 0 , 4 4 0 V ; E°Pb2+/Pb=−0,126V; E°2H+/H2=0,000V.
Liệt kê các phản ứng xảy ra ở điều kiện chuẩn theo thứ tự tăng dần (Ví dụ: 123, 234,…).
Một học sinh tiến hành điều chế xà phòng từ dầu dừa như sau :
• Bước 1: Cân m gam NaOH cho vào cốc đã chứa sẵn khoảng 100 mL nước và khuấy đều. Để nguội đến khoảng 38°C.
• Bước 2: Cho 300 gam dầu dừa vào cốc thuỷ tinh chịu nhiệt, đun nhẹ và khuấy đều để đưa nhiệt độ của dầu dừa lên khoảng 48°C.
• Bước 3: Rót dung dịch NaOH đã chuẩn bị (phía trên) vào cốc chứa dầu dừa và khuấy nhanh, liên tục trong 30 phút. Khi hỗn hợp chuyển màu sáng kem, sệt, mịn thì ngừng. Thêm ít tinh dầu chanh và khuấy đều.
• Bước 4: Đổ hỗn hợp thu được ở bước 3 vào khuôn, vỗ nhẹ thành khuôn để đuổi không khí ra ngoài. Để khuôn nơi khô ráo. Sau khoảng 24 giờ, lấy xà phòng đã đóng rắn ra khỏi khuôn. Sau 4 – 5 ngày, xà phòng có thể sử dụng được.
. Biết chỉ số xà phòng hóa là số miligam KOH cần để xà phòng hóa triglyceride và trung hòa acid béo tự do trong 1g chất béo; chỉ số xà phòng hóa của dầu dừa là 257. Học sinh trên đã lấy m gam NaOH ứng với lượng KOH cần dùng. Giá trị của m là 55 (làm tròn đến hàng đơn vị).
. Trong xà phòng thu được có chứa glycerol.
. Bước 3 xảy ra phản ứng xà phòng hóa của dầu dừa.
. Tinh dầu chanh là chất xúc tác cho phản ứng xà phòng hóa.
Ắc quy chì (Lead-acid Battery) là nguồn điện thông dụng, tạo ra dòng điện ổn định và đặc biệt có thể tái sử dụng. Khi ắc quy phóng điện, quá trình xảy ra tại các điện cực như sau:
Anode: Pb + HSO4− → PbSO4 + H+ + 2e
Cathode: PbO2 + HSO4− + 3H+ + 2e → PbSO4 + 2H2O
Khác với pin Galvani, ắc quy có thể tái sử dụng bằng cách áp dòng điện bên ngoài để các phản ứng ở điện cực xảy ra theo chiều ngược khi phóng điện (gọi là quá trình nạp điện hay tích điện).
. Khi ắc quy phóng điện, tại anode xảy ra quá trình oxi hóa chì (lead).
. Khi ắc quy phóng điện, tại cathode xảy ra quá trình khử lead dioxide (PbO2).
. Khi ắc quy phóng điện cũng như nạp điện, nồng độ H2SO4 không đổi.
. Khi nạp điện, ắc quy đóng vai trò như bình điện phân.
Một nhóm học sinh tiến hành thí nghiệm mạ đồng (copper) lên chiếc thìa kim loại. Giả thuyết được nhóm học sinh đưa ra là: “Nồng độ CuSO4 trước và sau quá trình mạ là không đổi”. Để kiểm chứng giả thuyết, nhóm học sinh tiến hành quá trình mạ theo các bước như sau :
• Bước 1: Cân để xác định khối ban đầu của chiếc thìa là 10 gam và của thanh đồng nguyên chất là 15 gam.
• Bước 2: Nối chiếc thìa với 1 điện cực và thanh đồng với điện cực còn lại của nguồn điện một chiều rồi nhúng vào cốc chứa dung dịch CuSO4 để tiến hành mạ với hiệu điện thế thích hợp.
• Bước 3: Sau thời gian 15 phút điện phân, lấy chiếc thìa và thanh đồng ra khỏi cốc, làm khô cẩn thận, đem cân thì thấy khối lượng của chiếc thìa là 10,32 gam, của thanh đồng là 14,68 gam. Biết hiệu suất của quá trình đạt 100%.
. Tại anode xảy ra quá trình khử ion Cu2+, tại cathode xảy ra quá trình oxi hóa Cu.
. Do khối lượng của thanh đồng giảm nên giả thuyết ban đầu của nhóm học sinh là sai.
. Sau khi mạ xong, độ giảm khối lượng của thanh đồng bằng độ tăng khối lượng của chiếc thìa.
. Thanh đồng được nối với cực dương, chiếc thìa được nối với cực âm của nguồn điện.
Quặng vàng (Gold) tồn tại trong tự nhiên thường có hàm lượng vàng thấp. Phương pháp tách vàng phù hợp hiện này là phương pháp Cyanide. Theo phương pháp này, để thu hồi vàng từ quặng, người ta thường nghiền nhỏ quặng rồi hòa tan trong dung dịch KCN (potassium cyanide, rất độc) cùng với dòng không khí liên tục được thổi vào. Khi đó, vàng bị hòa tan tạo thành phức chất (các chất khác trong quặng không phản ứng với KCN):
4Au(s) + 8KCN(aq) + O2(g) + 2H2O(l) → 4K[Au(CN)2](aq) + 4KOH(aq) (1)
Tiếp theo cho bột kẽm đến dư vào dung dịch phức, thu được bột vàng (có lẫn một ít bột kẽm):
Zn(s) + 2K[Au(CN)2](aq) → K2[Zn(CN)4](aq) + 2Au(s) (2)
. Phương pháp tách vàng ở trên là phương pháp thủy luyện.
. Để loại bỏ Zn lẫn trong bột vàng, có thể dùng dung dịch HCl.
. Phương pháp tách vàng ở trên thân thiện với môi trường.
. Để thu được 37,5 gam vàng cần 23,5 gam KCN (hiệu suất cả quá trình tách đạt 100%). Biết nguyên tử khối của C = 12; N = 14; K = 39; Au = 197.








