Đề thi tham khảo ôn thi THPT Hóa học có đáp án - Đề tham khảo số 1
28 câu hỏi
Chất nào sau đây thuộc loại monosaccharide?
Maltose.
Saccharose.
Fructose.
Tinh bột.
Tơ là những vật liệu polymer hình sợi dài và mảnh với độ bền nhất định. Tơ tằm được lấy từ kén của con sâu tằm thuộc loại
tơ hóa học.
tơ tổng hợp.
tơ tự nhiên.
tơ bán tổng hợp.
Chất béo là
triester của acid hữu cơ và glycerol.
triester của glycerol với acid béo.
ester của acid béo và alcohol đa chức.
hợp chất hữu cơ chứa C, H, N, O.
Cho các phát biểu sau về peptide T có công thức cấu tạo dưới đây:
H 2 N − C H ( C H 3 ) − C O − N H − C H 2 − C O − N H − C H ( C H 3 ) − C O O H
(a) Peptide T là dipeptide vì có chứa 2 liên kết peptide.
(b) Peptide T có phản ứng màu biuret.
(c) Peptide T tác dụng đủ với dung dịch NaOH theo tỉ lệ mol 1:3.
(d) Khi đun nóng peptide T với dung dịch acid hoặc kiềm dư sẽ xảy ra phản ứng thủy phân thu được 3 muối khác nhau.
(e) T có thể được biểu diễn là Gly-Ala-Ala.
Số phát biểu không đúng về peptide T là
3.
4.
2.
1.
Nhỏ nước bromine vào ống nghiệm đựng dung dịch aniline. Hiện tượng quan sát được là
xuất hiện kết tủa màu tím.
xuất hiện khí không màu.
xuất hiện kết tủa màu xanh.
xuất hiện kết tủa màu trắng.
PE là loại nhựa phổ biến, được ứng dụng để sản xuất túi nylon, bao gói, màng bọc thực phẩm, chai lọ, đồ chơi trẻ em, ... PE được cấu tạo từ các đơn vị mắt xích là
− C H 2 − C H ( C H 3 ) − .
− C H 2 − C H C l − .
− C H 2 − C H 2 − .
− C 6 H 1 0 O 5 − .
Chất giặt rửa tổng hợp thường có thành phần chính là
glycerol và ethanol.
saponin trong bồ hòn và bồ kết.
muối sodium hoặc potassium của acid béo (thường là các gốc acid béo no).
muối sodium alkylsulfate ( R – O S O 3 N a ) , sodium alkylbenzene sulfonate (R-C6H4-SO3Na).
Thực hiện thí nghiệm theo 2 bước sau:
Bước 1: Cho vào ống nghiệm khoảng 1 mL dung dịch NaOH 30%. Thêm tiếp vài giọt dung dịch C u S O 4 2 % , lắc đều (có thể khuấy bằng đũa thuỷ tinh).
Bước 2: Thêm vào ống nghiệm khoảng 3 mL dung dịch lòng trắng trứng, lắc hoặc khuấy đều hỗn hợp.
Phát biểu nào sau đây đúng?
Sau bước 1 xuất hiện kết tủa màu trắng.
Sau bước 2 kết tủa tan tạo dung dịch màu xanh.
Thí nghiệm trên dùng để phân biệt dipeptide với các peptide còn lại.
Thay lòng trắng trứng bằng dầu thực vật, hiện tượng xảy ra tương tự.
Cho pin điện F e − C u được tạo thành từ hai điện cực C u 2 + / C u và F e 2 + / F e với thế điện cực tương ứng E F e 2 + / F e o = − 0 , 4 4 V ; E C u 2 + / C u o = + 0 , 3 4 V . Cathode của pin là điện cực của cặp oxi hóa - khử nào?
C u 2 + / C u .
F e 2 + / F e .
C u 2 + / F e .
F e 2 + / C u .
Điện phân dung dịch chất T (với điện cực trơ, màng ngăn xốp), thu được dung dịch có chứa chất tan là base. Chất nào sau đây thỏa mãn tính chất của T?
C u S O 4 .
A g N O 3 .
F e C l 3 .
NaCl.
Cặp chất không xảy ra phản ứng hóa học là
Fe và dung dịch F e C l 3 .
Fe và dung dịch HCl.
Cu và dung dịch F e C l 3 .
Ag và dung dịch F e C l 2 .
Trong các kim loại sau, kim loại nào thường được dùng làm tế bào quang điện?
Cs.
Mg.
K.
Fe.
Magnesium là kim loại cơ bản trong hợp kim dùng để chế tạo khung và cánh của các thiết bị bay.

Ứng dụng trên không dựa vào tính chất vật lí nào của hợp kim magnesium?
Tính cứng.
Tính bền.
Tính nhẹ.
Tính ánh kim.
Dung dịch có chứa ion F e 3 + có màu
đỏ.
tím.
vàng nâu.
xanh lam.
Phức chất nào sau đây có dạng hình học tứ diện?
[ N i ( C O ) 4 ] .
[ C u ( N H 3 ) 4 ( O H 2 ) 2 ] 2 + .
[ C o ( N H 3 ) 6 ] 3 + .
[ C o C l 2 ( O H 2 ) 4 ] .
Muối Epsom có thành phần là M g S O 4 ⋅ 7 H 2 O . Khi đun nóng đến 70 - 8 0 ° C , nó mất đi một phần khối lượng, do một số phân tử nước trong muối ban đầu bị bay hơi đi mất. Giả sử đun nóng 2 , 4 6 5 g muối Epsom đến 7 5 ° C thấy khối lượng lúc này chỉ còn 1 , 7 4 4 g . Công thức của muối sau khi bị mất một vài phân tử nước là
M g S O 4 . 6 H 2 O .
M g S O 4 . 4 H 2 O .
M g S O 4 . 5 H 2 O .
M g S O 4 ⋅ 3 H 2 O .
Chỉ số xà phòng hóa là số miligan KOH dùng để trung hòa hết triglycerid và trung hòa hết lượng acid tự do trong 1 gam chất béo. Một chất béo chứa 3,55% stearic acid và 89% tristearin về khối lượng, còn lại là các chất khác không tham gia phản ứng với KOH. Tính chỉ số xà phòng hóa của chất béo trên.
Kim loại calcium (Ca) được điều chế bằng cách điện phân nóng chảy C a C l 2 với dòng điện có cường độ 3000 A và điện áp U = 2 5 V . Hiệu suất điện phân là 80%. Tính điện năng (theo kWh) đã sử dụng điều chế 1 kg Ca. (Làm tròn kết quả đến hàng phần mười)
Cho biết:
Điện năng A được xác định bởi công thức: A = U . n e . F (với n e là số mol electron trao đổi giữa điện cực với các chất điện phân; F = 9 6 4 8 5 C / m o l ).
Trong công nghiệp, dolomite là nguyên liệu sản xuất magnesium oxide (MgO, thành phần chính của gạch chịu lửa) theo phản ứng:
CaCO3.MgCO3(s) → CaO(s) + MgO(s) + 2CO2(g)
Cho enthalpy tạo thành chuẩn (kJ/mol) của các chất theo bảng sau:
| Chất | CaCO3.MgCO3(s) | CaO(s) | MgO(s) | CO2(g) |
| Δ f H 2 9 8 0 (kJ/mol) | -2326,3 | -634,9 | -601,6 | -393,5 |
Quá trình phân hủy hoàn toàn 2500 gam dolomite theo phản ứng trên đã hấp thụ a kJ nhiệt. Giá trị của a là bao nhiêu? (Kết quả làm tròn đến hàng đơn vị)
Dung dịch iron(II) sulfate để lâu ngày bị oxi hóa một phần bởi oxygen của không khí tạo thành iron(III) sulfate (hỗn hợp X). Cho 30 mL dung dịch H2SO4 0,5M vào 10 mL hỗn hợp X thu được dung dịch Y.
• Thí nghiệm 1: Chuẩn độ 10,0 mL dung dịch Y bằng dung dịch KMnO4 0,05M cho đến khi xuất hiện màu hồng nhạt bền (phản ứng coi như vừa đủ) thì thấy hết 9,0 mL dung dịch KMnO4.
• Thí nghiệm 2: Ngâm một lá sắt dư vào 10,0 mL dung dịch Y, khuấy đều đến khi khử hoàn toàn sắt(III) thành Fe(II). Lấy lá sắt ra, rồi chuẩn độ bằng dung dịch KMnO4 0,05M. Khi màu hồng nhạt bền xuất hiện thì thấy hết 10,5 mL dung dịch KMnO4. Tỉ lệ iron (II) sulfate đã bị oxi hóa trong không khí là a%. Giá trị của a bằng bao nhiêu? (kết quả làm tròn đến hàng đơn vị).
Tên gọi của ester HCOOCH3 là
methyl acetate.
ethyl formate.
methyl formate.
ethyl acetate.
Phần trăm khối lượng của nguyên tố nitrogen trong alanine là a%. Giá trị của a là bao nhiêu? (Làm tròn kết quả đến hàng phần mười).
Đồng là một kim loại dẫn điện tốt (chỉ xếp sau bạc), tuy nhiên các dây điện cao thế không được làm bằng đồng mà thường được làm bằng kim loại nào sau đây?
Fe.
Na.
Al.
Au.
Gang là hợp kim của sắt (iron) với carbon và một số nguyên tố khác. Gang được sản xuất từ nguyên liệu là quặng hematite (thành phần chính là Fe2O3) và carbon, với hiệu suất chuyển hóa từ Fe2O3 thành Fe đạt 80%. Để sản xuất được 5,9 tấn gang (chứa 95% Fe về khối lượng) cần dùng m tấn quặng hematite (chứa 60% Fe2O3 về khối lượng, các tạp chất khác không chứa Fe). Giá trị của m bằng bao nhiêu (làm tròn kết quả đến hàng phần mười)?
Aspirin là một hợp chất được sử dụng làm giảm đau, hạ sốt. Sau khi uống, aspirin bị thủy phân trong cơ thể sẽ tạo thành acid salicylic. Salicylic acid ức chế quá trình sinh tổng hợp prostaglandin (chất gây đau, sốt và viêm khi nồng độ trong máu cao hơn mức bình thường).
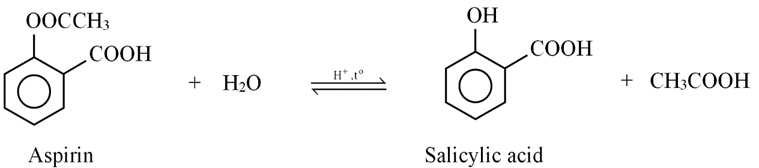
Công thức phân tử của aspirin là C9H10O4.
Trong một phân tử aspirin có chứa 5 liên kết \(\pi .\)
1 mol salicylic acid tác dụng tối đa với 2 mol NaOH trong dung dịch.
Thủy phân aspirin trong môi trường base thu được muối carboxylate và alcohol.
Polymer X có tính dai, bền, mềm mại, óng mượt, ít thấm nước, giặt mau khô. Polymer X dùng để dệt vải may mặc, vải lót săm lốp xe, dệt bít tất, bện làm dây cáp, dây dù, đan lưới, … Cấu tạo một đoạn mạch polymer X như sau:
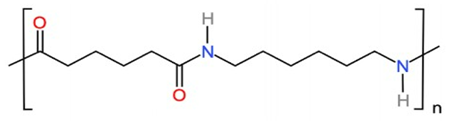
X có tên là tơ nylon-6.
Các loại vải làm từ polymer X có thể giặt trong nước có độ kiềm cao.
X được điều chế từ hexamethylenediamine và adipic acid bằng phản ứng trùng ngưng.
Các nhóm amide trong X có khả năng tạo liên kết hydrogen giữa các chuỗi polymer, giúp tăng cường các tính chất cơ học cho X.
Xét các phản ứng phân huỷ sau:
CaCO3( s)⇌CaO(s)+CO2( g) ΔrH298°=179,2 kJ
BaCO3( s)⇌BaO(s)+CO2( g) ΔrH298°=271,5 kJ
Nhiệt lượng toả ra khi phân huỷ 1 mol \({\rm{BaC}}{{\rm{O}}_3}\) lớn hơn nhiệt lượng toả ra khi phân huỷ 1 mol \({\rm{CaC}}{{\rm{O}}_3}.\)
\({\rm{BaC}}{{\rm{O}}_3}\) bị phân huỷ ở nhiệt độ thấp hơn \({\rm{CaC}}{{\rm{O}}_3}.\)
Khi tăng nhiệt độ, cả hai phản ứng đều dịch chuyển theo chiều thuận.
\({\rm{C}}{{\rm{O}}_2}\) cần được lấy ra khỏi lò nung để tăng hiệu suất của phản ứng.
Hemoglobin đóng vai trò quan trọng trong quá trình vận chuyển oxygen từ phổi đến tế bào và mô. Hemoglobin có chứa phức có công thức cấu tạo như sau:
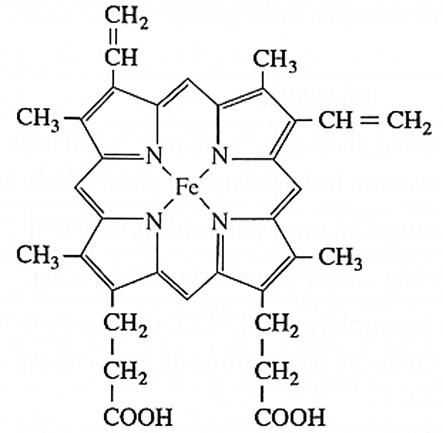
Phức chất trên có điện tích bằng 0.
Nguyên tử trung tâm trong hemoglobin là kim loại chuyển tiếp.
Trong phân tử hemoglobin có 4 phối tử.
Mỗi nguyên tử Fe đã nhận 4 electron chưa tham gia liên kết từ các phối tử.








