Bộ 3 đề thi giữa kì 2 Hóa 10 Cánh diều có đáp án - Đề 2
32 câu hỏi
Số oxi hoá của nguyên tử kim loại kiềm thổ (nhóm IIA) trong hợp chất là
-1.
0.
-2.
+2.
Số oxi hoá của nguyên tử phosphorus (P) trong đơn chất là
+3.
0.
-3.
+5.
Phát biểu nào sau đây là đúng?
Trong các hợp chất số oxi hoá của hydrogen luôn là +1.
Trong các hợp chất số oxi hoá của oxygen luôn là -2.
Số oxi hoá của nhôm trong hợp chất là +3.
Trong một ion đa nguyên tử, tổng số số oxi hoá của nguyên tử bằng 0.
Chất khử là
chất nhường electron, chứa nguyên tố có số oxi hóa tăng sau phản ứng.
chất nhường electron, chứa nguyên tố có số oxi hóa giảm sau phản ứng.
chất nhận electron, chứa nguyên tố có số oxi hóa tăng sau phản ứng.
chất nhận electron, chứa nguyên tố có số oxi hóa giảm sau phản ứng.
Dấu hiệu để nhận biết một phản ứng oxi hóa – khử là dựa trên sự thay đổi đại lượng nào sau đây của nguyên tử?
Số hiệu nguyên tử.
Số mol.
Số khối.
Số oxi hóa.
Trường hợp nào sau đây không xảy ra phản ứng oxi hoá – khử?
Đốt cháy than, củi để sưởi ấm.
Phản ứng quang hợp của cây xanh.
Nhỏ từ từ HCl vào dung dịch chứa NaOH.
Phản ứng tích trữ năng lượng của pin lithium – ion.
Dẫn khí CO đi qua ống sứ đựng bột CuO nung nóng để thực hiện phản ứng hóa học sau: CuO + CO → t o Cu + CO2. Trong phản ứng trên, chất đóng vai trò chất khử là
CuO.
CO.
Cu.
CO2.
Cho các phản ứng hóa học sau:
(a) C a C O 3 → t 0 C a O + C O 2 .
(b) C H 4 + 2 O 2 → t o C O 2 + 2 H 2 O .
(c) 2 A l ( O H ) 3 → t 0 A l 2 O 3 + 3 H 2 O .
(d) 2 N a H C O 3 → t 0 N a 2 C O 3 + C O 2 + H 2 O .
Số phản ứng oxi hóa – khử là
4.
2.
3.
1.
Phản ứng thu nhiệt là
phản ứng giải phóng năng lượng dưới dạng nhiệt.
phản ứng hấp thụ năng lượng dưới dạng nhiệt.
phản ứng giải phóng ion dưới dạng nhiệt.
phản ứng hấp thụ ion dưới dạng nhiệt.
Phản ứng nào sau đây là phản ứng tỏa nhiệt?
Phản ứng nung vôi.
Phản ứng phân huỷ thuốc tím.
Phản ứng đốt cháy cồn (ethanol).
Phản ứng nung NH4Cl(s) tạo ra NH3(g) và HCl(g).
Biến thiên enthalpy chuẩn của phản ứng hoá học là
nhiệt lượng toả ra của phản ứng ở điều kiện áp suất không đổi.
nhiệt lượng thu vào của phản ứng ở điều kiện áp suất không đổi.
nhiệt lượng toả ra hoặc thu vào của phản ứng ở điều kiện áp suất không đổi.
nhiệt lượng toả ra hoặc thu vào của phản ứng ở điều kiện chuẩn.
Nhiệt độ ở điều kiện chuẩn thường chọn là
25 oC.
289 oC.
289 K.
298 oC.
Cho phản ứng hoá học sau: 2Na(s) + Cl2(g) → 2NaCl(s). Biến thiên enthalpy chuẩn của phản ứng này được tính theo công thức là
Δ r H 2 9 8 0 = Δ f H 2 9 8 0 ( N a ( s ) ) + Δ f H 2 9 8 0 ( C l 2 ( g ) ) − Δ f H 2 9 8 0 ( N a C l ( s ) ) .
Δ r H 2 9 8 0 = Δ f H 2 9 8 0 ( N a C l ( s ) ) − Δ f H 2 9 8 0 ( N a ( s ) ) − Δ f H 2 9 8 0 ( C l 2 ( g ) ) .
Δ r H 2 9 8 0 = 2 × Δ f H 2 9 8 0 ( N a ( s ) ) + Δ f H 2 9 8 0 ( C l 2 ( g ) ) − 2 × Δ f H 2 9 8 0 ( N a C l ( s ) ) .
Δ r H 2 9 8 0 = 2 × Δ f H 2 9 8 0 ( N a C l ( s ) ) − 2 × Δ f H 2 9 8 0 ( N a ( s ) ) − Δ f H 2 9 8 0 ( C l 2 ( g ) ) .
Cho phản ứng sau:
H2(g) + Cl2(g) 2HCl (g) ΔrH298o=−184,6 kJ
Phản ứng này là
phản ứng thu nhiệt.
phản ứng tỏa nhiệt.
phản ứng thế.
phản ứng phân hủy.
Ở nhiệt độ 25oC và áp suất 1 bar, trong số các đơn chất halogen sau, đơn chất có enthalpy tạo thành chuẩn khác 0 là
F2(g).
I2(g).
Br2(l).
Cl2(g).
Ở điều kiện chuẩn, phản ứng có biến thiên enthalpy của phản ứng bằng enthalpy tạo thành của chất sản phẩm là
HCl(aq) + NaOH(aq) → NaCl(aq) + H2O.
N2(l) + 3F2(g) → 2NF3(g).
H2(g) + O2(g) → H2O2(g).
H2O(l) +12O2(g)→H2O2(l).
Số oxi hóa của lưu huỳnh (sulfur) trong SO42-là
+6.
+4.
-6.
-2.
Cho các hợp chất sau: NH3, NH4Cl, HNO3, NO2. Số hợp chất chứa nguyên tử nitrogen có số oxi hoá -3 là
1.
3.
2.
4.
Sục khí SO2 vào dung dịch KMnO4 (thuốc tím), màu tím nhạt dần rồi mất màu (biết sản phẩm tạo thành là MnSO4, H2SO4 và H2O). Nguyên nhân là do
SO2 đã oxi hóa KMnO4 thành MnO2.
SO2 đã khử KMnO4 thành Mn2+.
KMnO4 đã khử SO2 thành S + 6 .
H2O đã oxi hóa KMnO4 thành Mn2+.
Trong giai đoạn đầu sản xuất nitric acid từ ammonia. Ammonia bị oxi hóa bởi oxygen ở nhiệt độ cao khi có chất xúc tác.
NH3+ O2→pxt,t0NO + H2O
Tổng hệ số cân bằng (là các số nguyên, tối giản) của phản ứng là
18.
19.
20.
21.
Cho phản ứng: Mg + H2SO4 → MgSO4 + H2S + H2O. Khi hệ số cân bằng phản ứng là nguyên và tối giản thì số phân tử H2O tạo thành là:
3.
10.
5.
4.
Trong phản ứng: 3Cu + 8HNO3 → 3Cu(NO3)2 + 2NO + 4H2O
Số phân tử nitric acid (HNO3) đóng vai trò chất oxi hóa là
8.
6.
4.
2.
Khi nung vôi, người ta sử dụng phản ứng đốt than để cung cấp nhiệt cho phản ứng phân hủy đá vôi. Phát biểu nào sau đây là đúng?
Phản ứng đốt than là phản ứng thu nhiệt, phản ứng phân hủy đá vôi là phản ứng tỏa nhiệt.
Phản ứng đốt than là phản ứng tỏa nhiệt, phản ứng phân hủy đá vôi là phản ứng thu nhiệt.
Phản ứng đốt than và phản ứng phân hủy đá vôi là phản ứng tỏa nhiệt.
Phản ứng đốt than và phản ứng phân hủy đá vôi là phản ứng thu nhiệt.
Cho giản đồ năng lượng của các phản ứng 1 – 5 như sau:
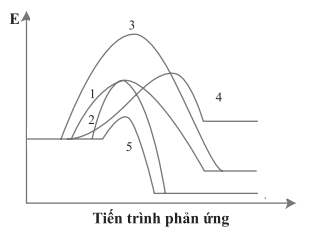
Số phản ứng toả nhiệt là
1.
2.
3.
4.
Cho phản ứng sau:
2NaCl(s) → 2Na(s) + Cl2(g)
Biết ∆fH298o (kJ mol-1) của NaCl là –411,2. Trong quá trình nấu ăn, dù bị đun nóng nhưng muối ăn không bị phân hủy thành khí Cl2 độc, vì
∆rH298o rất dương, phản ứng không thuận lợi xảy ra.
∆rH298o rất âm, phản ứng không thuận lợi xảy ra.
phản ứng trên là phản ứng tỏa nhiệt.
phản ứng trên là phản ứng thu nhiệt.
Cho các phát biểu sau:
(1). Tất cả các phản ứng cháy đều thu nhiệt.
(2). Phản ứng toả nhiệt là phản ứng giải phóng năng lượng dưới dạng nhiệt.
(3). Tất cả các phản ứng mà chất tham gia có chứa nguyên tố oxygen đều toả nhiệt.
(4). Phản ứng thu nhiệt là phản ứng hấp thụ năng lượng dưới dạng nhiệt.
Số phát biểu sai là
1.
2.
3.
4.
Cho các phương trình nhiệt hóa học sau:
(1) C S 2 ( l ) + 3 O 2 ( g ) → t ° C O 2 ( g ) + 2 S O 2 ( g ) Δ r H 2 9 8 o = − 1 1 1 0 , 2 1 k J
(2) C O 2 ( g ) → C O ( g ) + 1 2 O 2 ( g ) Δ r H 2 9 8 o = + 2 8 0 , 0 0 k J
(3) 2 N a ( s ) + 2 H 2 O ( l ) → 2 N a O H ( a q ) + H 2 ( g ) Δ r H 2 9 8 o = − 3 6 7 , 5 0 k J
(4) Z n S O 4 ( s ) → Z n O ( s ) + S O 3 ( g ) Δ r H 2 9 8 o = + 2 3 5 , 2 1 k J
Số phản ứng tỏa nhiệt là
1.
2.
3.
4.
Cho phản ứng: N2(g) + O2(g) → 2NO(g). Biết năng lượng liên kết trong các phân tử O2, N2 và NO lần lượt là 494 kJ/mol, 945 kJ/mol và 607 kJ/mol. Phát biểu đúng là
Phản ứng toả nhiệt.
Nhiệt lượng thu vào của phản ứng là 25 kJ.
Phản ứng xảy ra ở ngay điều kiện thường.
Phản ứng xảy ra ở nhiệt độ cao hoặc khi có tia lửa điện.
(1 điểm): Lập phương trình hoá học của các phản ứng sau bằng phương pháp thăng bằng electron, nêu rõ chất oxi hóa, chất khử.
(a) HI + H2SO4 → SO2 + I2 + H2O.
(b) Al + HNO3 → Al(NO3)3 + NH4NO3 + H2O.
(1 điểm): Quá trình đốt cháy ethanol diễn ra theo phản ứng:
C2H5OH(l) + 3O2 (g) → 2CO2 (g) + 3H2O(l)
Tính ∆rH298ocủa phản ứng trên từ các giá trị năng lượng liên kết sau:
EC–C = 347 kJ mol-1; EO=O = 496 kJ mol-1; EC–O = 336 kJ mol-1; EC–H = 410 kJ mol-1; EC=O = 805 kJ mol-1; EO–H = 465 kJ mol-1.
(0,5 điểm): Cho 2,34 gam kim loại M (có hóa trị không đổi là n) tác dụng với dung dịch H2SO4 (đặc nóng, dư) thu được 3,2227 L SO2 (điều kiện chuẩn). Xác định kim loại M.
(0,5 điểm): Tính lượng nhiệt tỏa ra ở điều kiện chuẩn khi đốt cháy 2 gam butane (C4H10) chứa trong một chiếc bật lửa gas. Biết sản phẩm của sự đốt cháy là khí carbon dioxide và hơi nước.
Cho ∆fH298ocủa C4H10 (g), CO2 (g) và H2O (l) lần lượt là –126,15 kJ mol-1, –393,51 kJ mol-1 và –285,83 kJ mol-1.








