Bộ 3 đề thi cuối kì 2 Hóa 10 Cánh diều cấu trúc mới có đáp án - Đề 3
28 câu hỏi
PHẦN I. Câu trắc nghiệm nhiều phương án lựa chọn. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
Cho các phản ứng sau:
(1) Phản ứng than cháy trong không khí.
(2) Phản ứng tạo gỉ sắt.
(3) Phản ứng nổ của khí bình gas.
(4) Phản ứng lên men rượu.
Phản ứng xảy ra với tốc độ nhanh nhất là
(1).
(2).
(3).
(4).
Chất xúc tác là chất
không làm thay đổi tốc độ phản ứng và không bị thay đổi cả chất và lượng sau phản ứng.
làm tăng tốc độ phản ứng nhưng không bị thay đổi cả chất và lượng sau phản ứng.
làm tăng tốc độ phản ứng và có khối lượng giảm sau khi phản ứng kết thúc.
làm tăng tốc độ phản ứng và có khối lượng tăng sau khi phản ứng kết thúc.
Với phản ứng đơn giản: aA + bB ⟶ sản phẩm, tốc độ phản ứng được tính theo công thức
\(v\) = \(kC_A^aC_B^b\).
\(v\) = \(kC_A^{}C_B^{}\).
\(v\) = \(C_A^aC_B^b\).
\(v\) = \(abC_A^{}C_B^{}\).
Hệ số nhiệt độ Van’t Hoff được kí hiệu là
∝.
γ.
φ.
θ.
Cho phản ứng: Br2(l) + HCOOH(aq)® 2HBr(aq) + CO2(s).
Nồng độ ban đầu của Br2 là aM, sau 50 giây nồng độ Br2 còn lại là 0,02M. Tốc độ trung bình của phản ứng trên là 4.10-5M/s. Giá trị của a là
0,02 M.
0,07 M.
0,02 M.
0,022 M.
Cho một mẩu đá vôi nguyên khối nặng 1 gam vào dung dịch HCl 2M ở nhiệt độ 25 oC. Sự thay đổi nào sau đây không làm bọt khí thoát ra mạnh hơn?
Tăng thể tích dung dịch HCl lên gấp đôi.
Thay mẩu đá vôi trên bằng 1 gam đá vôi bột.
Thay dung dịch HCl 2M bằng dung dịch HCl 4M.
Tăng nhiệt độ lên 50 oC.
Cho phản ứng đơn giản xảy ra trong bình kín: H2(g) + Cl2(g) ⟶ 2HCl(g).
Tốc độ phản ứng thay đổi như thế nào nếu nồng độ H2 giảm 4 lần và nồng độ Cl2 tăng 2 lần.
tăng 4 lần.
giảm 4 lần.
giảm 2 lần.
tăng 8 lần.
Phản ứng giữa đơn chất halogen nào sau đây với hydrogen diễn ra mãnh liệt, nổ ngay cả trong bóng tối hoặc ở nhiệt độ thấp?
I2.
Br2.
Cl2.
F2.
Cấu hình electron lớp ngoài cùng của nguyên tử các nguyên tố halogen là
ns2np3.
ns2np4.
ns2np5.
ns2np6.
Ở điều kiện thường, đơn chất chlorine có màu
lục nhạt.
vàng lục.
nâu đỏ.
tím đen.
Dung dịch chất nào sau đây được dùng để trung hòa môi trường base, hoặc thủy phân các chất trong quá trình sản xuất, tẩy rửa gỉ sắt (thành phần chính là các iron oxide) bám trên bề mặt của các loại thép?
H2SO4.
HCl.
NaOH.
NaCl.
Để phân biệt các dung dịch: KF, KCl, NaBr, NaI, ta dùng
dung dịch HCl.
quỳ tím.
dung dịch BaCl2.
dung dịch AgNO3.
Hydrohalic acid có tính acid mạnh nhất là
Hydrochloric acid.
Hydrofluoric acid.
Hydrobromic acid.
Hydroiodic acid.
Dẫn khí chlorine vào dung dịch KBr xảy ra phản ứng hoá học:
Cl2 + 2KBr → 2KCl + Br2
Trong phản ứng hoá học trên, xảy ra quá trình oxi hoá chất nào?
KCl.
Br2.
Cl2.
KBr.
Cho các phát biểu sau:
(a) Dẫn khí chlorine vào nước, thu được dung dịch nước chlorine màu vàng nhạt.
(b) Cho giấy quỳ tím ẩm vào bình đựng khí hydrogen chloride, giấy quỳ chuyển sang màu xanh.
(c) Nhỏ vài giọt dung dịch silver nitrate vào dung dịch muối ăn thấy xuất hiện kết tủa trắng.
(d) Cho mẩu giấy màu vào nước Javel, mẩu giấy bị mất màu.
Số phát biểu đúng là
1.
2.
3.
4.
Trong phòng thí nghiệm, có thể điều chế halogen (X2) theo sơ đồ phản ứng sau:
NaX(s) + MnO2(s) + H2SO4(đậm đặc) X2(g)
Phương pháp trên không được dùng để điều chế X2 nào sau đây?
I2.
F2.
Cl2.
Br2.
Phản ứng giữa chất nào sau đây với dung dịch H2SO4 đặc, nóng không phải là phản ứng oxi hóa – khử?
KBr(s).
KI(s).
NaCl(s).
NaBr(s).
Phản ứng hóa học nào sau đây là sai?
2HCl + Fe → FeCl2 + H2.
SiO2 + 4HF → SiF4 + 2H2O.
Cl2 + 2NaBr → 2NaCl + Br2.
AgNO3 + HF → HNO3 + AgF.
PHẦN II. Câu trắc nghiệm đúng sai. Thí sinh trả lời từ câu 1 đến câu 4. Trong mỗi ý a), b), c), d) ở mỗi câu, thí sinh chọn đúng hoặc sai. (Đ – S)
Cảnh sát giao thông sử dụng các dụng cụ phân tích ethanol có chứa CrO3. Khi tài xế hà hơi thở vào dụng cụ phân tích trên, nếu trong hơi thở có chứa hơi rượu thì hơi rượu sẽ tác dụng với CrO3 có màu da cam và biến thành Cr2O3 có màu xanh đen theo phản ứng hóa học sau:
CrO3 + C2H5OH → CO2↑ + Cr2O3 + H2O
Tỉ lệ chất khử : chất oxi hóa ở phương trình hóa học trên là 1: 4.
Trong phản ứng trên thì CrO3 đóng vai trò là chất khử.
Tỉ lệ hệ số cân bằng của các chất trong phản ứng trên là 4 : 1 : 2 : 2 : 3.
Số oxi hóa của carbon trước và sau phản ứng lần lượt là +2 và +4.
Ở áp suất 1 bar và nhiệt độ 25oC, phản ứng giữa 1 mol sulfur với oxygen xảy ra theo phương trình “S(s) + O2(g) → SO2(g)” và tỏa ra một lượng nhiệt là 296,9 kJ.
Biến thiên enthalpy chuẩn của phản ứng là 296,9 kJ.
Enthalpy tạo thành chuẩn của sulfur dioxide bằng -296,9 kJ mol-1.
Sulfur dioxide vừa có thể là chất khử vừa có thể là chất oxi hóa, tùy thuộc vào phản ứng mà nó tham gia.
0,5 mol sulfur tác dụng hết với oxygen giải phóng 148,45 kJ năng lượng dưới dạng nhiệt.
Thực hiện phản ứng: 2ICl + H2I2 + 2HCl. Nồng độ đầu của ICl và H2 được lấy đúng theo tỉ lệ phản ứng. Nghiên cứu sự thay đổi nồng độ các chất tham gia và chất tạo thành trong phản ứng theo thời gian, thu được đồ thị sau:
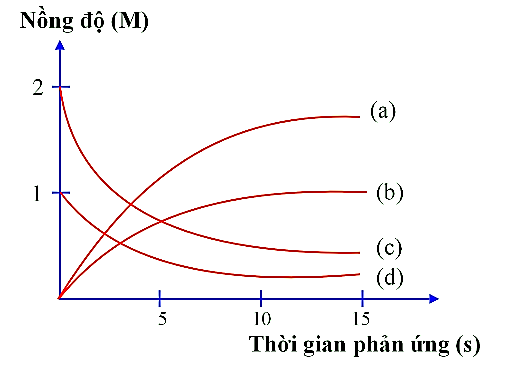
Đường (a) nồng độ HCl tăng dần theo thời gian, lượng tăng gấp đôi I2.
Trong quá trình phản ứng nồng độ ICl và H2 tăng dần còn nồng độ I2 và HCl giảm dần.
Đường (b) nồng độ I2 tăng dần theo thời gian.
Đường (c) nồng độ ICl giảm dần theo thời gian.
Nhóm VIIA trong bảng tuần hoàn các nguyên tố hóa học còn gọi là nhóm halogen, gồm 6 nguyên tố: fluorine (F); chlorine (Cl); bromine (Br); iodine (I); astatine (At) và tennessine (Ts). Bốn nguyên tố F, Cl, Br, I tồn tại trong tự nhiên; còn At và Ts là các nguyên tố phóng xạ.
Số oxi hóa của các halogen trong hợp chất là -1.
Nhiệt độ nóng chảy, nhiệt độ sôi giảm từ F2 đến I2
Liên kết trong phân tử hydrogen halide (HX) là liên kết cộng hóa trị.
Có thể phân biệt các ion F−; Cl−; Br−; I− trong dung bằng dung dịch silver nitrate.
Phần III. Câu hỏi trắc nghiệm yêu cầu trả lời ngắn. Thí sinh trả lời từ câu 1 đến câu 6.
Viết phương trình hoá học của phản ứng minh hoạ hiện tượng: vỏ trứng gà sủi bọt khí khi ngâm trong dung dịch hydrochloric acid.
Vì sao trong thí nghiệm điều chế chlorine, cần nút bông tẩm xút trên miệng bình thu khí?
Viết 1 phương trình hoá học chứng minh chlorine vừa có tính oxi hoá, vừa có tính khử.
Cho 2,24 gam hỗn hợp gồm: CaCO3 và Mg vào một lượng dung dịch HCl dư. Sau khi phản ứng xảy ra hoàn toàn thấy thoát ra 0,7437 lít hỗn hợp khí ở đkc. Tính khối lượng muối có trong dung dịch thu được sau phản ứng.
Cho m gam KClO3 tác dụng với HCl đến khi phản ứng xảy ra hoàn toàn thấy thoát ra V lít khí Cl2 ở đkc. Biết lượng Cl2 sinh ra phản ứng vừa đủ với 0,56 gam Fe. Xác định m và V.
Dẫn một lượng dư khí chlorine vào dung dịch chứa hỗn hợp muối NaBr và KBr sau phản ứng thu được hỗn hợp hai muối, đồng thời thấy khối lượng muối giảm 4,45 gam.
Tính số mol chlorine đã tham gia phản ứng.








