Bộ 3 đề thi cuối kì 2 Hóa 10 Cánh diều cấu trúc mới có đáp án - Đề 2
28 câu hỏi
PHẦN I. Câu trắc nghiệm nhiều phương án lựa chọn. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
Cho phản ứng tổng quát sau:
aA + bB → mM + nN
Tốc độ trung bình của phản ứng tính theo chất A là
\[\overline v = \frac{{\Delta {C_A}}}{{\Delta t}}.\]
\[\overline v = - \frac{{\Delta {C_A}}}{{\Delta t}}.\]
\[\overline v = \frac{1}{a}.\frac{{\Delta {C_A}}}{{\Delta t}}.\]
\[\overline v = - \frac{1}{a}.\frac{{\Delta {C_A}}}{{\Delta t}}.\]
Chất làm tăng tốc độ phản ứng hóa học, nhưng không bị thay đổi về chất và lượng khi kết thúc phản ứng là
chất xúc tác.
chất ban đầu.
chất sản phẩm.
chất ức chế.
Đơn vị nào dưới đây là đơn vị của tốc độ phản ứng?
m/s.
mol/ lít.
mol L-1 s-1.
mol.lít/ s.
Hãy sắp xếp tốc độ các phản ứng sau theo chiều tăng dần: 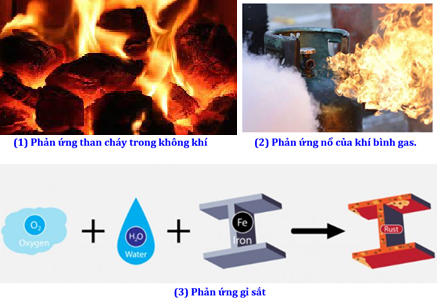
(1) < (2) < (3).
(2) < (3) < (1).
(3) < (2) < (1).
(3) < (1) < (2).
Khi cho một lượng xác định chất phản ứng vào bình để cho phản ứng hoá học xảy ra, tốc độ phản ứng sẽ
không đổi cho đến khi kết thúc.
tăng dần cho đến khi kết thúc.
chậm dần cho đến khi kết thúc.
tuân theo định luật tác dụng khối lượng.
Thí nghiệm nghiên cứu tốc độ phản ứng giữa kẽm (zinc) với dung dịch hydrochloric acid của hai nhóm học sinh được mô tả bằng hình sau:
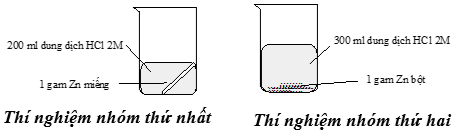
Kết quả cho thấy bọt khí thoát ra ở thí nghiệm của nhóm thứ hai mạnh hơn là do
nhóm thứ hai dùng axit nhiều hơn.
diện tích bề mặt kẽm bột lớn hơn kẽm miếng.
nồng độ kẽm bột lớn hơn.
áp suất tiến hành thí nghiệm nhóm thứ hai cao hơn nhóm thứ nhất.
Với phản ứng có \(\gamma = 2\). Nếu nhiệt độ tăng từ 30°C lên 70°C thì tốc độ phản ứng
tăng gấp 4 lần.
tăng gấp 8 lần.
giảm 4 lần.
tăng gấp 16 lần.
Halogen nào sau đây có màu nâu đỏ?
Chlorine.
Bromine.
Fluorine.
Iodine.
Đặc điểm chung của các nguyên tố nhóm halogen là
chất khí ở điều kiện thường.
có tính oxi hóa mạnh.
vừa có tính oxi hóa vừa có tính khử.
phản ứng mãnh liệt với nước.
Phản ứng nào dưới đây sai?
2Fe + 3Cl2 →t°2FeCl3.
H2 + I2⇌t°,Pt 2HI.
Cl2 + H2O ⇌ HCl + HClO.
F2 + H2O ⇌ HF + HFO.
Hydrogen halide có nhiệt độ sôi cao nhất là
HF.
HCl.
HBr.
HI.
Dung dịch nước của chất nào sau đây được sử dụng để khắc các chi tiết lên thủy tinh?
HF.
HCl.
HBr.
HI.
Chất nào sau đây không tạo kết tủa với AgNO3?
HCl.
NaBr.
KI.
NaF.
Cho các phát biểu sau về nguyên tử các nguyên tố nhóm VIIA:
(a). Có 7 electron hóa trị.
(b). Theo chiều tăng dần của điện tích hạt nhân nguyên tử thì độ âm điện giảm.
(c). Theo chiều tăng dần điện tích hạt nhân nguyên tử thì tính phi kim tăng.
(d). Theo chiều tăng dần điện tích hạt nhân nguyên tử thì bán kính nguyên tử giảm.
Số phát biểu đúng là
4.
3.
2.
1.
Cho phản ứng X2 + 2NaBr(aq) → 2NaX(aq) + Br2. X2 có thể là chất nào sau đây?
Cl2.
I2.
F2.
O2.
Cho các phát biểu sau về ion halide X-:
(a). Dùng dung dịch AgNO3 sẽ phân biệt được hai dung dịch NaCl và KBr.
(b). Với sulfuric acid đặc, các ion Cl-, Br-, I- thể hiện tính khử, ion F- không thể hiện tính khử.
(c). Tính khử của các ion halide giảm dần theo dãy: I-; Br-; Cl-.
(d). Ion Cl- kết hợp ion Ag+ tạo AgCl là chất không tan, màu vàng đậm.
Số phát biểu đúng là
1.
2.
3.
4.
Hòa tan 0,24 gam magnesium (Mg) trong dung dịch HCl dư. Sau phản ứng thu được thể tích khí H2 ở điều kiện chuẩn là
0,2479 lít.
0,4958 lít.
0,5678 lít.
1,487 lít.
Hòa tan hết 16,8 gam kim loại A hóa trị II trong dung dịch acid HCl, sau phản ứng thu được 7,437 lít khí H2 ở đkc. Kim loại A là
Fe.
Mg.
Cu.
Zn.
PHẦN II. Câu trắc nghiệm đúng sai. Thí sinh trả lời từ câu 1 đến câu 4. Trong mỗi ý a), b), c), d) ở mỗi câu, thí sinh chọn đúng hoặc sai. (Đ – S)
Phản ứng oxi hóa – khử là loại phản ứng xảy ra phổ biến trong tự nhiên, đời sống và sản xuất, trong phản ứng oxi hoá khử:
Chất khử là chất nhường electron.
Chất oxi hóa là chất nhận electron.
Quá trình oxi hóa là quá trình chất khử nhận electron.
Quá trình khử là quá trình chất oxi hóa nhường electron.
Cho phản ứng hoá học sau:
NH4HCO3 (s) \[ \to \] NH3 (g) + CO2 (g) + H2O (g)
Biết nhiệt tạo thành của các chất trong phản ứng được cho bởi bảng sau:
Chất | NH4HCO3 (s) | NH3 (g) | CO2 (g) | H2O (g) |
\[{\Delta _f}H_{298}^0\](kJmol-1) | –849,40 | –46,11 | –393,51 | –241,82 |
Phản ứng trên là phản ứng thu nhiệt.
Phản ứng toả ra nhiệt lượng 170 kJ.
Để NH4HCO3 ở nơi có nhiệt độ cao thì NH4HCO3 sẽ bị phân huỷ thành các khí.
Cần bảo quản NH4HCO3 ở nơi có nhiệt độ cao.
Tốc độ của một phản ứng hóa học:
là đại lượng đặc trưng cho sự thay đổi nồng độ của chất phản ứng hoặc sản phẩm trong một đơn vị thời gian.
được kí hiệu là n và có đơn vị là mol/L.
phụ thuộc vào nồng độ, áp suất, diện tích bề mặt, nhiệt độ và chất xúc tác.
là tốc độ tức thời của một phản ứng tại một thời điểm.
Tên gọi chung của các nguyên tố nhóm VIIA là halogen. Theo tiếng Hy Lạp “hals” là muối và “genes” là sinh ra, halogen nghĩa là sinh ra muối.
Sodium chloride là hợp chất quan trọng và phổ biến của chlorine trong tự nhiên, có nhiều trong nước biển và mỏ muối.
Rong biển chứa nguyên tố fluorine.
Halogen là các kim loại điển hình, có tính oxi hóa mạnh.
Chlorine phản ứng với dung dịch sodium hydroxide ở điều kiện thường, tạo thành nước Javel (Gia-ven).
Phần III. Câu hỏi trắc nghiệm yêu cầu trả lời ngắn. Thí sinh trả lời từ câu 1 đến câu 6.
Hydrochloric acid thường được dùng để đánh sạch lớp oxide, hydroxide, muối carbonate bám trên bề mặt kim loại trước khi sơn, hàn, mạ điện. Ứng dụng này dựa trên tính chất hóa học nào của hydrochloric acid?
Có 2 ống nghiệm, mỗi ống chứa 2 ml dung dịch muối X của potassium (kali). Cho vài giọt dung dịch AgNO3 vào ống nghiệm thứ nhất, thu được kết tủa màu vàng. Nhỏ vài giọt nước Br2 vào ống thứ hai, lắc đều rồi thêm hồ tinh bột, thấy có màu xanh. Xác định công thức hóa học của X.
Trong phòng thí nghiệm, một khí hydrogen halide (HX) được điều chế theo phản ứng sau: NaX (s) + H2SO4 (aq, đặc) HX↑ (g) + NaHSO4 (aq)
Cho biết HX có thể là những chất nào?
Cho một lượng khí Cl2 tác dụng hết với dung dịch chứa 6,18 muối NaX (X là một nguyên tố halogen) thu được 3,51 gam một muối duy nhất. Muối NaX là?
Có thể phân biệt các chất sau: HCl; HBr; NaI; KCl chứa trong các lọ riêng biệt, mất nhãn bằng các hoá chất lần lượt là?
Chia hỗn hợp gồm Mg và MgO thành hai phần bằng nhau:
Phần 1: Cho tác dụng hết với HCl thu được 3,4706 lít khí H2 (ở đkc), dung dịch sau phản ứng chứa 14,25 gam muối.
Phần 2: Hoà tan hoàn toàn bằng lượng vừa đủ 200 ml dung dịch HNO3 thì thu được 0,028 mol khí X và dung dịch chứa 1 muối duy nhất.
Công thức phân tử của khí X là?








