Bộ 10 Đề thi Đánh giá năng lực Bộ Quốc phòng phần Hoá học (có đáp án) - Đề số 1
25 câu hỏi
Đồng phân mạch hở và mạch vòng của glucose có thể chuyển hóa lẫn nhau. Cấu tạo dạng mạch hở của glucose và dạng vòng 6 cạnh α – glucose được cho ở hình bên. Liên kết nào trong số các liên kết được đánh số (1), (2), (3), (4) sẽ bị phá vỡ khi mở vòng α – glucose để chuyển hóa thành dạng mạch hở?
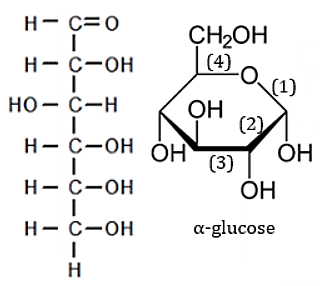
(4).
(3).
(2).
(1).
Phản ứng hóa học là quá trình phá vỡ các liên kết trong chất đầu và hình thành các liên kết mới để tạo thành sản phẩm. Sự phá vỡ liên kết cần cung cấp năng lượng, trong khi sự hình thành liên kết lại giải phóng năng lượng. Cho biết năng lượng liên kết trong các phân tử O 2 , N 2 và NO lần lượt là 494 kJ/mol, 945 kJ/mol và 607 kJ/mol. Biến thiên enthalpy chuẩn của phản ứng là
N 2 (g) + O 2 (g) → 2NO(g)
−225 kJ.
+225 kJ.
+832 kJ.
−832 kJ.
Có 5 ống nghiệm, mỗi ống chứa 2 mL dung dịch của một trong số các chất sau: K2CO3; CuCl2; MgSO4; Al(NO3)3, FeCl3, đều có nồng độ 0,01M. Sau khi cho dung dịch NaOH 0,1M dư vào lần lượt từng ống nghiệm và lắc đều, số lượng ống nghiệm quan sát thấy có kết tủa còn trong ống là
2.
3.
4.
5.
Trong cơ thể người, hemoglobin (Hb) kết hợp oxygen phản ứng của người được biểu diễn đơn giản như sau: H b + O 2 ⇌ H b O 2
Ở phổi, nồng độ oxygen lớn nên cân bằng trên chuyển dịch sang phải, hemoglobin kết hợp với oxygen. Khi đến các mô, nồng độ oxygen thấp, cân bằng trên chuyển dịch sang trái, giải phóng oxygen. Nếu thiếu oxygen ở não, con người có thể bị đau đầu, chóng mặt.
Vận dụng nguyên lý chuyển dịch cân bằng Le Chatelier, biện pháp nào sau đây giúp oxygen lên não nhiều hơn?
Hít thở sâu hoặc hít thở ở nơi có nhiều cây xanh.
Hít thở ở nơi không khí bị ô nhiễm và không có cây xanh.
Hít thở nhanh.
Hít thở trong phòng kín.
Trong phòng thí nghiệm, sodium (Na) được bảo quản bằng phương pháp ngâm trong dầu hỏa khan. Lí do của việc bảo quản theo phương pháp này là do
Na tan tốt trong dầu hỏa nên dễ dàng lưu trữ và vận chuyển.
Na hoạt động mạnh nên cần hạn chế tiếp xúc với nước, không khí và các tác nhân khác.
dầu hỏa tạo ra lớp màng ngăn cản sự bay hơi mạnh của Na vào không khí.
dầu hỏa giúp duy trì độ cứng của Na trong quá trình lưu trữ lâu dài.
Quá trình điện phân dung dịch NaCl bão hòa (điện cực trơ, có màng ngăn) và điện phân NaCl nóng chảy (điện cực trơ) có điểm giống nhau là
tại anode xảy ra sự oxi hóa ion C l − .
tại cathode xảy ra sự khử ion N a + .
tại anode xảy ra sự oxi hóa phân tử H 2 O .
tại cathode xảy ra sự khử phân tử H 2 O .
Trong phản ứng: C l 2 + H 2 O ⇌ HCl + HClO, chlorine thể hiện tính chất nào sau đây?
Tính oxi hóa.
Tính khử.
Tính acid.
Vừa có tính oxi hóa, vừa có tính khử.
Thực hiện các thí nghiệm sau:
(a) Cho kim loại Na vào dung dịch C u S O 4 .
(b) Cho kim loại Al vào dung dịch K O H dư.
(c) Cho dung dịch A g N O 3 vào dung dịch H C l .
(d) Cho N H 4 C l vào dung dịch B a ( O H ) 2 đun nóng.
(e) Cho dung dịch H 2 S O 4 vào dung dịch B a ( H C O 3 ) 2 .
Sau khi các phản ứng kết thúc, số thí nghiệm vừa thu được kết tủa vừa thu được chất khí là
5.
3.
2.
4.
Hòa tan 1,39 gam muối F e S O 4 ⋅ 7 H 2 O trong dung dịch H 2 S O 4 loãng được dung dịch X. Thêm từ từ từng giọt dung dịch K M n O 4 0 , 1 M vào dung dịch X, lắc đều cho đến khi bắt đầu xuất hiện màu tím thì dừng lại. Thể tích dung dịch K M n O 4 đã dùng là bao nhiêu m L ?
5.
10.
15.
20.
Nhỏ từ từ đến dư dung dịch ethylamine vào ống nghiệm (1) đựng dung dịch FeCl3; ống nghiệm (2) đựng dung dịch CuSO4; ống nghiệm (3) đựng dung dịch HCl có pha một vài giọt phenolphthalein; ống nghiệm (4) đựng nước bromine. Phát biểu nào sau đây sai?
Trong ống nghiệm (1) có kết tủa nâu đỏ.
Trong ống nghiệm (2) xuất hiện kết tủa màu xanh sau đó bị hoà tan thành dung dịch màu xanh lam.
Trong ống nghiệm (3) xuất hiện màu hồng.
Trong ống nghiệm (4) xuất hiện kết tủa trắng.
Cho sơ đồ chuyển hoá sau:
CaO → + X Y → + Z CaCO3 → + Z + X T → + E CaSO4
Biết: X, Y, Z, T, E là các hợp chất khác nhau; mỗi mũi tên ứng với một phương trình hoá học. Các chất Z, E thoả mãn sơ đồ trên lần lượt là
Na2CO3, H2SO4.
CO2, KHSO4.
NaHCO3, Na2SO4.
CO2, BaSO4.
Alcohol chứa liên kết O-H có số sóng hấp phụ trong khoảng 3 5 0 0 − 3 2 0 0 c m − 1 . Cho phổ IR của benzyl alcohol:
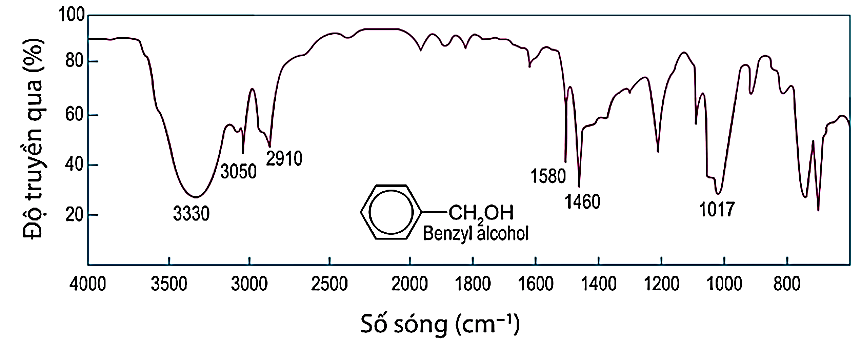
Peak đặc trưng với số sóng tương ứng của nhóm O-H trên phổ IR của benzyl alcohol là
3330.
3050.
1580.
1460.
Các nguyên tử trong pha khí ở trạng thái cơ bản có tính chất thuận từ (nếu có electron độc thân), hoặc nghịch từ (nếu không có electron độc thân). Ở pha khí, trong số các nguyên tử Na (Z = 11), Mg (Z = 12) và Al (Z = 13), (các) nguyên tử nào ở trạng thái cơ bản là nghịch từ?
Na, Mg.
Na, Al.
Mg.
Mg, Al.
Từ benzene, tổng hợp chất hữu cơ X2 theo sơ đồ chuyển hóa bên. Phát biểu nào sau đây đúng?
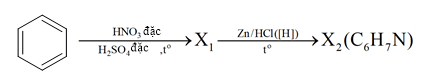
Benzene có nhiệt độ sôi cao hơn X2 do có tương tác van der Waals giữa các phân tử mạnh hơn.
Do ảnh hưởng của nhóm -NH2 nên phản ứng thể bromine ở nhân thơm của X2 khó hơn benzene.
Phản ứng chuyển hóa X1 thành X2 là phản ứng oxi hóa – khử.
Dung dịch X2 làm đổi màu quỳ tím sang màu xanh do X2 có tính base.
Khi để NaOH lâu ngày sẽ bị chuyển hóa một phần thành N a 2 C O 3 , làm khô thu được mẫu X. Đem cân lấy 1 gam mẫu X và hòa tan hoàn toàn trong 100 mL dung dịch HCl 0,5M đun nóng để đuổi hết C O 2 đi, thu được 100 mL dung dịch Y. Tiến hành chuẩn độ 10 mL dung dịch Y với chỉ thị phenolphathalein đến khi xuất hiện màu hồng nhạt thì hết 26,3 mL dung dịch NaOH 0,1M. Hàm lượng N a 2 C O 3 trong mẫu X là
1,06%.
2,12%.
10,6%.
21,2%.
Sau khi chưng cất cây sả bằng hơi nước, người ta dùng phương pháp chiết để tách riêng lớp tinh dầu ra khỏi nước. Phát biểu không đúng là
Hỗn hợp thu được tách thành hai lớp.
Lớp trên là tinh dầu sả, lớp dưới là nước.
Tinh dầu nặng hơn nước nên nằm phía dưới
Khối lượng riêng của tinh dầu sả nhẹ hơn nước.
Ethanol có công thức là C 2 H 5 O H , được dùng để sản xuất đồ uống có cồn, sản xuất xăng sinh học, làm dung môi pha chế nước hoa, mỹ phẩm,… Nhận định đúng về ethanol là
Hoà tan được C u ( O H ) 2 trong môi trường kiềm tạo dung dịch màu xanh lam đậm.
Xăng E5 RON 92 gồm 8% ethanol và 92% xăng RON 92 về thể tích.
Việc lạm dụng rượu, bia quá mức sẽ gây ảnh hưởng nghiêm trọng đến sức khỏe con người.
Ethanol có nhiệt độ sôi thấp hơn so với propane và dimethyl ether.
Malic acid là một loại acid tự nhiên, thường được tìm thấy trong các loại trái cây, đặc biệt là quả táo và các loại rau. Công thức cấu tạo của malic acid được cho như sau:
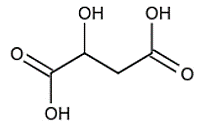
Phát biểu nào sau đây về malic acid là đúng?
Công thức phân tử của malic acid là C 4 H 7 O 5 .
1,0 mol malic acid phản ứng được tối đa với 2,0 mol K.
1,0 mol malic acid phản ứng được tối đa với 2,0 mol NaOH.
Dung dịch malic acid không tác dụng với N a H C O 3 .
Cho sơ đồ chuyển hóa:
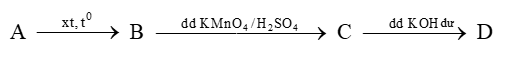
Biết A, B, C, D là các hợp chất hữu cơ. A là hydrocarbon (điều kiện thường ở trạng thái khí) có % m C = 9 0 % . Phân tử các chất B, C, D có tính đối xứng cao. B là hợp chất chứa vòng benzene. Cho các phát biểu sau:
(a) A là alkyne.
(b) B tác dụng với C l 2 (chiếu sáng, tỉ lệ 1 : 1) thu được một dẫn xuất monochloro duy nhất.
(c) Phản ứng của B với dung dịch K M n O 4 xảy ra ở nhiệt độ thường.
(d) Phần trăm khối lượng nguyên tố O trong D là 34,78%.
Số phát biểu đúng là
4.
2.
1.
3.
Phổ IR của hợp chất hữu cơ X (chỉ chứa C, H, O) và số sóng hấp thụ của một số
loại liên kết được biểu diễn ở hình sau:
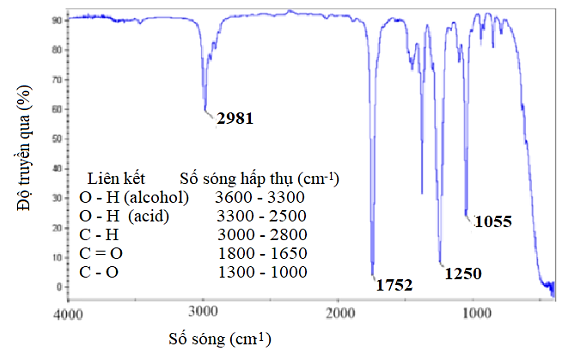
Tín hiệu hồng ngoại của liên kết O - H có đặc điểm là chân rộng và đỉnh tù. Phổ
khối lượng (MS) của hợp chất X có peak ion phân tử ở giá trị m/z = 74.
Cho 0,1 mol chất X tác dụng với 175 mL dung dịch NaOH 1,0 M, cô cạn dung dịch
sau phản ứng thu được a gam chất rắn khan, trong đó có chứa chất hữu cơ Y, biết
M Y > 8 1 . Giá trị của a là bao nhiêu (nhập đáp án vào ô trống)?
11,2
Cho các phát biểu sau:
(1) Các amino acid là chất rắn ở điều kiện thường.
(2) Glycine tác dụng với ethanol có mặt HCl thu được ester là
(3) Ở pH = 2, alanine di chuyển về phía cực âm dưới tác dụng của điện trường.
(4) Cho ethylamine dư vào dung dịch C u S O 4 thu được dung dịch có màu xanh đặc trưng.
(5) Methylamine có tính base yếu hơn ammonia.
Các phát biểu đúng là
(1), (3) và (4).
(1), (2) và (5).
(2), (3) và (4).
(1), (3) và (5).
Carbohydrate nào sau đây thuộc loại polysaccharide?
Glucose.
Tinh bột.
Fructose.
Saccharose.
Trong công nghiệp, ammonia được tổng hợp theo quá trình Haber (còn được gọi là quá trình Haber – Bosch). Phương trình hóa học của phản ứng diễn ra như sau:
N 2 ( g ) + 3 H 2 ( g ) ⇌ 2 N H 3 ( g ) Δ r H 2 9 8 o = − 9 1 , 8 k J
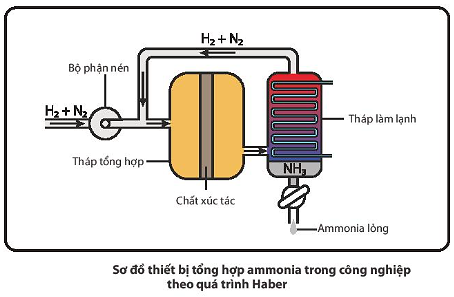
Quá trình Haber được thực hiện như sau:
- Hỗn hợp nitrogen và hydrogen (tỉ lệ mol 1 : 3) được nén ở áp suất cao và đưa vào tháp tổng hợp ammonia trong điều kiện nhiệt độ, áp suất và chất xúc tác thích hợp.
- Hỗn hợp khí đi ra từ tháp tổng hợp gồm N 2 , H 2 và N H 3 được dẫn đến tháp làm lạnh. Ở đây, N H 3 hóa lỏng và được tách riêng, còn hỗn hợp N 2 và H 2 chưa phản ứng được đưa trở lại tháp tổng hợp.
Vai trò của nitrogen trong phản ứng tổng hợp ammonia là
chất khử.
chất oxi hóa.
vừa là chất khử, vừa là chất oxi hóa.
acid.
Trong công nghiệp, ammonia được tổng hợp theo quá trình Haber (còn được gọi là quá trình Haber – Bosch). Phương trình hóa học của phản ứng diễn ra như sau:
N 2 ( g ) + 3 H 2 ( g ) ⇌ 2 N H 3 ( g ) Δ r H 2 9 8 o = − 9 1 , 8 k J

Quá trình Haber được thực hiện như sau:
- Hỗn hợp nitrogen và hydrogen (tỉ lệ mol 1 : 3) được nén ở áp suất cao và đưa vào tháp tổng hợp ammonia trong điều kiện nhiệt độ, áp suất và chất xúc tác thích hợp.
- Hỗn hợp khí đi ra từ tháp tổng hợp gồm N 2 , H 2 và N H 3 được dẫn đến tháp làm lạnh. Ở đây, N H 3 hóa lỏng và được tách riêng, còn hỗn hợp N 2 và H 2 chưa phản ứng được đưa trở lại tháp tổng hợp.
Trong phản ứng tổng hợp ammonia từ nitrogen và hydrogen. Hiệu suất phản ứng tổng hợp ammonia tăng nếu:
Giảm áp suất, tăng nhiệt độ, có xúc tác.
Giảm áp suất, giảm nhiệt độ, có xúc tác.
Tăng áp suất, giảm nhiệt độ, có xúc tác.
Tăng áp suất, tăng nhiệt độ, có xúc tác.
Trong công nghiệp, ammonia được tổng hợp theo quá trình Haber (còn được gọi là quá trình Haber – Bosch). Phương trình hóa học của phản ứng diễn ra như sau:
N 2 ( g ) + 3 H 2 ( g ) ⇌ 2 N H 3 ( g ) Δ r H 2 9 8 o = − 9 1 , 8 k J

Quá trình Haber được thực hiện như sau:
- Hỗn hợp nitrogen và hydrogen (tỉ lệ mol 1 : 3) được nén ở áp suất cao và đưa vào tháp tổng hợp ammonia trong điều kiện nhiệt độ, áp suất và chất xúc tác thích hợp.
- Hỗn hợp khí đi ra từ tháp tổng hợp gồm N 2 , H 2 và N H 3 được dẫn đến tháp làm lạnh. Ở đây, N H 3 hóa lỏng và được tách riêng, còn hỗn hợp N 2 và H 2 chưa phản ứng được đưa trở lại tháp tổng hợp.
Thực hiện phản ứng tổng hợp ammonia từ N 2 và H 2 với hiệu suất h%, thu được hỗn hợp X chứa 10% N H 3 (về thể tích). Cho X tác dụng với CuO dư, nung nóng. Sau khi phản ứng xảy ra hoàn toàn, thu được hỗn hợp Y (gồm khí và hơi) và hỗn hợp rắn Z có khối lượng giảm đi so với khối lượng CuO ban đầu là 12,8 gam. Làm lạnh Y, còn 7,437 lít khí (đkc) không bị ngưng tụ. Giá trị của h là
18,75%.
18,57%.
81,25%.
16,67%.








