Bộ 10 Đề thi Đánh giá năng lực Bộ Quốc phòng phần Hoá học (có đáp án) - Đề số 10
25 câu hỏi
Nguyên tử của nguyên tố X có cấu hình electron 1s22s22p63s1. Tính chất nào sau đây của nguyên tố X là không đúng?
Ở dạng đơn chất, X tác dụng với nước tạo ra khí hydrogen.
Hợp chất của X với chlorine là hợp chất ion.
Nguyên tử X dễ nhận thêm 1 electron để tạo cấu hình lớp vỏ 3s2 bền.
Hợp chất của X với oxygen có tính chất tan được trong nước tạo dung dịch có môi trường base.
Poly(ethylene oxide) được tổng hợp theo phương trình hoá học sau:
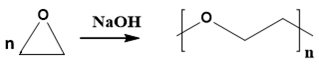
Poly(ethylene oxide) được điều chế bằng phản ứng
thế.
trùng hợp.
trao đổi.
trùng ngưng.
Khi cho ethylene tác dụng với dung dịch bromine trong điều kiện thường, xảy ra phản ứng cộng electrophile theo sơ đồ sau:
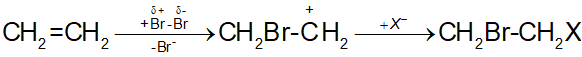
Ngoài sản phẩm chính là CH2Br-CH2Br, còn thu được một lượng nhỏ sản phẩm hữu cơ A, công thức là
CH2Br-CH3.
CH3-CHBr-OH.
CH2Br-CH2OH.
CH2Br-CHBr-OH.
Cho peptide X có công thức cấu tạo:
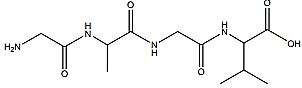
Phát biểu nào sau đây không đúng?
X có thể tham gia phản ứng với dung dịch acid HCl thu được muối.
Thủy phân hoàn toàn X trong NaOH dư thu được 4 muối.
Phân tử X có 3 liên kết peptide.
X phản ứng với Cu(OH)2 trong môi trường kiềm tạo phức chất có màu tím.
Phát biểu nào sau đây là không đúng?
Liên kết σ có thể tạo thành từ sự xen phủ trục của hai AO khác loại.
Liên kết σ bền vững hơn liên kết π.
Các AO p không có khả năng xen phủ tạo liên kết σ.
Các AO s chỉ có khả năng xen phủ tạo liên kết σ.
Phức chất nào sau đây là phức chất aqua ?
[Cu(NH3)4(OH2)2]2+.
[Pt(NH3)2Cl2].
[Ti(OH2)6]3+.
[Fe(OH)3(OH2)3].
Cho công thức cấu tạo của 2 chất sau:
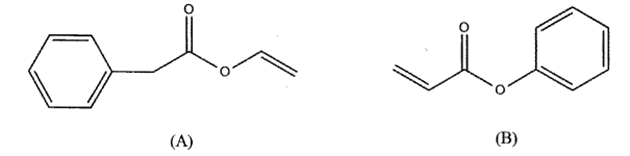
Cho các phát biểu sau:
(a). (B) được điều chế từ phản ứng ester hóa giữa acrylic acid với phenol.
(b). Thủy phân (A) trong kiềm thu được sản phẩm có chất CH3CHO.
(c). (A) là vinyl benzoate, B là phenyl acrylate.
(d). (A) và (B) đều có công thức phân tử là C9H8O2.
Các phát biểu đúng là
(a) và (b).
chỉ có (b).
(c) và (d).
chỉ có (d).
Cho các phát biểu sau:
(a) Hoà tan hết CaCO3 bằng một lượng dư HCl thu được dung dịch X. Cô cạn dung dịch X thu được chất rắn Y. Đốt nóng Y trên ngọn lửa đèn cồn thấy ngọn lửa có màu đỏ cam.
(b) Cho một mẫu nhỏ Ca vào dung dịch Na2CO3. Hiện tượng xảy ra là mẫu Ca tan dần, sủi bọt khí và xuất hiện kết tủa trắng.
(c) Ca, Ba, Sr đều tác dụng được với nước tạo dung dịch làm quỳ tím hóa đỏ.
(d) Một mẫu nước cứng có chứa: 0,01 mol Ca2+; 0,03 mol HCO3- và x mol Mg2+. Nếu đun nóng mẫu nước cứng này thì sẽ loại bỏ được khối lượng cặn là 14,2 gam.
Số phát biểu đúng là
2.
4.
3.
1.
Butane là một trong hai thành phần chính của khí LPG - Khí dầu mỏ hóa lỏng. Phản ứng đốt cháy butane sau:
C 4 H 1 0 ( g ) + O 2 ( g ) → C O 2 ( g ) + H 2 O ( g )
Biết năng lượng liên kết trong các hợp chất cho trong bảng sau:
| Liên kết | Phân tử | Eb (kJ/mol) | Liên kết | Phân tử | Eb (kJ/mol) |
| C – C | C 4 H 1 0 | 346 | C = O | C O 2 | 799 |
| C – H | C 4 H 1 0 | 418 | O – H | H 2 O | 467 |
| O = O | O 2 | 495 |
Giả thiết mỗi ấm nước chứa 2 L nước ở 2 5 o C , nhiệt dung của nước là 4,2 J/g.K, có 40% nhiệt đốt cháy butane bị thất thoát ra ngoài môi trường. Một bình gas chứa 12 kg butane có thể đun sôi bao nhiêu ấm nước?
518.
612.
305.
204.
Trong quy trình sản xuất sulfuric acid ( H 2 S O 4 ) có giai đoạn dùng dung dịch H 2 S O 4 98% hấp thụ sulfur trioxide ( S O 3 ) thu được oleum ( H 2 S O 4 . S O 3 ). Sulfur trioxide được tạo thành bằng cách oxi hóa sulfur dioxide bằng oxygen hoặc lượng dư không khí ở nhiệt độ 4 5 0 o C – 5 0 0 o C , chất xúc tác vanadium(V) oxide ( V 2 O 5 ) theo phương trình hóa học:
2 S O 2 ( g ) + O 2 ( g ) ⇌ V 2 O 5 , 4 5 0 0 C − 5 0 0 0 C 2 S O 3 ( g ) Δ r H 2 9 8 0 = − 1 9 8 , 4 k J
Cân bằng hóa học sẽ chuyển dịch theo chiều nghịch khi nào?
Tăng nhiệt độ của hệ phản ứng.
Tăng nồng độ của khí S O 2 .
Tăng nồng độ của khí O 2 .
Dùng dung dịch H 2 S O 4 98% hấp thụ S O 3 sinh ra.
Phương trình hóa học nào sau đây biểu diễn quá trình điều chế kim loại bằng phương pháp điện phân dung dịch?
C u C l 2 → C u + C l 2 .
2 A l + C r 2 O 3 → A l 2 O 3 + 2 C r .
2 A l 2 O 3 → 4 A l + 3 O 2 .
Z n + C u S O 4 → Z n S O 4 + C u .
Công thức Lewis là công thức biểu diễn cấu tạo phân tử qua các liên kết và các electron hóa trị riêng. Công thức Lewis của HCl là
H – Cl.
HCl.
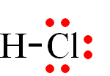 .
.
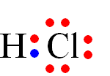 .
.
Thực hiện các thí nghiệm sau:
(1) Cho Na vào dung dịch C u S O 4 .
(2) Điện phân dung dịch C u S O 4 bằng điện cực trơ.
(3) Thổi luồng khí H 2 đến dư qua ống nghiệm chứa C u O nung nóng.
(4) Nung nóng hỗn hợp gồm Al và CuO trong khí trơ.
(5) Cho bột Fe vào dung dịch C u C l 2 .
Sau khi kết thúc thí nghiệm, số trường hợp thu được C u đơn chất là
5.
2.
4.
3.
Hòa tan hết 47,4 gam phèn chua có công thức K A l ( S O 4 ) 2 . 1 2 H 2 O vào nước, thu được dung dịch X. Cho X phản ứng với 200 mL dung dịch B a ( O H ) 2 1 M được m gam kết tủa. Giá trị của m là
62,2.
54,4.
46,6.
7,8.
Chuẩn độ hàm lượng ion F e 2 + trong môi trường acid (chứa trong bình tam giác) bằng dung dịch K M n O 4 đã biết nồng độ (chứa trên burette). Trong quá trình chuẩn độ, nếu dung dịch trên burette được thêm vào bình tam giác quá nhanh thì trong bình sẽ xuất hiện kết tủa nâu M n O 2 theo phương trình hoá học dưới đây, dẫn đến sai lệch kết quả chuẩn độ:
M n O 4 − ( a q ) + H + ( a q ) + F e 2 + ( a q ) → M n O 2 ( s ) + F e 3 + ( a q ) + H 2 O ( 1 )
Giả sử một học sinh thao tác sai, làm 60% lượng M n O 4 − chuẩn độ chuyển thành M n O 2 (phần còn lại vẫn phản ứng tạo M n 2 + ), tổng lượng F e 2 + bị oxi hoá là 2,2 mmol. Thể tích dung dịch K M n O 4 0,020 M đã dùng tăng bao nhiêu mL so với khi chuẩn độ với thao tác phù hợp?
22 mL.
28,95 mL.
6,95 mL.
8,95 mL.
Trong công nghiệp, nhôm được tách ra từ quặng bauxite bằng cách nào sau đây?
Nung nóng quặng bauxite.
Nung nóng quặng bauxite với carbon.
Nung nóng quặng bauxite với hydrogen.
Tinh chế quặng bauxide, sau đó điện phân nóng chảy A l 2 O 3 .
Formalin có tác dụng diệt khuẩn nên được dùng để bảo quản mẫu sinh vật, tẩy uế, khử trùng,... Formalin là
dung dịch rất loãng của aldehyde formic.
dung dịch aldehyde formic 37-40%.
aldehyde formic nguyên chất.
tên gọi khác của aldehyde formic nguyên chất.
Cho hợp chất hữu cơ X có công thức dạng khung phân tử:
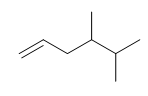
Phát biểu nào dưới đây là đúng?
Công thức phân tử của X là C 8 H 1 8 .
X thuộc dãy đồng đẳng alkane.
X phản ứng với H 2 (xúc tác Ni, đun nóng).
X phản ứng A g N O 3 / N H 3 tạo kết tủa màu vàng nhạt.
Tiến hành thí nghiệm phản ứng xà phòng hóa theo các bước sau đây:
Bước 1: Cho vào bát sứ khoảng 1 gam chất béo và 2 – 2,5 mL dung dịch NaOH 40%.
Bước 2: Đun hỗn hợp sôi nhẹ và liên tục khuấy đều bằng đũa thủy tinh. Thỉnh thoảng thêm vài giọt nước cất để giữ cho thể tích của hỗn hợp không đổi.
Bước 3: Sau 8 – 10 phút, rót thêm vào hỗn hợp 4 – 5 mL dung dịch NaCl bão hòa nóng, khuấy nhẹ.
Cho các phát biểu sau:
(a) Sau bước 3, thấy có lớp chất rắn màu trắng nổi lên trên.
(b) Mục đích của việc thêm dung dịch NaCl bão hòa để tách muối của acid béo.
(c) Nếu thay chất béo bằng ethyl acetate, hiện tượng quan sát được giống nhau.
(d) Sản phẩm rắn của thí nghiệm thường dùng để sản xuất xà phòng.
(e) Phần dung dịch còn lại sau bước 3 có khả năng hòa tan C u ( O H ) 2 .
Số phát biểu đúng là
5.
4.
2.
3.
Phản ứng tổng hợp glucose trong cây xanh cần được cung cấp năng lượng từ ánh sáng mặt trời:
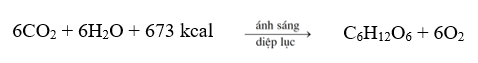
Cứ trong một phút, mỗi cm2 lá xanh nhận được 0,5 cal năng lượng mặt trời, nhưng chỉ có 10% được sử dụng vào phản ứng tổng hợp glucose. Thời gian để một cây có 1000 lá xanh (diện tích mỗi lá 10 cm2) sản sinh được 18 gam glucose là bao nhiêu phút? Kết quả làm tròn đến hàng đơn vị. (nhập đáp án vào ô trống)
Đáp án: ____
135
135
Cho các phát biểu sau:
(1) Khi làm đậu phụ xảy ra sự đông tụ protein.
(2) Enzyme bị biến tính không thể thực hiện vai trò xúc tác.
(3) Không nên vắt chanh vào sữa khi uống.
(4) Sự thủy phân protein xảy ra trong quá trình làm nước mắm hay nấu nước tương.
(5) Mỗi enzyme có một nhiệt độ tối ưu. Tại nhiệt độ tối ưu, enzyme có hoạt tính tối đa làm tốc độ phản ứng nhanh nhất.
Các phát biểu đúng là
(1), (2), (3).
(1), (3), (4), (5).
(2), (3), (4), (5).
(1), (2), (3), (4), (5).
Amino acid X chứa một nhóm − N H 2 và một nhóm − C O O H trong phân tử. Y là ester của X với alcohol đơn chức, M Y = 8 9 . Công thức của X, Y lần lượt là
H 2 N − C H 2 − C O O H , H 2 N − C H 2 − C O O C H 3 .
H 2 N − [ C H 2 ] 2 − C O O H , H 2 N − [ C H 2 ] 2 − C O O C 2 H 5 .
H 2 N − [ C H 2 ] 2 − C O O H , H 2 N − [ C H 2 ] 2 − C O O C H 3 .
H 2 N − C H 2 − C O O H , H 2 N − C H 2 − C O O C 2 H 5 .
Alkane được dùng làm nhiên liệu, nguyên liệu … trong đời sống và trong các ngành công nghiệp. Với alkane có số nguyên tử cacbon từ C 1 − C 4 được dùng làm khí đốt, khí hóa lỏng. Với các alkane có số nguyên tử cacbon từ C 5 − C 2 0 dùng làm xăng dầu, chất đốt. Với các alkane có số nguyên tử cacbon từ C 2 0 trở lên dùng để sản xuất nến, dầu mỡ bôi trơn. Alkane còn là nguyên liệu để tổng hợp một số chất hữu cơ như ethylene, acetylene …
Alkane là những hydrocarbon no, mạch hở, có công thức chung là
C n H 2 n + 2 ( n ≥ 1 ) .
C n H 2 n ( n ≥ 2 ) .
C n H 2 n − 2 ( n ≥ 2 ) .
C n H 2 n − 6 ( n ≥ 6 ) .
Alkane được dùng làm nhiên liệu, nguyên liệu … trong đời sống và trong các ngành công nghiệp. Với alkane có số nguyên tử cacbon từ C 1 − C 4 được dùng làm khí đốt, khí hóa lỏng. Với các alkane có số nguyên tử cacbon từ C 5 − C 2 0 dùng làm xăng dầu, chất đốt. Với các alkane có số nguyên tử cacbon từ C 2 0 trở lên dùng để sản xuất nến, dầu mỡ bôi trơn. Alkane còn là nguyên liệu để tổng hợp một số chất hữu cơ như ethylene, acetylene …
Phản ứng đặc trưng của các alkane là
phản ứng tách.
phản ứng thế.
phản ứng cộng.
phản ứng oxi hóa.
Alkane được dùng làm nhiên liệu, nguyên liệu … trong đời sống và trong các ngành công nghiệp. Với alkane có số nguyên tử cacbon từ C 1 − C 4 được dùng làm khí đốt, khí hóa lỏng. Với các alkane có số nguyên tử cacbon từ C 5 − C 2 0 dùng làm xăng dầu, chất đốt. Với các alkane có số nguyên tử cacbon từ C 2 0 trở lên dùng để sản xuất nến, dầu mỡ bôi trơn. Alkane còn là nguyên liệu để tổng hợp một số chất hữu cơ như ethylene, acetylene …
Một loại bình gas có chứa 13 kg khí hóa lỏng có thành phần chính là khí methane, ethane và một số thành phần khác, trong đó tỉ lệ thể tích của methane : ethane là 85 : 15 (thành phần khác không đáng kể). Khi đốt cháy hoàn toàn, 1 mol methane cháy tỏa ra lượng nhiệt là 802 kJ và 1 mol ethane cháy tỏa lượng nhiệt là 1428 kJ. Trung bình, lượng nhiệt tiêu thụ từ đốt khí gas trên của một hộ gia đình X là 10000 kJ/ngày, hiệu suất sử dụng nhiệt là 62%, giá của bình gas trên là 450 000 đồng. Số tiền một hộ gia đình X cần trả cho việc mua gas trong một tháng (30 ngày) gần nhất với giá trị nào sau đây?
345 000 đồng.
297 000 đồng.
414 000 đồng.
333 000 đồng.








