Bộ 10 Đề thi Đánh giá năng lực Bộ Quốc phòng phần Hoá học (có đáp án) - Đề số 9
25 câu hỏi
Nguyên tố X ở ô thứ 17 của bảng tuần hoàn. Có các phát biểu sau:
(a) X có độ âm điện lớn và là một phi kim mạnh.
(b) X có thể tạo thành ion bền có dạng X+.
(c) Oxide cao nhất của X có công thức X2O5 và là acidic oxide.
(d) Hydroxide của X có công thức HXO4 và là acid mạnh.
Số phát biểu đúng là
1.
2.
3.
4.
Phosphine ( P H 3 ) là một chất khí không màu, nhẹ hơn không khí, rất độc và dễ cháy. Khí này thường thoát ra từ xác động vật thối rữa, khi có mặt diphosphine ( P 2 H 4 ) thường tự bốc cháy trong không khí, đặc biệt ở thời tiết mưa phùn, tạo hiện tượng “ma trơi” ngoài nghĩa địa.
Phản ứng cháy của phosphine: 2 P H 3 ( g ) + 4 O 2 ( g ) → P 2 O 5 ( s ) + 3 H 2 O ( l )
Biết nhiệt tạo thành chuẩn của các chất cho trong bảng sau:
Chất | PH3(g) | P2O5(s) | H2O(l) |
ΔfH298o (kJ/mol) | 5,4 | −365,8 | −285,8 |
Phản ứng cháy của phosphine có đặc điểm
Δ r H 2 9 8 o < 0, phản ứng tỏa nhiệt.
Δ r H 2 9 8 o > 0, phản ứng toả nhiệt.
Δ r H 2 9 8 o < 0, phản ứng thu nhiệt.
Δ r H 2 9 8 o > 0, phản ứng thu nhiệt.
Điện khí, hay còn được gọi là điện được sản xuất từ khí tự nhiên, điển hình nhất là LNG (Liquefied Natural Gas). Đầu tiên, khí tự nhiên được khai thác tại các mỏ khí, được làm sạch và làm lạnh để chuyển đổi thành khí thiên nhiên hóa lòng LNG (thuận tiện cho việc tồn trữ và vận chuyển; thành phần chứa 95% CH4, 5% C2H6 về số mol). Sau đó, LNG được vận chuyển tới các nhà máy điện khí để tạo ra điện năng. Một nhà máy điện khí có sản lượng điện 3,6.106 kWh/ngày (1 kWh = 3600 kJ), các nhiên liệu bị đốt cháy hoàn toàn (biết 60% nhiệt lượng tỏa ra của quá trình đốt cháy được chuyển hóa thành điện năng). Biết CH4, C2H6 cháy theo các phương trình:
CH4(g) + 2O2(g) → CO2(g) + 2H2O(g)
C2H6(g) + 3,5O2(g) → 2CO2(g) + 3H2O(g)
| Chất | CH4(g) | C2H6(g) | CO2(g) | H2O(g) |
| Δ f H 2 9 8 o (kJ/mol) | -74,6 | -84,7 | -393,5 | -241,8 |
Mỗi ngày nhà máy điện khí cần sử dụng bao nhiêu tấn LNG (Chỉ làm tròn phép tính cuối, làm tròn đến hàng đơn vị)
433.
432.
342.
243.
Hai kim loại Cu, Fe có E C u 2 + / C u 0 = 0 , 3 4 V ; E Z n 2 + / Z n 0 = - 0 , 7 6 V và một pin Galvani Zn-Cu được thiết lập như hình vẽ ở 25 °C.
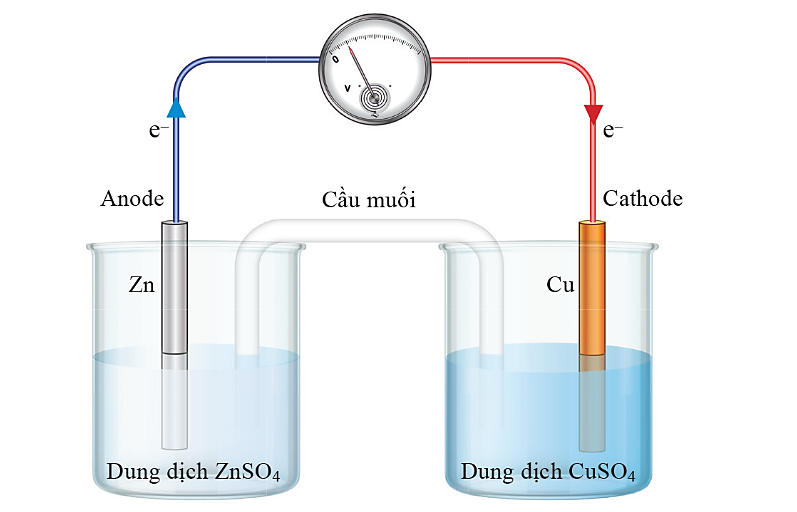
Giả sử trong thí nghiệm này, cầu muối là ống thủy tinh chứa thạch được tẩm dung dịch muối KNO3 bão hòa. Dung dịch ZnSO4 và CuSO4 ban đầu trong cốc thủy tinh đều có nồng độ là 1M.
Phát biểu nào dưới đây không đúng?
Nồng độ Zn2+ trong dung dịch sẽ tăng lên, còn nồng độ Cu2+ trong dung dịch CuSO4 sẽ giảm xuống.
Dòng điện đi qua vôn kế là dòng electron di chuyển từ cực dương là thanh Cu sang cực âm là thanh Zn.
Trong cầu muối ion K+ sẽ di chuyển vào dung dịch CuSO4 còn ion N O 3 − sẽ di chuyển vào dung dịch ZnSO4.
Nếu điện trở của dây dẫn không đáng kể thì pin mới hoạt động.
Cho phản ứng hóa học sau:
4CrO3 + C2H5OH → 2CO2↑ + 2Cr2O3 + 3H2O
Cho hai mệnh đề sau:
- Mệnh đề khẳng định (1): Phản ứng của CrO3 với C2H5OH được ứng dụng trong máy đo nồng độ cồn của cảnh sát giao thông.
- Mệnh đề giải thích (2): Khi tài xế hà hơi thở vào dụng cụ phân tích nồng độ cồn của cảnh sát giao thông, nếu trong hơi thở có chứa hơi rượu thì hơi rượu sẽ tác dụng với CrO3 có màu da cam và biến thành Cr2O3 có màu xanh đen.
Cả (1) và (2) đều đúng, trong đó (2) là lời giải thích đúng cho khẳng định (1).
Cả (1) và (2) đều đúng, nhưng (2) không phải lời giải thích đúng cho khẳng định (1).
Mệnh đề khẳng định (1) đúng, mệnh đề giải thích (2) sai.
Mệnh đề khẳng định (1) sai, mệnh đề giải thích (2) đúng.
Chất X là một hợp chất carbonyl có công thức phân tử C3H6O được sử dụng phổ biến với vai trò là dung môi hữu cơ. Khi cho X vào nước bromine không có phản ứng hoá học xảy ra. Phát biểu nào sau đây là không đúng về chất X?
Chất X có tên là propanone.
Chất X tan được trong nước.
Chất X có 3 đồng phân cấu tạo mạch hở.
Chất X không tạo được kết tủa màu vàng khi cho X vào dung dịch iodine trong NaOH.
Một nhà máy sản xuất túi nilon tử PE cần sản xuất túi đựng hình chữ nhật có kích thước là 20 × 30 cm (hình dưới), bề dày của lớp nylon là 0,02 cm. Biết hiệu suất phản ứng trùng hợp ethylene để điều chế PE là 60%, quá trình chuyển nhựa thành túi có hiệu suất là 95% và biết khối lượng riêng của nhựa PE là 0 , 9 5 g / c m 3 . Khối lượng nguyên liệu ethylene dùng để sản xuất đơn hàng 100 000 túi trên (đơn vị: tấn) là

4,00.
2,28.
3,80.
2,40.
Cho các phát biểu sau:
(a) Oxi hóa glucose bằng thuốc thử Tollens thu được sản phẩm cuối cùng là gluconic acid.
(b) Dung dịch saccharose có thể hòa tan C u ( O H ) 2 trong môi trường kiềm ở điều kiện thường.
(c) Cellulose trinitrate là nguyên liệu để sản xuất thuốc súng không khói.
(d) Trong amilopectin, các gốc α-glucose chỉ liên kết với nhau bằng liên kết α-1,4-glycoside.
(e) Glucose và fructose có thể chuyển hóa lẫn nhau trong môi trường kiềm.
(g) Glucose là hợp chất hữu cơ đa chức có công thức dạng C 6 ( H 2 O ) 6 .
Số phát biểu đúng là
5.
6.
4.
3.
Methane là thành phần chính của khí thiên nhiên. Xét phản ứng đốt cháy methane:
C H 4 ( g ) + 2 O 2 ( g ) → C O 2 ( g ) + 2 H 2 O ( l ) Δ r H 2 9 8 o = − 8 9 0 , 3 k J
Biết nhiệt tạo thành chuẩn của C O 2 (g) và H 2 O (l) tương ứng là −393,5 kJ/mol và −285,8 kJ/mol.
Hãy tính nhiệt tạo thành chuẩn của khí methane?
+74,8 kJ.
−74,8 kJ.
−211 kJ.
+211 kJ.
Trong phản ứng điều chế khí oxygen trong phòng thí nghiệm bằng cách nhiệt phân muối potassium chlorate ( K C l O 3 ).
(a) Dùng chất xúc tác manganese dioxide ( M n O 2 ).
(b) Nung hỗn hợp potassium chlorate và manganese dioxide ở nhiệt độ cao.
(c) Dùng phương pháp dời nước để thu khí oxygen.
Những biện pháp nào dưới đây được sử dụng để làm tăng tốc độ phản ứng là
a, c.
a, b.
b, c.
a, b, c.
Tiến hành mạ bạc cho một huy chương bằng kim loại đồng (copper) theo sơ đồ minh họa bên dưới.
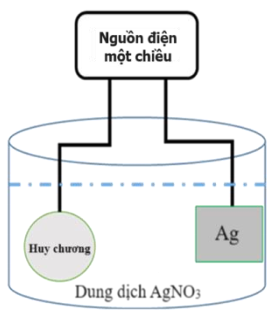
Phát biểu đúng là
Huy chương được nối với anode và tại anode, Cu bị oxi hoá.
Huy chương được nối với anode và tại anode, Ag+ bị khử.
Huy chương được nối với cathode và tại cathode, Cu2+ bị khử.
Huy chương được nối với cathode và tại cathode, Ag+ bị khử.
Khi mở vòi nước máy, nếu chú ý một chút sẽ phát hiện mùi lạ. Đó là do nước máy còn lưu giữ vết tích của chất khử trùng. Đó chính là chlorine và người ta giải thích khả năng diệt khuẩn là do
chlorine độc nên có tính sát trùng.
chlorine có tính oxi hóa mạnh.
chlorine tác dụng với nước tạo ra HClO chất này có tính oxi hóa mạnh.
một nguyên nhân khác.
Tiến hành các thí nghiệm sau:
(a) Nung nóng hỗn hợp gồm K M n O 4 và K C l O 3 .
(b) Dẫn khí C O dư đi qua ống sứ đựng bột A l 2 O 3 nung nóng.
(c) Điện phân dung dịch N a C l bão hòa (điện cực trơ, màng ngăn xốp).
(d) Cho bột Cr vào dung dịch H 2 S O 4 loãng, đun nóng.
(e) Cho dung dịch F e C l 2 vào dung dịch A g N O 3 dư.
(g) Cho mẩu nhỏ Na vào dung dịch K 2 S O 4 dư.
Sau khi phản ứng hoàn toàn, số thí nghiệm có sinh ra đơn chất là
3.
4.
6.
5.
Muối Mohr là một muối kép ngậm 6 phân tử nước được tạo thành từ hỗn hợp đồng mol iron(II) sulfate ngậm 7 phân tử nước và ammonium sulfate khan.
F e S O 4 . 7 H 2 O + ( N H 4 ) 2 S O 4 → F e S O 4 . ( N H 4 ) 2 S O 4 . 6 H 2 O + H 2 O
Cho độ tan của muối Mohr ở 2 0 o C là 26,9 g/100 g H 2 O và ở 8 0 o C là 73,0 g/100g H 2 O . Tính khối lượng của muối Iron(II) sulfate ngậm 7 nước cần thiết để tạo thành dung dịch muối Mohr bão hòa 8 0 o C , sau khi làm nguội dung dịch này xuống 2 0 o C để thu được 100 gam muối Mohr tinh thể và dung dịch bão hòa. Giả thiết trong quá trình kết tinh nước bay hơi không đáng kể.
213,2 gam.
132,1 gam.
321,1 gam.
112,3 gam.
Khi chuẩn độ 100,0 mL dung dịch NaOH 0,1 M (dung dịch A) bằng dung dịch HCl 1,0 M, thể tích dung dịch HCl cần thêm vào để pH của dung dịch A bằng 12 là
10,0 mL.
9,52 mL.
8,91 mL.
10,5 mL.
Thêm hexane (một hydrocarbon trong phân tử có 6 nguyên tử carbon) vào dung dịch iodine trong nước, lắc đều rồi để yên. Sau đó thu lấy lớp hữu cơ, làm bay hơi dung môi để thu lấy iodine. Phương pháp nào đã được sử dụng để thu lấy iodine từ dung dịch iodine trong nước trong quy trình được mô tả ở trên?
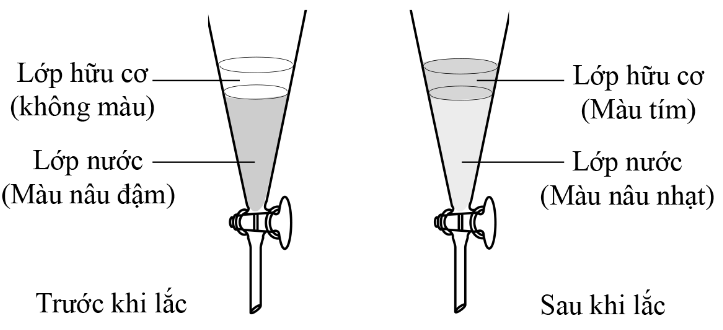
Phương pháp chưng cất.
Phương pháp chiết rắn – lỏng.
Phương pháp chiết lỏng – lỏng.
Phương pháp kết tinh.
Formaldehyde có công thức là HCHO được dùng để sản xuất vật liệu nhựa, keo dán, sơn, chất nổ, bảo quản mẫu sinh vật, … Nhận định đúng về formaldehyde là
HCHO có tên thông thường là aldehyde acetic.
Ở điều kiện thường, formaldehyde tan vô hạn trong nước.
Không thể dùng thuốc thử Tollens để phân biệt formaldehyde với acetone.
HCHO không bị oxi hóa bởi copper(II) hydroxide trong môi trường kiềm.
Hợp chất hữu cơ X có công thức cấu tạo như sau:
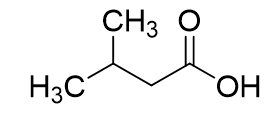
Phát biểu nào sau đây là đúng?
X có công thức phân tử là C 5 H 1 0 O 2 .
Phân tử X có chứa nhóm chức −OH.
X là hợp chất hữu cơ tạp chức.
Công thức đơn giản nhất của X là C 5 H 5 O .
Cho hai chất hữu cơ mạch hở E, F có cùng công thức đơn giản nhất là C 3 H 4 O 2 . Các chất E, F, X, Z tham gia phản ứng theo đúng tỉ lệ mol như sơ đồ dưới đây:
(1) E + NaOH X + Y (2) F + NaOH Z + T
(3) X + HCl J + NaCl (4) Z + HCl G + NaCl
Biết: X, Y, Z, T, J, G là các chất hữu cơ, trong đó T đa chức; M T > 8 8 và M E < M F < 1 4 6 . Cho các phát biểu sau:
(a) Chất J có nhiều trong nọc độc con kiến.
(b) Từ Y có thể điều chế trực tiếp được acetic acid.
(c) Ở nhiệt độ thường, T tác dụng với C u ( O H ) 2 tạo dung dịch xanh lam.
(d) E và F đều tạo kết tủa khi cho tác dụng với A g N O 3 trong dung dịch N H 3 .
(e) Nung nóng chất rắn Z với hỗn hợp vôi tôi xút thu được khí ethylene.
Số phát biểu đúng là
5.
4.
2.
3.
Phân tích nguyên tố hợp chất hữu cơ đơn chức E cho kết quả phần trăm khối lượng C, H và O lần lượt là 54,55%; 9,09% và 36,36%. Phổ hồng ngoại IR của E có dạng như sau:
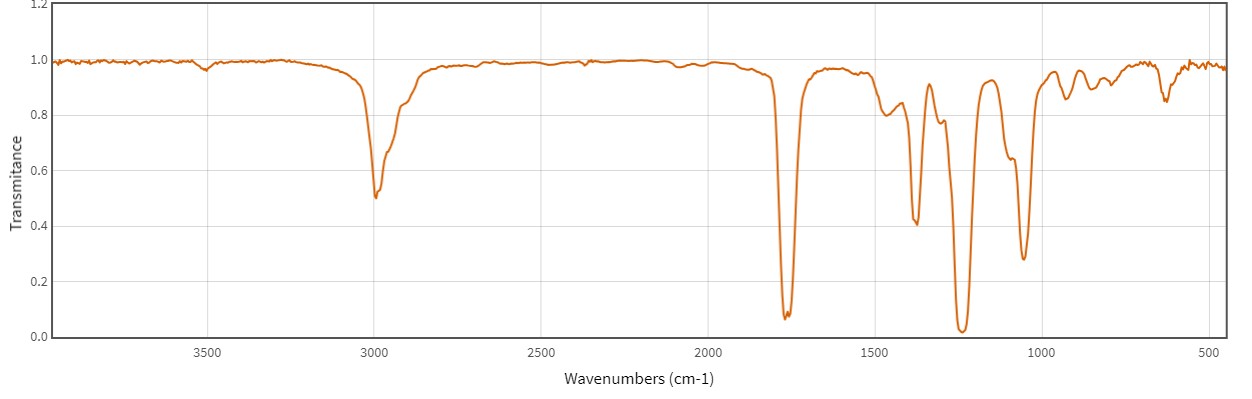
Thủy phân hoàn toàn E trong dung dịch NaOH, thu được muối của carboxylic acid X và chất Y. Đốt cháy Y với cùng số mol E thì số mol CO2 của Y bằng một nửa của E.
Cho các phát biểu sau:
(a). Nhiệt độ sôi của E, X, Y được xếp theo thứ tự tăng dần là Y, E, X.
(b). Từ X có thể điều chế trực tiếp ra Y.
(c). Y có vai trò chính trong nước rửa tay sát khuẩn thông thường.
(d).Có thể tách E ra khỏi hỗn hợp E, X, Y bằng phương pháp chiết.
Số phát biểu đúng là (nhập đáp án vào ô trống)?
Cho các phát biểu sau: (a). Nhiệt độ sôi của E, X, Y được xếp theo thứ tự tăng dần là Y, E, X. (b). Từ X có thể điều chế trực tiếp ra Y. (c). Y có vai trò chính trong nước rửa tay sát khuẩn thông thường. (d).Có thể tách E ra khỏi hỗn hợp E, X, Y bằng phương pháp chiết. Số phát biểu đúng là (nhập đáp án vào ô trống)?
Cho các polymer sau: (1) tơ tằm; (2) sợi bông; (3) tơ visco; (4) tơ capron; (5) sợi đay. Loại tơ có nguồn gốc cellulose là
(2), (3), (5).
(1), (4), (5).
(1), (2), (3).
(3), (4), (5).
Amine tồn tại ở trạng thái lỏng trong điều kiện thường là
aniline.
ethylamine.
methylamine.
dimethylamine.
Điện phân là một quá trình oxi hóa – khử xảy ra tại các điện cực khi có dòng điện một chiều với hiệu điện thế đủ lớn đi qua chất điện li nóng chảy hoặc dung dịch chất điện li.
Phương trình hóa học của phản ứng điện phân dung dịch NaCl bão hòa trong bể điện phân có màng ngăn như sau:
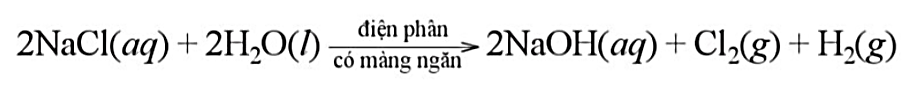
Dung dịch thu được sau quá trình điện phân có thành phần chính là NaOH nhưng còn lẫn NaCl. Cô đặc dung dịch, NaCl tan ít hơn so với NaOH nên kết tinh trước và được tách ra khỏi dung dịch. Sau đó, tiếp tục cô cạn dung dịch NaOH và làm lạnh để tách được NaOH rắn.
Điện phân dung dịch sodium chloride bão hòa trong bể điện phân có màng ngăn xốp là công đoạn chính của phương pháp chlorine – kiềm. Các sản phẩm của công nghiệp chlorine – kiềm có nhiều ứng dụng:
+ Sodium hydroxide: Được dùng trong chế biến dầu mỏ, sản xuất nhôm, giấy, xà phòng và nhiều hóa chất khác.
+ Chlorine: Được dùng để sản xuất chất tẩy trắng và sát trùng; sản xuất hydrochloric acid; potassium chlorate …
+ Hydrogen: Được dùng để sản xuất hydrochloric acid, ammonia …
Khi điện phân dung dịch NaCl có màng ngăn, các chất được tạo ra ở anode (cực dương) và cathode (cực âm) lần lượt là
Cl2 và NaOH, H2.
Na và Cl2.
Cl2 và Na.
NaOH và H2.
Điện phân là một quá trình oxi hóa – khử xảy ra tại các điện cực khi có dòng điện một chiều với hiệu điện thế đủ lớn đi qua chất điện li nóng chảy hoặc dung dịch chất điện li.
Phương trình hóa học của phản ứng điện phân dung dịch NaCl bão hòa trong bể điện phân có màng ngăn như sau:
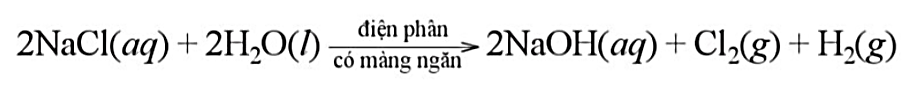
Dung dịch thu được sau quá trình điện phân có thành phần chính là NaOH nhưng còn lẫn NaCl. Cô đặc dung dịch, NaCl tan ít hơn so với NaOH nên kết tinh trước và được tách ra khỏi dung dịch. Sau đó, tiếp tục cô cạn dung dịch NaOH và làm lạnh để tách được NaOH rắn.
Điện phân dung dịch sodium chloride bão hòa trong bể điện phân có màng ngăn xốp là công đoạn chính của phương pháp chlorine – kiềm. Các sản phẩm của công nghiệp chlorine – kiềm có nhiều ứng dụng:
+ Sodium hydroxide: Được dùng trong chế biến dầu mỏ, sản xuất nhôm, giấy, xà phòng và nhiều hóa chất khác.
+ Chlorine: Được dùng để sản xuất chất tẩy trắng và sát trùng; sản xuất hydrochloric acid; potassium chlorate …
+ Hydrogen: Được dùng để sản xuất hydrochloric acid, ammonia …
Điện phân dung dịch NaCl có màng ngăn với cường độ dòng điện 10A trong 2 giờ. Giả thiết chỉ có phản ứng điện phân dung dịch NaCl, bỏ qua lượng nước bay hơi. Cho biết các công thức: Q = n.F = I.t, trong đó: Q là điện lượng (C), n là số mol electron đi qua dây dẫn, I là cường độ dòng điện (A), t là thời gian (giây), F là hằng số Faraday ( 9 6 5 0 0 C m o l − 1 ) . Khối lượng dung dịch giảm sau khi điện phân là
27,229 gam.
0,746 gam.
26,483 gam.
29,722 gam.
Điện phân là một quá trình oxi hóa – khử xảy ra tại các điện cực khi có dòng điện một chiều với hiệu điện thế đủ lớn đi qua chất điện li nóng chảy hoặc dung dịch chất điện li.
Phương trình hóa học của phản ứng điện phân dung dịch NaCl bão hòa trong bể điện phân có màng ngăn như sau:
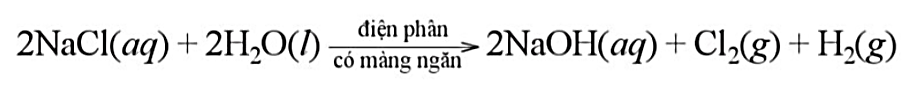
Dung dịch thu được sau quá trình điện phân có thành phần chính là NaOH nhưng còn lẫn NaCl. Cô đặc dung dịch, NaCl tan ít hơn so với NaOH nên kết tinh trước và được tách ra khỏi dung dịch. Sau đó, tiếp tục cô cạn dung dịch NaOH và làm lạnh để tách được NaOH rắn.
Điện phân dung dịch sodium chloride bão hòa trong bể điện phân có màng ngăn xốp là công đoạn chính của phương pháp chlorine – kiềm. Các sản phẩm của công nghiệp chlorine – kiềm có nhiều ứng dụng:
+ Sodium hydroxide: Được dùng trong chế biến dầu mỏ, sản xuất nhôm, giấy, xà phòng và nhiều hóa chất khác.
+ Chlorine: Được dùng để sản xuất chất tẩy trắng và sát trùng; sản xuất hydrochloric acid; potassium chlorate …
+ Hydrogen: Được dùng để sản xuất hydrochloric acid, ammonia …
Tại nhà máy giấy Bãi Bằng có xưởng sản xuất chlorine – kiềm với công suất lớn nhất trong cả nước. Kiềm được dùng cho việc nấu bột giấy, chlorine dùng cho việc tẩy trắng bột giấy. Nước muối đi vào thùng điện phân có hàm lượng 316 g/lít. Dung dịch thu được sau điện phân có chứa sodium hydroxide với hàm lượng 100 g/lít. Giả sử muối ăn là tinh khiết, thể tích dung dịch điện phân không thay đổi. Hiệu suất chuyển hoá muối trong thùng điện phân gần nhất với giá trị nào sau đây?
46,5%.
47%.
60%.
55%.








