Bộ 10 Đề thi Đánh giá năng lực Bộ Quốc phòng phần Hoá học (có đáp án) - Đề số 5
25 câu hỏi
Phương trình hoá học thuỷ phân 2-bromo-2-methylpropane trong NaOH là:
(CH3)3CBr + NaOH → (CH3)3COH + NaBr
Phản ứng trên diễn ra theo 2 giai đoạn được mô tả như sau:
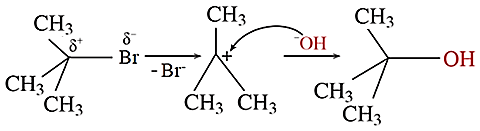
Nhận định nào sau đây đúng?
Phản ứng thuỷ phân 2-bromo-2-methylpropane là phản ứng tách hydrogen halide.
Trong giai đoạn (1) do độ âm điện C lớn hơn Br nên liên kết phân cực về phía Br.
Trong giai đoạn (2) có sự hình thành liên kết σ.
Sản phẩm thu được sau phản ứng thủy phân là alcohol bậc IV.
Cho các phát biểu sau:
(1) Để làm mềm nước cứng tạm thời có thể dùng dung dịch Ca(OH)2 hoặc NaOH.
(2) Nhúng thanh Cu trong dung dịch Fe2(SO4)3 có nhỏ vài giọt dung dịch H2SO4 có xuất hiện ăn mòn điện hóa.
(3) Các kim loại nhóm IIA có nhiệt độ sôi, nhiệt độ nóng chảy biến đổi không theo quy luật nhất định.
(4) Các kim loại đều có bán kính nhỏ hơn các phi kim thuộc cùng một chu kì.
(5) Khử zinc oxide ở nhiệt độ cao bằng than cốc thu được zinc ở trạng thái khí.
(6) Dùng dung dịch Fe2(SO4)3 dư có thể tách Ag ra khỏi hỗn hợp Ag và Cu.
Có bao nhiêu phát biểu đúng?
3.
4.
5.
6.
Alanine, ký hiệu là Ala là một amino acid được sử dụng trong quá trình sinh tổng hợp protein. Trong dung dịch ở pH khác nhau, alanine sẽ tồn tại ở các dạng như dưới đây:
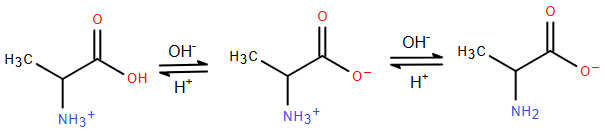
Ở pH = 6 alanine tồn tại chủ yếu ở dạng ion lưỡng cực có tổng điện tích bằng không. Khi đặt trong điện trường, alanine hầu như không di chuyển. Nhận định nào sau đây về alanine là không đúng?
Alanine là một α-amino acid.
Trong môi trường kiềm, dạng tồn tại của alanine là dạng anion.
Alanine có tính lưỡng tính.
Ở pH < 6, alanine nhận proton trở thành anion, khi đặt trong điện trường di chuyển về cực dương.
Phát biểu nào dưới đây là sai về quá trình sản xuất aluminium (Al) trong công nghiệp?
Điện phân nóng chảy Al2O3 với cryolite (Na3AlF6) làm xúc tác thu được Al ở cathode dưới dạng nóng chảy.
Trong quá trình điện phân phải hạ thấp dần các điện cực anode vào thùng điện phân, do khí O2 thoát ra đốt cháy dần điện cực.
Al có thể được tái chế nhiều lần do các tính chất vốn có của nó bị biến đổi, nên chủ yếu sử dụng trong xây dựng.
Vai trò cryolite để tiết kiệm năng lượng, tạo chất lỏng có tính dẫn điện tốt và nổi lên trên Al lỏng để ngăn cách Al lỏng với không khí.
Kết quả thí nghiệm của các chất X, Y, Z với các thuốc thử được ghi ở bảng sau:
| Chất | Thuốc thử | Hiện tượng |
| X | Quỳ tím | Quỳ tím chuyển màu hồng |
| Y | Dung dịch AgNO3 trong NH3 | Tạo kết tủa Ag |
| Z | Nước bromine | Tạo kết tủa trắng |
Các chất X, Y, Z lần lượt là
ethyl formate, glutamic acid, aniline.
aniline, ethyl formate, glutamic acid.
glutamic acid, ethyl formate, aniline.
glutamic acid, aniline, ethyl formate.
Amine X có phân tử khối nhỏ hơn 80. Trong phân tử X, nitrogen chiếm 19,18% về khối lượng. Cho X tác dụng với nitrous acid (HNO2) ở nhiệt độ thường thu được alcohol và giải phóng khí. Số công thức cấu tạo thỏa mãn X là
4.
8.
3.
2.
Cũng giống như nam châm, mỗi nguyên tử/ ion cũng có thể có từ tính (bị nam châm hút). Nếu nguyên tử/ ion có electron độc thân thì nó có từ tính và được gọi là chất thuận từ. Ngược lại, nguyên tử/ ion nếu không có electron độc thân thì được gọi là chất nghịch từ. Nguyên tử/ ion nào sau đây nghịch từ?
Cu.
Cu+.
Na.
Al.
Cho phản ứng cracking sau:
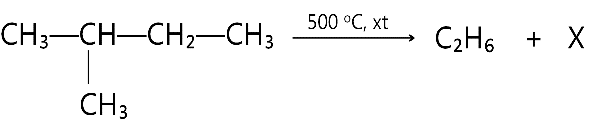
Công thức cấu tạo thu gọn của X là
CH3CH2CH3.
CH3CH=CH2.
CH3CH=CHCH3.
CH3CH2CH2CH3.
Enthalpy tạo thành của một chất là nhiệt kèm theo phản ứng tạo thành 1 mol chất đó từ các đơn chất bền nhất. Biết nhiệt tạo thành chuẩn tính theo kJ/mol của C 2 H 5 O H ( l ) , C O 2 ( g ) và H 2 O ( l ) lần lượt là −267, −393,5 và −285,8. Giả thiết, cồn là C 2 H 5 O H nguyên chất và có 40% nhiệt lượng thất thoát ra môi trường. Số gam cồn cần đốt cháy để đun 100 gam nước từ 2 5 o C đến 1 0 0 o C (biết nhiệt dung của nước là 4,2 J/g.K) là
3,5 gam.
2,7 gam.
5,4 gam.
1,75 gam.
Trong phản ứng tổng hợp ammonia:
N2(g) + 3H2(g) ⇌ x t , t o , p 2NH3(g) Δ r H 2 9 8 o = − 92 kJ
Để tăng hiệu suất phản ứng tổng hợp phải
giảm nhiệt độ và áp suất.
tăng nhiệt độ và áp suất.
tăng nhiệt độ và giảm áp suất.
giảm nhiệt độ vừa phải và tăng áp suất.
Cho các thí nghiệm sau:
(1) Một điện cực nhôm và một điện cực đồng cùng nhúng vào nước cất.
(2) Một điện cực nhôm và một điện cực đồng, tiếp xúc với nhau cùng nhúng vào dung dịch nước muối.
(3) Hai điện cực làm bằng nhựa nhúng vào dầu hỏa.
(4) Hai điện cực làm bằng đồng cùng nhúng vào dung dịch nước vôi trong.
Thí nghiệm có thể tạo thành một pin điện hóa là
(2).
(2) và (3).
(4).
(1) và (4).
Phát biểu nào sau đây không đúng về đơn chất halogen?
Khí chlorine ẩm và nước chlorine đều có tính tẩy màu.
Tính oxi hoá của đơn chất halogen giảm dần từ F 2 đến I 2 .
Trong tự nhiên không tồn tại đơn chất halogen.
Fluorine có tính oxi hoá mạnh hơn chlorine, oxi hoá C l − trong dung dịch NaCl thành C l 2 .
Tiến hành các thí nghiệm sau:
(a) Cho kim loại Cu dư vào dung dịch F e ( N O 3 ) 3 .
(b) Sục khí C O 2 dư vào dung dịch N a O H .
(c) Cho N a 2 C O 3 vào dung dịch C a ( H C O 3 ) 2 (tỉ lệ mol 1:1).
(d) Cho bột F e dư vào dung dịch F e C l 3 .
(e) Cho hỗn hợp B a O và A l 2 O 3 (tỉ lệ mol 1:1) vào nước dư.
(g) Cho hỗn hợp F e 2 O 3 và C u (tỉ lệ mol 1:1) vào dung dịch H C l dư.
Sau khi các phản ứng xảy ra hoàn toàn, số thí nghiệm thu được dung dịch chứa một muối là
2.
4.
5.
3.
Cho 25,6 gam tinh thể muối ngậm nước có dạng M g ( N O 3 ) 2 . n H 2 O hòa tan vào trong nước thu được dung dịch muối M g ( N O 3 ) 2 . Cho tiếp 200mL dung dịch NaOH 1M vào dung dịch trên thu được kết tủa trắng. Biết rằng phản ứng xảy ra vừa đủ. Giá trị của n là
4.
6.
7.
10.
Cần dùng 22,5 mL dung dịch K M n O 4 0,04 M để phản ứng vừa đủ với 20 mL dung dịch A gồm F e 2 + (hay [ F e ( O H 2 ) 6 ] 2 + ), H + và S O 4 2 − . Nồng độ mol của F e 2 + trong dung dịch A là
0,225M.
0,45M.
0,045M.
0,09M.
Trong công nghiệp, người ta tách tinh dầu quả hồi bằng phương pháp chưng cất lôi cuốn hơi nước. Anethole là thành phần chính trong tinh dầu quả hồi (chiếm khoảng 85% khối lượng tinh dầu), có mùi thơm nhẹ, là chất lỏng, không tan trong nước ở điều kiện thường, là một ether phân tử có vòng benzene. Một trong các ứng dụng của anethole là làm tiền chất để sản xuất thuốc chống cúm Tamiflu. Công thức cấu tạo phân tử của anethole là p-CH3OC6H4CH=CHCH3. Phát biểu nào sau đây là không đúng về anethole?
Oxi hoá anethole bằng dung dịch KMnO4/acid H2SO4, đun nóng thu được hỗn hợp 2 acid.
Có thể tách anethole từ hỗn hợp với nước bằng phương pháp chiết.
Anethole không tạo được liên kết hydrogen với nước.
Anethole là chất lỏng nặng hơn nước, không tác dụng được với nước bromine.
Lactic acid có trong sữa chua, dưa chua,… Công thức cấu tạo của lactic acid là C H 3 C H ( O H ) C O O H . Phát biểu đúng là
Lactic acid là hợp chất đa chức.
Dung dịch lactic acid có pH > 7.
Giữa hai phân tử lactic acid có phản ứng tạo ester và nước.
Lactic acid phản ứng với NaOH theo tỉ lệ 1 : 2.
Chanh là một loài thực vật cho quả nhỏ, thuộc chi Cam chanh (Citrus), khi chín có màu xanh hoặc vàng, thịt quả có vị chua. Quả chanh được sử dụng làm thực phẩm trên khắp thế giới - chủ yếu dùng nước ép của nó, thế nhưng phần cơm (các múi của chanh) và vỏ cũng được sử dụng, chủ yếu là trong nấu ăn và nướng bánh. Nước ép chanh chứa khoảng 5% (khoảng 0,3 mol/lít) citric acid, điều này giúp chanh có vị chua, và độ pH của chanh từ 2 - 3. Citric acid có công thức cấu tạo là
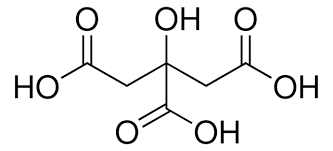
Trong các phát biểu sau về citric acid, phát biểu nào là đúng?
Công thức phân tử của citric acid là C 6 H 6 O 7 .
Citric acid thuộc loại hợp chất đa chức.
1 mol citric acid tác dụng được với Na sinh ra 2 mol H 2 .
Citric acid tác dụng với NaOH theo tỉ lệ mol 1 : 4.
Adrenaline là một trong những loại chất kích thích (doping) bị cấm sử dụng trong thể thao có công thức hóa học như hình dưới:
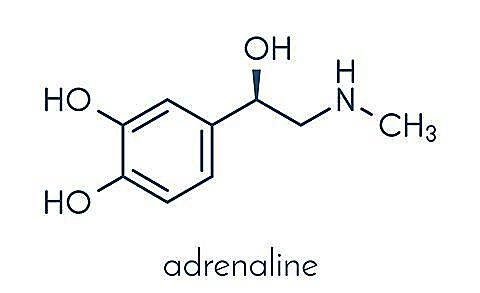
Cho các phát biểu sau về adrenaline:
(a). Adrenaline có khả năng tham gia phản ứng với NaOH theo tỉ lệ mol 1 : 4.
(b). Adrenaline có khả năng làm mất màu nước bromine.
(c). Adrenaline tham gia phản ứng với hydrogen theo tỉ lệ mol 1:1.
(d). Công thức phân tử của adrenaline là C 9 H 1 1 O 3 N .
Số phát biểu đúng là
3.
4.
1.
2.
Hợp chất hữu cơ X gồm 3 nguyên tố C, H, O. Kết quả phân tích nguyên tố của hợp chất hữu cơ X có m C : m H : m O = 4 2 : 7 : 1 6 . Phân tử khối của X gấp 4,0625 lần phân tử khối của oxygen. X có mạch không phân nhánh và phổ hồng ngoại của X như sau
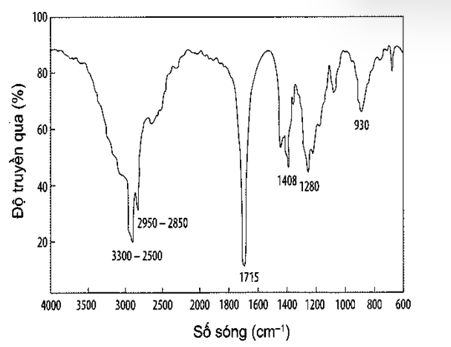
Biết:
| Loại hợp chất | Liên kết | Số sóng (cm-1) |
| Alcohol | O−H | 3600 − 3300 |
| Aldehyde | C=O | 1740 − 1720 |
| C−H | 2900 − 2700 | |
| Carboxylic acid | C=O | 1725 − 1700 |
| O−H | 3300 − 2500 | |
| Ester | C=O | 1750 − 1735 |
| C−O | 1300 − 1000 | |
| Ketone | C=O | 1725 − 1700 |
| Amine | N−H | 3500 − 3300 |
Cho các phát biểu sau
(a) X có 6 nguyên tử carbon.
(b) X tác dụng được với N a H C O 3 .
(c) X làm quỳ tím hóa đỏ.
(d) X có số nguyên tử hydrogen gấp 7 lần số nguyên tử oxygen.
(e) X thuộc loại hợp chất ester.
(g) Tỉ lệ số nguyên tử C và H trong X là 1 : 2.
Số phát biểu đúng là (nhập đáp án vào ô trống)?
4
Khi nhiệt độ tăng lên 10 oC, tốc độ của một phản ứng hóa học tăng lên 3 lần. Hỏi tốc độ của phản ứng đó tăng lên bao nhiêu lần khi nâng nhiệt độ lên từ 30 oC đến 50 oC?
3 lần.
6 lần.
9 lần.
27 lần.
Polymer nào sau đây được điều chế bằng phản ứng trùng ngưng?
Poly(methyl methacrylate).
Polyethylene.
Poly(hexamethylene adipamide).
Poly(vinyl chloride).
Tiến hành phản ứng tráng bạc của glucose với thuốc thử Tollens, người ta tiến hành các bước sau đây:
Bước 1: Rửa sạch ống nghiệm, bằng cách nhỏ vào mấy giọt NaOH, đun nóng nhẹ, tráng đều, sau đó đổ đi và tráng lại ống nghiệm bằng nước cất.
Bước 2: Cho vào ống nghiệm trên khoảng 2 mL dung dịch A g N O 3 1% và thêm từ từ dung dịch N H 3 , trong ống nghiệm xuất hiện kết tủa nâu xám của silver hydroxide, nhỏ tiếp vài giọt dung dịch N H 3 đến khi kết tủa tan hết. Dung dịch thu được là thuốc thử Tollens.
Bước 3: Thêm tiếp vào ống nghiệm khoảng 2 mL dung dịch glucose 2%.
Bước 4: Lắc đều ống nghiệm, đun cách thủy (trong cốc nước nóng) vài phút ở 60 – 70°C
Thí nghiệm trên chứng minh:
Glucose có các nhóm – OH liền kề.
Glucose có tính oxi hóa.
Glucose có nhóm chức aldehyde.
Glucose là một acid mạnh.
Tiến hành phản ứng tráng bạc của glucose với thuốc thử Tollens, người ta tiến hành các bước sau đây:
Bước 1: Rửa sạch ống nghiệm, bằng cách nhỏ vào mấy giọt NaOH, đun nóng nhẹ, tráng đều, sau đó đổ đi và tráng lại ống nghiệm bằng nước cất.
Bước 2: Cho vào ống nghiệm trên khoảng 2 mL dung dịch A g N O 3 1% và thêm từ từ dung dịch N H 3 , trong ống nghiệm xuất hiện kết tủa nâu xám của silver hydroxide, nhỏ tiếp vài giọt dung dịch N H 3 đến khi kết tủa tan hết. Dung dịch thu được là thuốc thử Tollens.
Bước 3: Thêm tiếp vào ống nghiệm khoảng 2 mL dung dịch glucose 2%.
Bước 4: Lắc đều ống nghiệm, đun cách thủy (trong cốc nước nóng) vài phút ở 60 – 70°C
Cho các phát biểu sau:
(a) Sau bước 4 quan sát thấy thành ống nghiệm sáng bóng như gương.
(b) Ở bước 4 xảy ra phản ứng oxi hóa – khử trong đó glucose là chất bị khử.
(c) Sản phẩm hữu cơ thu được trong dung dịch sau bước 4 là ammonium gluconate.
(d) Có thể thay dung dịch N H 3 bằng dung dịch NaOH.
Số phát biểu đúng là
1.
2.
3.
4.
Tiến hành phản ứng tráng bạc của glucose với thuốc thử Tollens, người ta tiến hành các bước sau đây:
Bước 1: Rửa sạch ống nghiệm, bằng cách nhỏ vào mấy giọt NaOH, đun nóng nhẹ, tráng đều, sau đó đổ đi và tráng lại ống nghiệm bằng nước cất.
Bước 2: Cho vào ống nghiệm trên khoảng 2 mL dung dịch A g N O 3 1% và thêm từ từ dung dịch N H 3 , trong ống nghiệm xuất hiện kết tủa nâu xám của silver hydroxide, nhỏ tiếp vài giọt dung dịch N H 3 đến khi kết tủa tan hết. Dung dịch thu được là thuốc thử Tollens.
Bước 3: Thêm tiếp vào ống nghiệm khoảng 2 mL dung dịch glucose 2%.
Bước 4: Lắc đều ống nghiệm, đun cách thủy (trong cốc nước nóng) vài phút ở 60 – 70°C
Để tráng một số lượng gương soi có diện tích bề mặt 0 , 3 5 m ² với độ dày 0,1 μm người ta đun nóng dung dịch chứa 26,77 gam glucose với một lượng dung dịch silver nitrate trong ammonia. Biết khối lượng riêng của silver là 1 0 , 4 9 g / c m ³ , hiệu suất phản ứng tráng gương là 80% (tính theo glucose). Số lượng gương soi tối đa sản xuất được khoảng
80.
70.
85.
90.








