Bộ 10 Đề thi Đánh giá năng lực Bộ Quốc phòng phần Hoá học (có đáp án) - Đề số 6
25 câu hỏi
Polymer X được dùng sản xuất một loại chất dẻo an toàn thực phẩm trong công nghệ chế tạo chai lọ đựng nước, bao bì đựng thực phẩm. Phân tích thành phần nguyên tố của monomer dùng điều chế X thu được kết quả: %C = 85,71%; %H = 14,29% (về khối lượng). Từ phổ khối lượng, xác định được phân tử khối của monomer bằng 42. Tên của polymer X là
polymethylene.
polyethylene.
polybuta-1,3-diene.
polypropylene.
Cho biết sức điện động chuẩn của các pin sau:
Pin điện hoá | X-Y | M-Y | M-Z |
Sức điện động chuẩn (V) | 0,20 | 0,60 | 0,30 |
Sự sắp xếp nào sau đây đúng với tính khử của các kim loại X, Y, Z, M?
Y < X < Z < M.
M < Z < Y < X.
X < Y < M < Z.
X < Y < Z < M.
Khi có mặt xúc tác FeBr3, benzene tác dụng với bromine theo phản ứng:
C6H6 + Br2 → F e B r 3 , t ° C6H5Br + HBr
Cơ chế của phản ứng trên như sau:
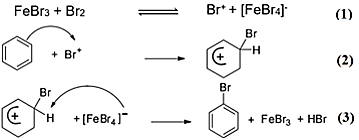
Nhận định nào sau đây không đúng?
Phản ứng giữa benzene với bromine thuộc loại phản ứng thế.
Bước 1 xảy ra sự phân cắt dị li phân tử Br2 (sự phân cắt mà cặp electron dùng chung chỉ thuộc về 1 nguyên tử).
Bước 2 xảy ra quá trình tương tác giữa benzene với tác nhân nucleophile.
Bước 3 xảy ra quá trình tách proton (H+) để tạo ra sản phẩm.
Cho bảng số liệu sau:
| Chất | Nước (H2O) | Hydrogen sulfide (H2S) |
| Nhiệt độ sôi ( o C ) ở 1 atm | 100,0 | -60,7 |
Phát biểu nào sau đây sai?
Liên kết O – H trong phân tử H2O kém phân cực hơn liên kết S – H trong phân tử H2S.
Số liên kết trong phân tử H2O bằng số liên kết trong phân tử H2S.
Trong phân tử H2O và phân tử H2S chỉ có các liên kết cộng hóa trị.
Do có liên kết hydrogen giữa các phân tử nên nước có nhiệt độ sôi cao hơn hydrogen sulfide.
Trong phân tử phức chất K 3 [ F e ( C N ) 6 ] , Fe3+ được gọi là
phối tử.
base.
chất khử.
nguyên tử trung tâm.
Tiến hành điều chế ethyl acetate theo các bước như hình sau:
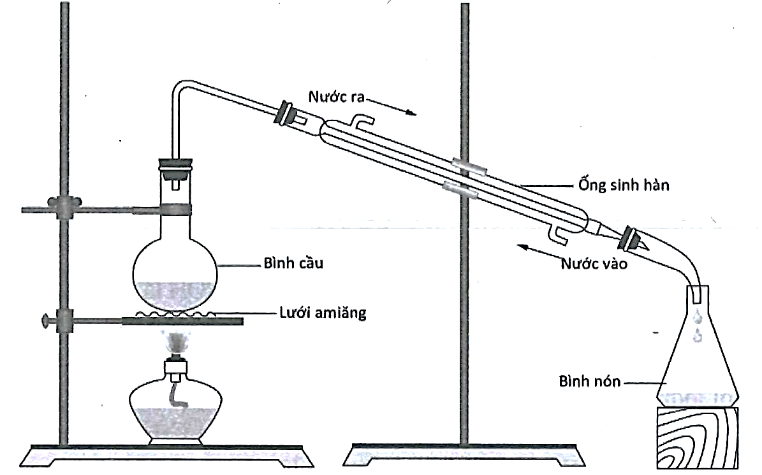
Bước 1: Cho 10 mL C2H5OH (D = 0,78 g/cm3) cùng với 10 mL CH3COOH (D = 1,05 g/cm3), vài giọt dung dịch H2SO4 đặc và lắc đều bình cầu.
Bước 2: Đun nóng bình cầu đến 70oC trong khoảng từ 5 đến 6 phút.
Bước 3: Các chất thu được ở bình nón được thêm tiếp vào 2 mL dung dịch NaCl bão hòa.
Phát biểu nào dưới đây là đúng?
Sau bước 1, trong bình cầu có phản ứng ester hóa sau: CH3COOH + HOCH2CH3 ⇌ H 2 S O 4 d , t o CH3COOCH2CH3 + H2O
Ở bước 3, dung dịch NaCl bão hòa có vai trò làm tăng hiệu suất phản ứng ester hóa.
Sau bước 2, các chất C2H5OH và CH3COOH vẫn còn trong bình cầu.
Đun nóng 6 gam acetic acid với 6 gam ethyl alcohol có H2SO4 đặc làm xúc tác. Khối lượng ester tạo thành khi hiệu suất phản ứng 80% là 8,8 gam.
Xét hai phân tử NH3 và CH4. Phát biểu nào sau đây sai?
Trong cả hai phân tử, nguyên tử trung tâm lai hóa sp3
Góc liên kết trong phân tử NH3 lớn hơn trong CH4.
Trong các phân tử này chỉ có liên kết đơn.
Phân tử NH3 phân cực, phân tử CH4 không phân cực.
Cho phản ứng:
H2 (g) + I2(g) ⇌ 2HI (g)
Ở nhiệt độ 430°C, hằng số cân bằng KCcủa phản ứng trên bằng 53,96. Đun nóng một bình kín dung tích không đổi 10 lít chứa 4,0 gam H2và 406,4 gam I2. Khi hệ phản ứng đạt trạng thái cân bằng ở 430°C, nồng độ của HI gần nhất với
0,275M.
0,320M.
0,151M.
0,225M.
Một bình gas (khí hóa lỏng) chứa hỗn hợp propane và butane với tỉ lệ mol 1:2. Xác định nhiệt lượng tỏa ra khi đốt cháy hoàn toàn 12 kg khí gas trên ở điều kiện chuẩn.
Cho biết các phản ứng:
C 3 H 8 ( g ) + 5 O 2 ( g ) → 3 C O 2 ( g ) + 4 H 2 O ( l ) Δ r H 2 9 8 o = − 2 2 2 0 k J
C 4 H 1 0 ( g ) + O 2 ( g ) → 4 C O 2 ( g ) + 5 H 2 O ( l ) Δ r H 2 9 8 o = − 2 8 7 4 k J
Trung bình mỗi ngày, một hộ gia đình cần đốt gas để cung cấp 10 000 kJ nhiệt (hiệu suất hấp thụ nhiệt là 80%). Sau bao nhiêu ngày hộ gia đình trên sẽ sử dụng hết bình gas 12 kg?
48 ngày.
75 ngày.
38 ngày.
47 ngày.
Cho phản ứng: 2 K C l O 3 (s) → M n O 2 , t o 2KCl(s) + 3 O 2 (g). Yếu tố không ảnh hưởng đến tốc độ của phản ứng trên là
kích thước các tinh thể KClO3.
áp suất.
chất xúc tác.
nhiệt độ.
Điện phân dung dịch NaCl bão hòa (với điện cực trơ, màng ngăn xốp) đến khi nồng độ NaCl giảm đi một nửa thì dừng điện phân. Nhận xét đúng nào sau đây là đúng?
Thứ tự điện phân ở anode là H 2 O , C l − .
Dung dịch sau điện phân làm phenolphthalein chuyển màu hồng.
Ở cathode chỉ xảy ra quá trình khử ion N a + .
Số mol khí C l 2 thoát ra ở cathode bằng số mol H 2 thoát ra ở anode.
Nguyên nhân dẫn tới nhiệt độ nóng chảy, nhiệt độ sôi của các đơn chất halogen tăng từ fluorine đến iodine là do từ fluorine đến iodine là
khối lượng phân tử và tương tác van der Waals đều tăng.
tính phi kim giảm và tương tác van der Waals tăng.
khối lượng phân tử tăng và tương tác van der Waals giảm.
độ âm điện và tương tác van der Waals đều giảm.
Thực hiện các thí nghiệm sau:
(a) Đun nóng hỗn hợp bột FeO và CO .
(b) Cho Fe vào dung dịch HCl.
(c) Cho F e ( O H ) 2 vào dung dịch H N O 3 loãng, dư.
(d) Đốt Fe dư trong C l 2 .
(e) Cho F e 3 O 4 vào dung dịch H 2 S O 4 loãng, dư.
Số thí nghiệm tạo ra muối iron(III) là
1.
4.
3.
2.
Cho 4,29 gam tinh thể muối N a 2 C O 3 . n H 2 O tác dụng với 85,8 mL dung dịch
BaCl2 0,2 M thu được 2,955 gam kết tủa khan. Giá trị của n là
6.
8.
10.
12
Tiến hành thí nghiệm theo các bước sau:
Bước 1: Dùng pipette hút chính xác 5,00 mL dung dịch F e S O 4 nồng độ a mol/L cho vào bình định mức loại 50 mL. Thêm tiếp nước cất và định mức đến vạch, thu được 50 mL dung dịch Y.
Bước 2: Chuẩn độ 10,00 mL dung dịch Y trong môi trường H 2 S O 4 loãng cần vừa đủ 8,80 mL dung dịch K M n O 4 0,02M.
Giá trị của a là
0,176.
0,88.
1,76.
0,44.
Với quá trình tách natri (sodium) bằng phương pháp điện phân sodium chloride nóng chảy, phát biểu nào sau đây là đúng?
Tại anode xảy ra quá trình khử ion N a + .
Tại cathode xảy ra quá trình khử ion C l − .
Tại cathode xảy ra quá trình khử ion N a + .
Tại anode xảy ra quá trình khử ion C l − .
Sulfuric acid ( H 2 S O 4 ) là hóa chất quan trọng, được sản xuất trong công nghiệp bằng phương pháp tiếp xúc. Nhận định nào sau đây là đúng về sulfuric acid?
Sulfuric acid loãng có tính acid yếu, không làm quỳ tím đổi màu.
Sulfuric acid đặc, nóng có tính oxi hóa mạnh, phản ứng với hầu hết các kim loại (trừ Au, Pt), nhiều phi kim, nhiều hợp chất.
Sulfuric acid đặc, nguội phản ứng được với Fe, Al và Cr.
Ion H + trong sulfuric acid loãng thể hiện tính khử.
Dopamine là một hóa chất não quan trọng ảnh hưởng đến tâm trạng và cảm giác của bạn về sự hưng phấn và vui vẻ. Chính vì vậy, dopamine còn được gọi là hormone hạnh phúc.
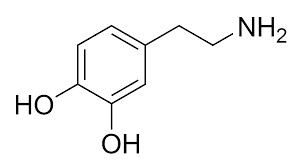
Công thức phân tử của dopamine là
C 9 H 1 3 O 2 N .
C 8 H 1 1 O 2 N .
C 8 H 4 O 2 N .
C 9 H 1 4 O 2 N .
Trong phòng thí nghiệm người ta điều chế isoamyl acetate (Y) theo sơ đồ hình vẽ:
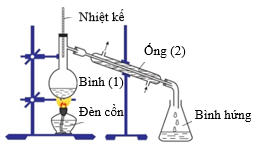
Cho các phát biểu sau:
(1) Các chất điều chế trực tiếp Y gồm C H 3 − C O O H , ( C H 3 ) 2 C H − C H 2 − O H .
(2) Nước trong ống (2) ở hình vẽ có tác dụng làm lạnh để ngưng tụ chất Y.
(3) Phản ứng trong bình (1) là phản ứng thuận nghịch.
(4) Trong bình (1) cần thêm sulfuric acid đặc nhằm hút nước và xúc tác cho phản ứng.
(5) Chất lỏng Y được sử dụng làm hương liệu trong sản xuất bánh kẹo.
(6) Có thể sử dụng giấm ăn (dung dịch C H 3 − C O O H 3 % ) cho quá trình điều chế trên.
Số phát biểu đúng là
6.
4.
3.
5.
Chất X no, đơn chức có công thức phân tử là C 5 H x O y và có phổ hồng ngoại như sau:
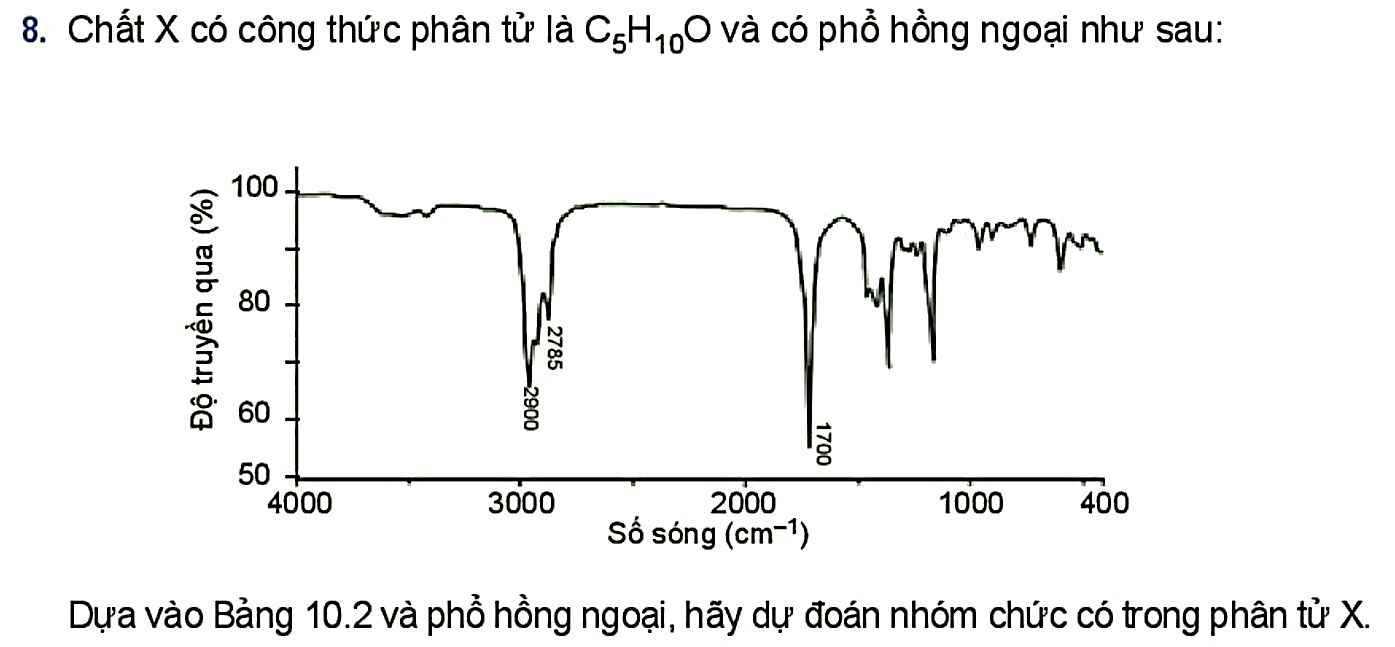
Biết:
| Loại hợp chất | Liên kết | Số sóng (cm-1) |
| Alcohol | O−H | 3600 − 3300 |
| Aldehyde | C=O | 1740 − 1720 |
| C−H | 2900 − 2700 | |
| Carboxylic acid | C=O | 1725 − 1700 |
| O−H | 3300 − 2500 | |
| Ester | C=O | 1750 − 1735 |
| C−O | 1300 − 1000 | |
| Ketone | C=O | 1725 − 1700 |
| Amine | N−H | 3500 − 3300 |
Phần trăm khối lượng nguyên tử O có trong X là h%. Giá trị của h là (nhập đáp án vào ô trống)?
18,60
Các phát biểu về tính chất của peptide:
(1). Thủy phân hoàn toàn Gly-Ala-Val thì thu được Gly, Ala và Val.
(2). Thủy phân không hoàn toàn Gly-Ala-Val có thể thu được Gly-Ala và Ala-Val.
(3). Gly-Ala-Val không phản ứng với C u ( O H ) 2 trong môi trường kiềm tạo thành dung dịch màu tím.
(4). Gly-Gly phản ứng hoàn toàn với NaOH thu được H 2 N C H 2 C O O N a .
Các phát biểu đúng là
(1), (2) và (3).
(1), (2) và (4).
(2), (3) và (4).
(1) và (3).
Tinh thể chất rắn X vị ngọt, dễ tan trong nước. X có nhiều trong các bộ phận của cây đặc biệt là quả chín. Oxi hóa chất X bằng nước bromine thu được chất hữu cơ Y. Tên gọi của X và Y lần lượt là
fructose và gluconic acid.
glucose và gluconic acid.
glucose và ammonium gluconate.
saccharose và glucose.
Hiện nay người ta dùng thiết bị breathalyzer để đo nồng độ cồn trong khí thở của người tham gia giao thông. Khi có nồng độ cồn trong khí thở sẽ xảy ra phản ứng:
C 2 H 5 O H + K 2 C r 2 O 7 + H 2 S O 4 → A g + C H 3 C O O H + C r 2 ( S O 4 ) 3 + K 2 S O 4 + H 2 O ( * ) \(?{Ag}^{+}\)
Tùy thuộc vào lượng K 2 C r 2 O 7 phản ứng, trên màn hình thiết bị sẽ xuất hiện số chỉ nồng độ cồn tương ứng. Người đi xe máy có nồng độ cồn trong khí thở sẽ bị xử phạt theo khung sau đây (trích từ Nghị định 100/ 2019/ NĐ−CP sửa đổi tại Nghị định 123/2021/NĐ−CP):
| Nồng độ cồn (mg/1L khí thở) | Mức tiền phạt (VND) | Hình phạt bổ sung (tước giấy phép lái xe) |
| 0,25 | 2 triệu - 3 triệu | 10 - 12 tháng |
| 0,25 đến 0,4 | 4 triệu - 5 triệu | 16 - 18 tháng |
| > 0,4 | 6 triệu - 8 triệu | 22 - 24 tháng |
Trong phản ứng (*) chất oxi hóa là
K 2 C r 2 O 7 .
H 2 S O 4 .
C 2 H 5 O H .
C H 3 C O O H .
Hiện nay người ta dùng thiết bị breathalyzer để đo nồng độ cồn trong khí thở của người tham gia giao thông. Khi có nồng độ cồn trong khí thở sẽ xảy ra phản ứng:
C 2 H 5 O H + K 2 C r 2 O 7 + H 2 S O 4 → A g + C H 3 C O O H + C r 2 ( S O 4 ) 3 + K 2 S O 4 + H 2 O ( * ) \(?{Ag}^{+}\)
Tùy thuộc vào lượng K 2 C r 2 O 7 phản ứng, trên màn hình thiết bị sẽ xuất hiện số chỉ nồng độ cồn tương ứng. Người đi xe máy có nồng độ cồn trong khí thở sẽ bị xử phạt theo khung sau đây (trích từ Nghị định 100/ 2019/ NĐ−CP sửa đổi tại Nghị định 123/2021/NĐ−CP):
| Nồng độ cồn (mg/1L khí thở) | Mức tiền phạt (VND) | Hình phạt bổ sung (tước giấy phép lái xe) |
| 0,25 | 2 triệu - 3 triệu | 10 - 12 tháng |
| 0,25 đến 0,4 | 4 triệu - 5 triệu | 16 - 18 tháng |
| > 0,4 | 6 triệu - 8 triệu | 22 - 24 tháng |
Sau khi cân bằng với các hệ số của các chất là số nguyên nhỏ nhất thì tổng hệ số các chất tham gia phản ứng và sản phẩm của phản ứng trên là
30.
31.
32.
33.
Hiện nay người ta dùng thiết bị breathalyzer để đo nồng độ cồn trong khí thở của người tham gia giao thông. Khi có nồng độ cồn trong khí thở sẽ xảy ra phản ứng:
C 2 H 5 O H + K 2 C r 2 O 7 + H 2 S O 4 → A g + C H 3 C O O H + C r 2 ( S O 4 ) 3 + K 2 S O 4 + H 2 O ( * ) \(?{Ag}^{+}\)
Tùy thuộc vào lượng K 2 C r 2 O 7 phản ứng, trên màn hình thiết bị sẽ xuất hiện số chỉ nồng độ cồn tương ứng. Người đi xe máy có nồng độ cồn trong khí thở sẽ bị xử phạt theo khung sau đây (trích từ Nghị định 100/ 2019/ NĐ−CP sửa đổi tại Nghị định 123/2021/NĐ−CP):
| Nồng độ cồn (mg/1L khí thở) | Mức tiền phạt (VND) | Hình phạt bổ sung (tước giấy phép lái xe) |
| 0,25 | 2 triệu - 3 triệu | 10 - 12 tháng |
| 0,25 đến 0,4 | 4 triệu - 5 triệu | 16 - 18 tháng |
| > 0,4 | 6 triệu - 8 triệu | 22 - 24 tháng |
Một mẫu khí thở của một người điều khiển xe máy tham gia giao thông có thể tích 26,25 mL được thổi vào thiết bị breathalyzer thì có 0,056 mg K 2 C r 2 O 7 phản ứng (trong môi trường H 2 S O 4 và ion Ag+ xúc tác). Người điều khiển xa máy đã vi phạm giao thông với mức
tiền phạt (6 triệu - 8 triệu), tước giấy phép lái xe (22 - 24 tháng).
tiền phạt (2 triệu - 3 triệu), tước giấy phép lái xe (10 - 12 tháng).
tiền phạt (4 triệu - 5 triệu), tước giấy phép lái xe (16 - 18 tháng).
tiền phạt (2 triệu - 3 triệu), tước giấy phép lái xe (16 - 18 tháng).








