Đề thi Đánh giá năng lực ĐHQG Hà Nội phần Hóa (có đáp án) - Đề 28
17 câu hỏi
X là ester tạo nên mùi thơm của dứa chín. Xà phòng hóa X bằng dung dịch NaOH thu được ethyl alcohol và sodium butyrate. Phát biểu nào sau đây là đúng?
Công thức cấu tạo của X là C 2 H 5 C O O C H 2 C H 2 C H 2 C H 3 .
Trong mỗi phân tử X có 6 nguyên tử carbon.
X là ester không no, đơn chức, mạch hở.
X có phản ứng với thuốc thử Tollens.
Hợp chất hữu cơ X mạch hở có công thức phân tử là C 3 H 6 O . X không có phản ứng iodoform, X không phản ứng với thuốc thử Tollens. Cho các phát biểu sau về X:
(a) Phổ MS của X xuất hiện tín hiệu có giá trị m/z lớn nhất là 58.
(b) X thuộc loại hợp chất carbonyl, phân tử có nhóm chức C=O.
(c) X là hợp chất không no.
(d) X có 2 đồng phân cấu tạo thỏa mãn.
Số phát biểu đúng là
1.
3.
2.
4.
Dung dịch C a ( O H ) 2 bão hòa ở 2 0 ° C có độ tan 0,173 gam và khối lượng riêng là 1,04 g/mL. Nồng độ mol của ion C a 2 + trong dung dịch bão hòa C a ( O H ) 2 ở 2 0 ° C có giá trị gần đúng là (Coi C a ( O H ) 2 phân li hoàn toàn cả hai nấc trong nước, kết quả lấy đến hàng phần nghìn)
1,796.
0,048.
0,024.
0,023.
Sulfuric acid là hoá chất quan trọng số một trong công nghiệp hoá học. Sulfuric acid được dùng để xuất phân bón, chất tẩy rửa, sơn, phẩm nhuộm, chế tạo acquy,… Người ta sản xuất sulfuric acid trong 3 nghiệp theo sơ đồ:
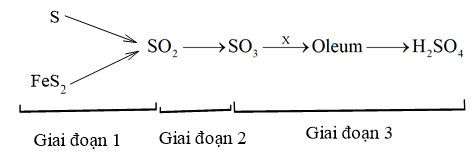
Phát biểu nào dưới đây là đúng?
Trong sơ đồ điều chế trên có 4 phản ứng oxi hoá - khử.
Giai đoạn 3 chất X là H 2 S O 4 loãng.
Theo QCVN 05:2013/BTNMT về ô nhiễm chất lượng không khí hàm lượng cho phép tối đa của S O 2 là 350 μg/m³ không khí đo trong một giờ. Nếu người ta lấy 50 lít không khí trong một giờ ở một thành phố và phân tích thấy có 0,018 mg S O 2 thì không khí ở đó không bị ô nhiễm.
Sulfuric acid loãng dùng để tạo môi trường acid trong sản xuất acquy chì.
Điện phân dung dịch NaCl bão hòa là một phương pháp thu được những sản phẩm có tính ứng dụng rất cao trong ngành công nghiệp sản xuất.
- Để điều chế chlorine với xút thì trong quá trình điện phân người ta dùng màng ngăn giữa các điện cực.
- Để điều chế nước Javel thì trong quá trình điện phân người ta không dùng màng ngăn giữa các điện cực.
Cho các phát biểu sau:
(a) Theo thời gian, cả hai cách điện phân trên nồng độ cation N a + không thay đổi.
(b) Trong quá trình điện phân, điều chế nước Javel thì số NaCl và NaClO luôn bằng nhau.
(c) Trong cả hai quá trình điện phân trên pH của dung dịch đều tăng lên.
(d) Trong cả hai quá trình điện phân trên tại anode đều xảy ra bán phản ứng khử anion Cl− (aq) thành khí chlorine.
(e) Một loại nước Javel có khối lượng riêng 1,15 g/mL được bán trên thị trường với dung tích là 1,0 lít có nồng độ % NaClO và NaCl lần lượt là: 12,96% và 15,26%. Nồng độ % của dung dịch NaCl trước khi điện phân là 25,3%. (Coi khí sinh ra không tan trong nước và hiệu suất phản ứng đạt 100%). Làm tròn kết quả đến hàng phần mười.
Số phát biểu đúng là
5.
3.
2.
4.
Ammonia là một hợp chất vô cơ có công thức phân tử N H 3 . Trong tự nhiên, ammonia sinh ra trong quá trình bài tiết và xác sinh vật thối rữa. Ammonia ( N H 3 ) nặng gần bằng nửa không khí. Sau khi nén và làm lạnh, nó biến thành chất lỏng giống như nước nhưng sôi ở nhiệt độ − 3 3 ° C . Khi bị nén xong, N H 3 dễ bay hơi. Ở điều kiện tiêu chuẩn, nó là một chất khí, không màu, có mùi khai, tan nhiều trong nước do hình thành liên kết hydrogen với phân tử nước. Trong dung dịch N H 3 (hỗn hợp N H 3 và H 2 O ) tồn tại số loại liên kết hydrogen là
1.
2.
3.
4.
Một khối đồng kim loại hình trụ đường kính 5 cm, chiều dài 30 cm cần được mạ vàng với chiều dày lớp mạ 5,0 μm. Cho biết: cường độ dòng điện đi qua bể mạ là 3,0 A; dung dịch trong bể mạ là A u ( N O 3 ) 3 ; hiệu suất điện phân là 100%; khối lượng riêng của Au bằng 19,3 g / c m ³ ; hằng số Faraday F = 96500 C/mol. Thời gian cần để mạ khối kim loại trên gần nhất với (Cho biết nguyên tử khối của các nguyên tố: N = 14; O = 16; Au = 197)
13,40 phút.
37,11 phút.
40,20 phút.
38,66 phút.
Cho mô hình tinh thể NaCl như hình dưới:
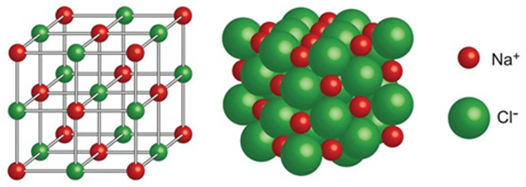
Số ion chloride ( C l − ) bao quanh gần nhất với ion sodium ( N a + ) là
3.
1.
6.
4.
Butane là một trong hai thành phần chính của khí đốt hóa lỏng. Khi đốt cháy hoàn toàn 1 mol butane tỏa ra lượng nhiệt là 2497 kJ. Để thực hiện việc đun nóng 1 gam nước tăng thêm 1 ° C cần cung cấp nhiệt lượng là 4,18 J. Tính khối lượng butane cần đốt để đưa 2 lít nước từ 2 5 ° C lên 1 0 0 ° C . Biết rằng khối lượng riêng của nước là 1 gam/mL và 60% nhiệt lượng tỏa ra khi đốt cháy butane dùng để nâng nhiệt độ của nước.
23,2 gam.
26,5 gam.
24,3 gam.
25,4 gam.
Vị tanh của cá đặc biệt là cá mè, là do các amine gây ra, trong đó có amine X. Phân tích nguyên tố đối với X thu được kết quả: %C = 61,02%; %H = 15,25%; %N = 23,73% (về khối lượng). Từ phổ khối lượng, xác định được phân tử khối của X bằng 59. Bằng các phương pháp khác, thấy phân tử X có cấu trúc đối xứng cao. Phát biểu nào sau đây là sai?
Công thức phân tử của X là C 3 H 9 N .
X là tồn tại trạng thái khí ở điều kiện thường.
Công thức cấu tạo của X là ( C H 3 ) 3 N .
Dung dịch X tác dụng với nitrous acid tạo ra N 2 .
Biết những chất lỏng có điểm chớp cháy thấp hơn 3 7 , 8 ° C là chất lỏng dễ cháy. Cho bảng số liệu về điểm chớp cháy của một số chất lỏng sau:
| Chất | Pentane | Ethanol | Formic acid | Ethylen glycol |
| Điểm chớp cháy | -49 | 13 | 50 | 111 |
Trong số các chất trên, pentane có khả năng gây cháy, nổ cao nhất.
Trong số các chất trên, ethylene glycol có khả năng gây cháy, nổ thấp nhất.
Pentane có điểm chớp cháy thấp hơn ethanol nên dễ bốc cháy hơn.
Trong số các chất trên, có một chất lỏng dễ cháy.
Trong phòng thí nghiệm trimesic acid (hay 1,3,5-benzenetricarboxylic acid) được điều chế bằng cách đun mesitylene (hay 1,3,5-trimethylbenzene) với dung dịch K M n O 4 trong môi trường H 2 S O 4 dư theo sơ đồ sau:
m e s i t y l e n e + K M n O 4 + H 2 S O 4 → t o t r i m e s i c a c i d + K 2 S O 4 + M n S O 4 + H 2 O
Nếu hệ số cân bằng của mesitylene là 1 thì tổng hệ số cân bằng của phản ứng xảy ra là bao nhiêu?
24,8
Cho các phản ứng thuận nghịch đang ở trạng thái cân bằng:
( 1 ) H 2 ( g ) + I 2 ( g ) ⇋ 2 H I ( g ) .
( 2 ) F e 2 O 3 ( s ) + 3 C O ( g ) ⇋ 2 F e ( s ) + 3 C O 2 ( g ) .
( 3 ) 2 N O 2 ( g ) ⇋ N 2 O 4 ( g ) .
Yếu tố áp suất ảnh hưởng đến chuyển dịch cân bằng của phản ứng thuận nghịch nào?
(3).
(1).
(2).
(2); (3).
Hạt cau được sử dụng để điều trị tình trạng sâu răng nhờ tính diệt khuẩn và sát trùng, giúp ngăn chặn sự phát triển của vi khuẩn có hại trong khoang miệng. Cách làm, lấy khoảng 20 đến 25 quả cau già, bổ tách lấy hạt và cho vào bình ngâm với 1 lít rượu trắng. Sau khoảng 1 tháng, khi rượu cau bắt đầu chuyển sang màu cánh gián là bạn có thể dùng được. Cách làm rượu hạt cau trên đã áp dụng phương pháp tách biệt nào sau đây?
Phương pháp chưng cất.
Phương pháp chiết.
Phương pháp kết tinh.
Phương pháp sắc kí cột.
Bọ rùa “pháo thủ” là một loài côn trùng thuộc loại bọ cánh cứng đất, tên khoa học là Carabidae. Sở dĩ chúng có biệt danh như vậy là bởi mỗi khi cảm thấy bị đe dọa hay đi săn mồi, Carabidae sẽ phun ra một loạt "đại bác" - vốn là các hóa chất rất độc hại từ phía chóp bụng kèm theo một tiếng nổ nhẹ. Ước tính, trong vòng một giây, số viên "đại bác" được khai hỏa của bọ rùa có thể lên tới 368 - 735 viên. Đặc biệt hơn, bọ rùa "pháo thủ" sản xuất "đại bác" ngay trong các tuyến thuộc khoang bụng của mình. Cụ thể, chúng có hai khoang đựng hydrogen peroxide và hydroquinone dạng lỏng. Hai hóa chất này sẽ được bọ rùa tiết ra, hòa lẫn trong một khoang riêng, với chất xúc tác bao gồm các enzyme như peroxidise và catalase.
Đó là thời điểm tất cả hòa trộn và tạo thành những viên "đại bác" p-benzoquinone ( C 6 H 4 O 2 ) có sức nóng lên tới 1 0 0 ° C và vận tốc gần 10 m/s. Không chỉ vậy mà chất này còn vô cùng độc hại. Nếu người dính phải "đại bác" của bọ rùa, nạn nhân có thể bị bỏng rát, còn những loài côn trùng nhỏ như kiến, mối. thì chắc chắn tử nạn nếu trúng phải đòn tấn công này.

Phản ứng xảy ra khi phóng “đại bác” như sau:
C 6 H 6 O 2 ( a q ) + H 2 O 2 ( a q ) → C 6 H 4 O 2 ( a q ) + 2 H 2 O ( l ) ( 1 )
Tiến hành thí nghiệm cho 5 , 0 0 . 1 0 − 4 m L dung dịch C6H6O2 3,29 mol/L tác dụng với lượng dư H 2 O 2 như phản ứng (1) nhận thấy lượng nhiệt toả ra làm 1 , 0 0 . 1 0 − 3 m L nước tăng từ 2 0 ° C đến 1 0 0 ° C . Biết mối quan hệ giữa nhiệt lượng, nhiệt dung riêng và nhiệt độ như sau: q = m × C × ΔT. Nhiệt dung riêng của nước bằng 4,18 J/g.K và khối lượng riêng của nước: 1,00 g/mL.
Chọn phát biểu đúng?
Phản ứng (1) là phản ứng oxi hoá – khử, H 2 O 2 chất oxi hoá.
Phản ứng (1) là phản ứng oxi hoá – khử, H 2 O 2 chất khử.
Phản ứng (1) là phản ứng trao đổi, H 2 O 2 là chất xúc tác.
Phản ứng (1) là phản ứng trao đổi, H 2 O 2 là dung môi.
Cho các công thức:
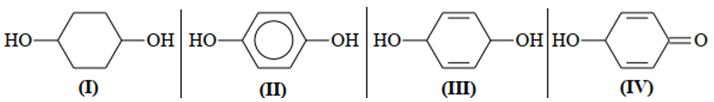
Công thức của hydroquinone ứng với
(I).
(II).
(III).
(IV).
Dựa vào kết quả thí nghiệm tính được hiệu ứng nhiệt của phản ứng (1) là x kJ. x gần nhất với
-550.
202.
302.
+550.








