Đề thi Đánh giá năng lực ĐHQG Hà Nội phần Hóa (có đáp án) - Đề 27
17 câu hỏi
Phát biểu nào sau đây là đúng?
HCl có phân tử khối cao hơn HF nên có nhiệt độ sôi cao hơn.
Phân tử C O 2 ít tan trong nước là do hai liên kết C=O không phân cực.
Hợp chất N a 2 S O 4 có cả liên kết cộng hóa trị và liên kết ion.
Trong phân tử C 2 H 2 có 4 liên kết σ và 2 liên kết π.
Trong phương pháp sắc kí, hỗn hợp lỏng hoặc khí của các chất cần tách là pha động. Pha động tiếp xúc liên tục với pha tĩnh là một chất rắn có diện tích bề mặt rất lớn, có khả năng hấp phụ …(1)… với các chất trong hỗn hợp cần tách, khiến cho các chất trong hỗn hợp di chuyển với tốc độ …(2)… và tách ra khỏi nhau. Cụm từ thích hợp điền vào chỗ trống (1) và (2) lần lượt là
(1) giống nhau và (2) giống nhau.
(1) khác nhau và (2) khác nhau.
(1) khác nhau và (2) giống nhau.
(1) giống nhau và (2) khác nhau.
X, Y, Z, T là một trong số các dung dịch sau: glucose; fructose; glycerol; phenol. Thực hiện các thí nghiệm để nhận biết chúng và có kết quả như sau:
| Chất | Y | Z | X | T |
| Thuốc thử Tollens | Kết tủa bạc trắng | Kết tủa bạc trắng | ||
| Nước Br2 | Nhạt màu | Kết tủa trắng |
Chú ý: Ô để trống là không có hiện tượng xảy ra. Phát biểu nào dưới đây không đúng?
Ở điều kiện thường, X tồn tại chủ yếu ở mạch vòng 6 cạnh có nhóm -OH hemiketal.
Dung dịch Y có nồng độ 5% dùng để truyền tĩnh mạch.
Trong quá trình thủy phân chất béo, có sinh ra chất Z.
Chất T ở điều kiện thường ít tan trong nước nhưng tan tốt trong dung dịch NaOH.
Tiến hành thí nghiệm phản ứng xà phòng hóa theo các bước sau đây:
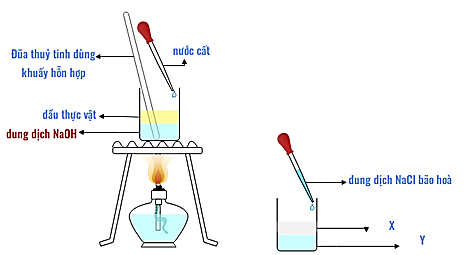
• Bước 1: Cho vào bát sứ khoảng 1 gam mỡ (hoặc dầu thực vật) và 2 - 2,5 mL dung dịch NaOH 40%.
• Bước 2: Đun hỗn hợp sôi nhẹ và liên tục khuấy đều bằng đũa thủy tinh. Thỉnh thoảng thêm vài giọt nước cất để giữ cho thể tích của hỗn hợp không đổi.
• Bước 3: Sau 8 - 10 phút, rót thêm vào hỗi hợp 4 - 5 mL dung dịch NaCl bão hòa nóng, khuấy nhẹ.
Phát biểu nào sau đây sai?
Ở bước 2, xảy ra phản ứng thủy phân chất béo, tạo thành glyccerol và muối sodium của acid béo.
Sau bước 3, lớp X là lớp glycerol và lớp Y là lớp xà phòng.
Sau bước 3, thấy có một lớp dày đóng bánh màu trắng X nổi lên trên, lớp này là muối của acid béo hay còn gọi là xà phòng.
Mục đích của việc thêm dung dịch NaCl bão hòa là làm kết tinh muối của acid béo, đó là do muối của acid béo khó tan trong NaCl bão hòa.
Xà phòng hóa hoàn toàn ester X mạch hở trong dung dịch NaOH, thu được hỗn hợp các chất hữu cơ gồm: ( C O O N a ) 2 , C H 3 C H O và C 2 H 5 O H . Công thức phân tử của X là
C 6 H 1 0 O 4 .
C 6 H 1 0 O 2 .
C 6 H 8 O 2 .
C 6 H 8 O 4 .
Cellulose trinitrate được điều chế từ cellulose và nitric acid đặc có xúc tác sulfuric acid đặc, nóng. Để có 14,85 kg cellulose trinitrate cần dung dịch chứa a kg nitric acid (hiệu suất phản ứng đạt 90% tính theo nitric acid). Giá trị của a là
10,5.
21.
11,5.
30.
Tiêu lệnh chữa cháy do cục cảnh sát phòng cháy, chữa cháy ban hành bao gồm các bước: (a) Dùng bình chữa cháy, cát và nước để dập tắt. (b) Điện thoại số 114 đội chữa cháy chuyên nghiệp. (c) Khi xảy ra cháy báo động gấp. (d) Cúp cầu dao điện nơi xảy ra cháy. Thứ tự đúng của các bước trên là
(d), (c), (a), (b).
(c), (d), (a), (b).
(d), (b), (a), (c).
(c), (d), (b), (a).
Phân tích định lượng Atebrin, một loại thuốc chống sốt rét được quân đồng minh sử dụng rộng rãi trong chiến tranh thế giới lần thứ hai, người ta xác định được chất này chứa 69,1% C, 7,5% H, 10,5% N, 8,9% Cl và 4,0% O. Biết công thức phân tử trùng với công thức đơn giản nhất, tổng số nguyên tử trong một phân tử Atebrin là
58.
60.
59.
57.
Bradykinin là một peptide có trong huyết tương, có vai trò quan trọng trong phản ứng viêm (gây giãn mạch, tăng tính thấm mao mạch và gây đau). Bradykinin có trật tự sắp xếp các amino acid như sau: Arg-Pro-Pro-Gly-Phe-Ser-Pro-Phe-Arg.
Cho các nhận định sau:
(a) Bradykinin thuộc loại nonapeptide.
(b) Thuỷ phân hoàn toàn bradykinin thu được 5 amino acid.
(c) Thuỷ phân không hoàn toàn bradykinin thu được tối đa 7 dipeptide.
(d) Bradykinin phản ứng với C u ( O H ) 2 trong môi trường kiềm tạo dung dịch màu xanh lam.
Các nhận định đúng là
(a), (d).
(c), (d).
(b), (c).
(a), (b).
Poly(vinyl acetate) có kí hiệu là PVAc, được sử dụng phổ biến là làm keo dán gỗ, keo dán giấy, … Poly(vinyl alcohol) có kí hiệu PVOH, được dùng làm chất kết dính, sợi vinylon, vật liệu ứng dụng trong y tế, … PVAc và PVOH được tổng hợp theo sơ đồ sau đây:
H C ≡ C H → + C H 3 C O O H X → x t , t o , p P V A c → + N a O H , t o P V O H
Cho các nhận định sau:
(a) Trong phân tử X có chứa một liên kết đôi C=C.
(b) Phản ứng chuyển hóa từ PVAc thành PVOH làm tăng mạch carbon.
(c) PVOH thuộc loại polymer có mạch không phân nhánh.
(d) Phản ứng điều chế PVAc từ X là phản ứng trùng hợp.
Các nhận định đúng là
(a), (b), (d).
(a), (c), (d).
(b), (d), (d).
(a), (b), (c).
Một pin điện hóa tạo bởi hai cặp oxi hóa – khử ở điều kiện chuẩn: F e 2 + / F e và S n 2 + / S n với thế điện cực chuẩn tương ứng là -0,44 V và -0,137 V.
Cho các phát biểu về pin điện hóa trên như sau:
(a) Anode của pin là Fe.
(b) Cathode của pin là F e 2 + .
(c) Quá trình xảy ra ở anode khi pin hoạt động là: F e 2 + + 2 e → F e .
(d) Quá trình xảy ra ở cathode khi pin hoạt động là: S n 2 + + 2 e → S n .
(e) Sức điện động chuẩn của pin là 0,303 V.
Số phát biểu đúng là
3.
2.
1.
4.
Để xác định nồng độ dung dịch NaOH người ta tiến hành như sau: cân 1,26 gam oxalic acid ngậm nước ( H 2 C 2 O 4 . 2 H 2 O ) hòa tan hoàn toàn vào nước, định mức thành 100 mL. Lấy 10 mL dung dịch này thêm vào đó vài giọt phenolphthalein, đem chuẩn độ bằng dung dịch NaOH đến xuất hiện màu hồng (ở pH = 9) (acid đã bị trung hòa hết) thì hết 17,5 mL dung dịch NaOH. Nồng độ dung dịch NaOH đã dùng là bao nhiêu M? (Làm tròn kết quả đến hàng phần trăm).
0,11
Tiến hành các thí nghiệm điện phân với điện cực trơ sau:
(1) Điện phân sodium chloride nóng chảy.
(2) Điện phân aluminium oxide nóng chảy.
(3) Điện phân dung dịch sodium chloride với màng ngăn xốp.
(4) Điện phân dung dịch copper(II) sulfate.
(5) Điện phân dung dịch nikel sulfate.
Số thí nghiệm thu được kim loại là
4.
2.
1.
5.
Củ sắn khô chứa 38% khối lượng là tinh bột, còn lại là các chất không có khả năng lên men thành ethanol. Lên men 1 tấn sắn khô với hiệu suất cả quá trình là 81%. Toàn bộ lượng ethanol sinh ra để điều chế xăng E5 (có chứa 5% thể tích ethanol). Biết khối lượng riêng của ethanol là 0,8 g/mL, thể tích xăng E5 thu được sau pha trộn là
218,5 lít.
4370 lít.
5430 lít.
534 lít.
Hydrazine ( N 2 H 4 ) là chất lỏng, được sử dụng rộng rãi trong tổng hợp hoá hữu cơ và là một thành phần quan trọng trong nhiên liệu tên lửa, có mùi giống ammonia nhưng lại rất nguy hiểm. Nhiệt lượng toả ra khi 1 mol hydrazine lỏng bị phân huỷ thành ammonia và nitrogen là 111,9 kJ ở điều kiện chuẩn.
Phương trình nhiệt hoá học của phản ứng phân hủy hydrazine lỏng thành ammonia và nitrogen là (biết hệ số cân bằng là số nguyên tối giản nhất)
3 N 2 H 4 ( l ) → 4 N H 3 ( g ) + N 2 ( g ) Δ r H 2 9 8 0 = − 3 3 5 , 7 k J .
3 N 2 H 4 ( g ) → 4 N H 3 ( l ) + N 2 ( g ) Δ r H 2 9 8 0 = − 3 3 5 , 7 k J .
N 2 H 4 ( l ) → 4 N H 3 ( g ) + N 2 ( g ) Δ r H 2 9 8 0 = − 1 1 1 , 9 k J .
3 N 2 H 4 ( l ) → 4 N H 3 ( g ) + N 2 ( g ) Δ r H 2 9 8 0 = − 1 1 1 , 9 k J .
Hydrazine ( N 2 H 4 ) là chất lỏng, được sử dụng rộng rãi trong tổng hợp hoá hữu cơ và là một thành phần quan trọng trong nhiên liệu tên lửa, có mùi giống ammonia nhưng lại rất nguy hiểm. Nhiệt lượng toả ra khi 1 mol hydrazine lỏng bị phân huỷ thành ammonia và nitrogen là 111,9 kJ ở điều kiện chuẩn.
Cho các phát biểu sau về hydrazine, phát biểu nào không đúng?
Hydrazine tan tốt trong nước.
Hydrazine có thể tạo liên kết hydrogen với nước.
Hai nguyên tử N trong hydrazine đều còn đôi electron tự do chưa tham gia liên kết.
Hydrazine không tan được trong nước.
Hydrazine ( N 2 H 4 ) là chất lỏng, được sử dụng rộng rãi trong tổng hợp hoá hữu cơ và là một thành phần quan trọng trong nhiên liệu tên lửa, có mùi giống ammonia nhưng lại rất nguy hiểm. Nhiệt lượng toả ra khi 1 mol hydrazine lỏng bị phân huỷ thành ammonia và nitrogen là 111,9 kJ ở điều kiện chuẩn.
Một nhóm nghiên cứu của trường đại học Old Dominion (Hoa Kỳ) đã tiến hành khảo sát sự chuyển hoá năng lượng nhiệt của phản ứng thành năng lượng cơ học để sử dụng trong động cơ tên lửa mô hình. Thí nghiệm cho thấy rằng với lượng nhiệt toả ra là 4029,5 kJ thì tên lửa đạt độ cao cực đại khi bắn là 134,7 m. Trong các phát biểu sau phát biểu nào đúng?
Với lượng nhiệt toả ra khi phân huỷ 500 gam N 2 H 4 có thể bắn tên lửa đạt độ cao cực đại.
Với lượng nhiệt toả ra khi phân huỷ 500 gam N 2 H 4 không thể bắn tên lửa đạt độ cao cực đại.
Lượng nhiệt tỏa ra khi 500 gam N 2 H 4 bị phân hủy lớn hơn 4029,5 kJ.
Lượng nhiệt tỏa ra khi 500 gam N 2 H 4 bị phân hủy đúng bằng 4029,5 kJ.








