Đề thi Đánh giá năng lực ĐHQG Hà Nội phần Hóa (có đáp án) - Đề 18
17 câu hỏi
Hình dưới đây là ký hiệu của 6 polymer nhiệt dẻo phổ biến có thể tái chế:
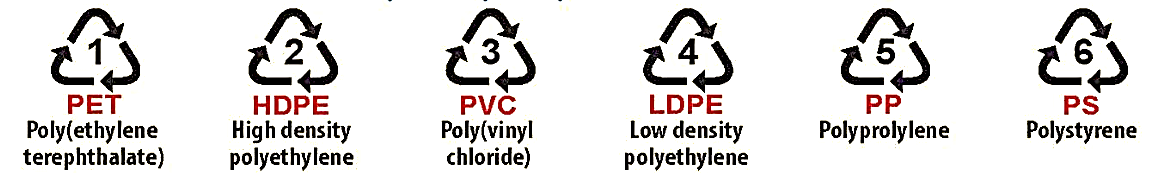
Các ký hiệu này thường được in trên bao bì, vỏ hộp, đồ dùng,… để giúp nhận biết vật liệu polymer cũng như thuận lợi cho việc thu gom, tái chế. Polymer có ký hiệu số 6 được điều chế bằng phản ứng trùng hợp monomer là
C H 2 = C H – C 6 H 5 .
C H 2 = C H – C l .
C H 2 = C H – C H 3 .
C H 2 = C H 2 .
Insulin là hormone có tác dụng điều tiết lượng đường trong máu. Thủy phân một phần insulin thu được heptapeptide X mạch hở. Khi thủy phân không hoàn toàn X, thu được hỗn hợp chứa các peptide: Phe-Phe-Tyr, Pro-Lys-Thr, Tyr-Thr-Pro, Phe-Tyr-Thr. Nếu đánh số thứ tự amino acid đầu N là số 1, thì amino acid ở vị trí số 6 trong X có kí hiệu là
Lys.
Tyr.
Pro.
Thr.
Ethylene là một hydrocarbon không no, có thể tham gia phản ứng với nhiều chất. Phản ứng hóa học của ethylene với dung dịch Br2 có cơ chế phản ứng như sau:
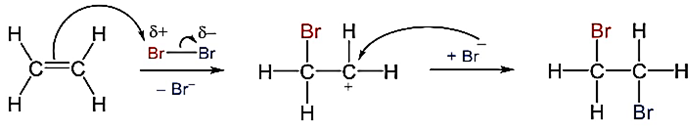
Cho các phát biểu sau:
(a) Phản ứng trên thuộc loại phản ứng thế.
(b) Giai đoạn 1, liên kết đôi phản ứng với tác nhân B r δ + tạo thành phần tử mang điện dương.
(c) Giai đoạn 2, phần tử mang điện dương kết hợp với anion B r − tạo thành sản phẩm.
(d) Hiện tượng của phản ứng là dung dịch bromine bị mất màu.
Số phát biểu đúng là
4.
1.
3.
2.
Tiến hành điện phân dung dịch NaCl bão hoà với điện cực trơ, không sử dụng màng ngăn xốp. Bố trí thí nghiệm như hình vẽ sau:
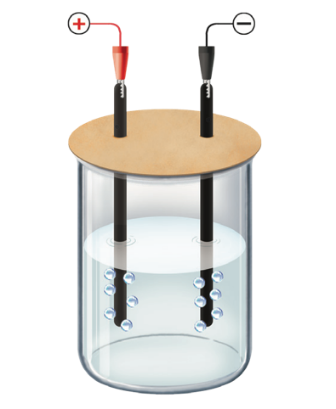
Phát biểu nào dưới đây là đúng?
Dung dịch thu được sau điện phân có khả năng tẩy màu.
Thí nghiệm trên được sử dụng để điều chế kim loại Na trong công nghiệp.
Quá trình xảy ra tại cathode là: 2 H 2 O → O 2 + 4 H + + 4 e .
Quá trình xảy ra tại anode là: 2 H 2 O + 2 e → H 2 + 2 O H − .
Một trong những phương pháp điều chế ester là đun hồi lưu hỗn hợp ethanol, acetic acid và H 2 S O 4 đặc trong bình cầu 1 có chứa đá bọt trong một khoảng thời gian nhất định. Sau đó chưng cất để thu được ester ở nhiệt độ thích hợp như hình bên:
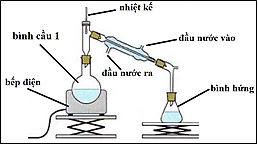
Nhận định nào dưới đây không đúng?
Nếu tiến hành thí nghiệm với 46,0 gam ethanol và 60,0 gam acetic acid, sau một thời gian thu được 22,0 gam chất lỏng ở bình hứng, thì kết luận rằng hiệu suất phản ứng ester hóa đúng bằng 25% (không làm tròn) là hoàn toàn chính xác.
Phản ứng giữa ethanol và acetic acid khi có mặt xúc tác H 2 S O 4 gọi là phản ứng ester hóa.
Ngoài sản phẩm ester và nước thì trong quá trình thí nghiệm còn sinh ra một số sản phẩm phụ.
Ethyl acetate hoặc ethyl ethanoate đều là tên gọi đúng của ester sinh ra trong thí nghiệm trên.
Để xác định nồng độ của dung dịch F e S O 4 bằng dung dịch K M n O 4 (dung dịch thuốc tím), người ta lắp bộ dụng cụ thí nghiệm như hình bên dưới.
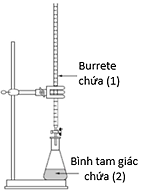
Nhận định nào sau đây đúng?
(1) dung dịch hỗn hợp F e S O 4 và H 2 S O 4 loãng; (2) dung dịch K M n O 4 .
(1) dung dịch hỗn hợp F e S O 4 và K M n O 4 ; (2) dung dịch H 2 S O 4 loãng.
(1) dung dịch K M n O 4 ; (2) dung dịch hỗn hợp F e S O 4 và quỳ tím.
(1) dung dịch K M n O 4 ; (2) dung dịch hỗn hợp F e S O 4 và H 2 S O 4 loãng.
Cho các phát biểu sau:
(a) Tất cả các phản ứng cháy đều tỏa nhiệt.
(b) Phản ứng tỏa nhiệt là phản ứng giải phóng năng lượng dưới dạng nhiệt.
(c) Tất cả các phản ứng mà chất tham gia có chứa nguyên tố oxygen đều tỏa nhiệt.
(d) Phản ứng thu nhiệt là phản ứng hấp thụ năng lượng dưới dạng nhiệt.
(e) Lượng nhiệt mà phản ứng hấp thụ hay giải phóng không phụ thuộc vào điều kiện thực hiện phản ứng và thể tồn tại của chất trong phản ứng.
(g) Sự cháy của nhiên liệu (xăng, dầu, khí gas, than, gỗ, ...) là những ví dụ về phản ứng thu nhiệt vì cần phải khơi mào.
Số phát biểu đúng là
2.
3.
4.
5.
Cồn 70 độ dùng sát khuẩn trong y tế được pha loãng từ ethanol nguyên chất. Trong công nghiệp, ethanol được sản xuất từ nhiều phương pháp khác nhau. Một trong những phương pháp được đánh giá thân thiện hơn với môi trường là đi từ cellulose.
Tại một nhà máy đã tiến hành sản xuất ethanol từ cellulose với hiệu suất của toàn bộ quá trình là 80%. Nhà máy đó đã phải sử dụng bao nhiêu tấn cellulose để thu được 1000 lít cồn nói trên? Biết khối lượng riêng của ethanol nguyên chất là 0,8 gam/mL? (Làm tròn kết quả đến hàng phần trăm).
1,32.
1,23.
0,98.
0,89.
Các nhà nghiên cứu thuộc Viện Công nghệ sinh học và Công nghệ Nano (IBN) của Singapore vừa phát hiện một sơ đồ hóa học mới có thể chuyển hóa đường glucose thành adipic acid như sau:
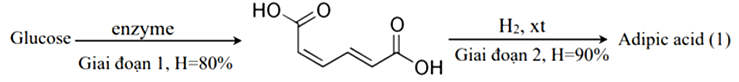
Trong công nghiệp, adipic acid được dùng để sản xuất poly(hexamethylene adipamide) qua phản ứng trùng ngưng giữa hexamethylenediamine và adipic acid với hiệu suất đạt 90%.
Cho các phát biểu sau:
(a) Poly(hexamethylene adipamide) thuộc loại tơ polyamide.
(b) Poly(hexamethylene adipamide) kém bền với acid và kiềm.
(c) Poly(hexamethylene adipamide) có tên gọi khác là nylon-6,6.
(d) Lượng adipic acid được tạo từ 225 kg glucose theo sơ đồ (1) có thể sản xuất được 179 kg chỉ nha khoa. Biết rằng chỉ nha khoa chứa 92% về khối lượng poly (hexamethylene adipamide).
Các phát biểu đúng là
(a), (b), (c).
(b), (c), (d).
(a), (b), (c), (d).
(a), (b), (d).
Biết độ tan trong nước của monosodium glutamate (mì chính hay bột ngọt) ở 6 0 o C là 112 g/100 g nước; ở 2 5 o C là 74 g/ 100 g nước. Có bao nhiêu gam monosodium glutamate kết tinh khi làm nguội 1000 g dung dịch monosodium glutamate bão hoà ở 6 0 o C xuống 2 5 o C ? (giả thiết lượng nước bay hơi không đáng kể)
38 gam.
103,1 gam.
179,24 gam.
145,67 gam.
Các muối carbonate của kim loại nhóm IIA đều bị phân hủy bởi nhiệt:
M C O 3 ( s ) → M O ( s ) + C O 2 ( g ) Δ r H 2 9 8 0
Biến thiên enthalpy chuẩn của quá trình trên được cho trong bảng sau:
| Muối | M g C O 3 (s) | C a C O 3 (s) | S r C O 3 (s) | B a C O 3 (s) |
| Δ r H 2 9 8 0 (kJ) | 100,70 | 179,20 | 234,60 | 271,50 |
Cho các phát biểu sau:
(a). Phản ứng phân hủy muối carbonate của các kim loại nhóm IIA đều là phản ứng toả nhiệt.
(b). Vôi sống CaO tác dụng với nước tỏa nhiệt mạnh, tạo thành vôi tôi C a ( O H ) 2 .
(c). Năng lượng tối thiểu để sản xuất 1,2 tấn vôi sống theo phương pháp nung đá vôi (có hàm lượng C a C O 3 là 72%, còn lại là tạp chất trơ) với than đá là 3480000 kJ.
(d). Độ bền với nhiệt: M g C O 3 < C a C O 3 < S r C O 3 < B a C O 3 .
Các phát biểu đúng là
(a) và (b).
(b) và (c).
(b) và (d).
(c) và (d).
Hydrocarbon X được dùng làm chất chuẩn để đánh giá chất lượng của nhiên liệu hoá thạch (xăng, dầu). Cho phổ khối lượng (MS) và phần trăm khối lượng các nguyên tố trong phân tử của chất X trong hình dưới đây.
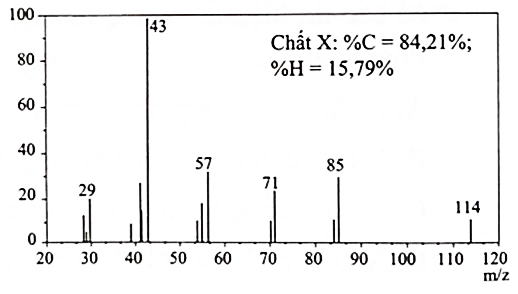
X có số nguyên tử C là (nhập đáp án vào ô trống)?
8
Xét phản ứng giữa methane với chlorine:
C H 4 + C l 2 → a s k t C H 3 C l + H C l
Phản ứng xảy ra theo cơ chế gốc tự do, trong đó giai đoạn phát triển mạch có sự hình thành các gốc tự do C • H 3 và C • l . Giai đoạn tắt mạch có sự kết hợp 2 gốc tự do nói trên, tạo thành C H 3 C l như sau:
C • H 3 + C • l → CH3Cl
Bên cạnh sản phẩm thế mong muốn C H 3 C l , phản ứng còn tạo sản phẩm phụ nào dưới đây?
C 2 H 2 .
C 2 H 4 .
C 2 H 6 .
C 2 H 5 O H .
Chỉ số octane là một đại lượng biểu thị khả năng chống kích nổ của nhiên liệu xăng trong động cơ đốt trong. Quy ước isooctane có chỉ số octane bằng 100 và heptane có chỉ số octane bằng 0. Một công ty sản xuất nhiên liệu đang triển khai chiến dịch “Nhiên liệu sạch – Động cơ bền – Môi trường xanh”. Trong chiến dịch này, họ loại bỏ dần các phụ gia chứa chì, nâng cao chỉ số octane của xăng và cung cấp nguồn nhiên liệu thân thiện với môi trường. Có một số giải pháp được đưa ra như sau:
(a) Tăng hàm lượng heptane để giảm chi phí.
(b) Phối trộn ethanol vào xăng truyền thống để tạo ra xăng sinh học (E5, E10).
(c) Thêm các hợp chất chứa lưu huỳnh để làm tăng hiệu suất cháy của nhiên liệu.
(d) Sử dụng tetraethyl chì ( P b ( C 2 H 5 ) 4 ) làm phụ gia để nâng cao chỉ số octane.
(e) Sử dụng các quá trình reforming xúc tác để tăng hàm lượng hydrocarbon phân nhánh.
Các giải pháp phù hợp được lựa chọn là
(b), (d).
(c), (d).
(b), (c), (d).
(a), (b), (d).
Giả sử phản ứng đơn giản: mM + nN → sản phẩm có biểu thức tốc độ phản ứng:
v = k C M m C N n .
Biểu thức này cho thấy khi nồng độ các chất được giữ không đổi, hằng số tốc độ k tăng (giảm) bao nhiêu lần thì tốc độ phản ứng v cũng tăng (giảm) bấy nhiêu lần. Như vậy, có thể thông qua sự thay đổi giá trị của k để đánh giá sự thay đổi tốc độ phản ứng.
Phương trình Arrehenius giúp chúng ta có thể tính được sự thay đổi của hằng số tốc độ phản ứng k theo năng lượng hoạt hóa E a ( J m o l − 1 ) và nhiệt độ T (Kelvin).
k = A e − E a R T
Trong đó:
A là một hằng số cho một phản ứng xác định.
R là hằng số khí, R = 8,314 J K − 1 m o l − 1 .
Phản ứng giữa H 2 và N 2 là phản ứng đơn giản: N 2 (g) + 3 H 2 (g) 2 N H 3 (g). Tốc độ của phản ứng trên được viết dưới dạng:
v = k C N H 3 3 C H 2 3 .
v = k C N 2 C H 2 3 .
v = k C N H 3 C H 2 .
v = k C N H 3 3 C H 2 .
Phản ứng của H 2 và I 2 là phản ứng đơn giản: H 2 (g) + I 2 (g) 2HI(g). Nếu nồng độ của H2 tăng lên 4 lần thì tốc độ phản ứng thay đổi như thế nào?
tăng lên 4 lần.
giảm đi 4 lần.
tăng lên 16 lần.
giảm đi 16 lần.
Cho hằng số tốc độ của một phản ứng là 1 1 M − 1 . s − 1 tại nhiệt độ 345K và hằng số thực nghiệm Arrhenius là 2 0 M − 1 . s − 1 . Năng lượng hoạt hóa của phản ứng trên gần với
1715 mol.
1715 k J m o l − 1 .
715 k J m o l − 1 .
715 mol.








