Đề thi cuối kì 2 Hóa 10 Chân trời sáng tạo cấu trúc mới (có tự luận) có đáp án - Đề 3
21 câu hỏi
Số oxi hóa của Fe trong hợp chất Fe2O3 là
+2.
+3.
+4.
+6.
Phản ứng oxi hóa – khử là
phản ứng hóa học giữa đơn chất và hợp chất, trong đó nguyên tử của đơn chất thay thế nguyên tử của một nguyên tố khác trong hợp chất.
phản ứng hóa học trong đó một chất sinh ra hai hay nhiều chất mới.
phản ứng hóa học trong đó có sự thay đổi số oxi hóa của ít nhất một nguyên tố hóa học.
phản ứng hóa học trong đó hai hay nhiều chất ban đầu sinh ra một chất mới.
Kí hiệu biến thiên enthalpy (nhiệt phản ứng) của phản ứng ở điều kiện chuẩn là
Δ r H 2 9 8 o .
Δ f H 2 9 8 o .
Δ f H .
Δ r H .
Phương trình hóa học nào sau đây biểu thị enthalpy tạo thành chuẩn của CO(g)?
2C (graphite) + O 2 ( g ) → 2 C O ( g ) .
C (graphite) + O ( g ) → C O ( g ) .
C (graphite) + 1 2 O 2 ( g ) → C O ( g ) .
C (graphite) + C O 2 ( g ) → 2 C O ( g ) .
Tốc độ phản ứng là
độ biến thiên nồng độ của một chất phản ứng trong một đơn vị thời gian.
độ biến thiên nồng độ của một sản phẩm phản ứng trong một đơn vị thời gian.
độ biến thiên nồng độ của một chất phản ứng hoặc sản phẩm phản ứng trong một đơn vị thời gian.
độ biến thiên nồng độ của các chất phản ứng trong một đơn vị thời gian.
Trong các cặp phản ứng sau, nếu lượng Fe trong các cặp đều được lấy bằng nhau và có kích thước như nhau thì cặp nào có tốc độ phản ứng lớn nhất?
Fe + dung dịch HCl 0,3 M.
Fe + dung dịch HCl 0,5 M.
Fe + dung dịch HCl 0,1 M.
Fe + dung dịch HCl 0,2 M.
Nguyên tố nào sau đây là nguyên tố halogen?
Nitrogen.
Bromine.
Oxygen.
Carbon.
Khi đun nóng, chất thăng hoa chuyển từ thể rắn sang thể hơi màu tím là
C l 2 .
F 2 .
B r 2 .
I 2 .
Hòa tan khí C l 2 vào dung dịch KOH loãng, dư ở nhiệt độ phòng thu được dung dịch chứa các chất
K C l , K C l O , K O H , H 2 O .
K C l , K C l O , H 2 O .
K C l , K C l O 3 , K O H .
K C l , K C l O 3 , C l 2 .
Để khắc chữ lên thủy tinh người ta dùng chất nào?
HF đặc.
HBr đặc.
HI đặc.
HCl đặc.
Phát biểu nào sau đây liên quan đến halogen halide (HX) là không đúng?
Các halogen halide dễ tan trong nước phân li hoàn toàn thanh H + và X − .
Liên kết H – I kém bền nhất trong các liên kết H – X.
Tính acid của các hydrogen halide tăng dần từ HF đến HI.
Liên kết trong phân tử hydrogen halide là liên kết công hóa trị không phân cực.
Cho muối halide nào sau đây tác dụng với dung dịch H 2 S O 4 đặc, nóng thì chỉ xảy ra phản ứng trao đổi?
KBr.
KI.
NaCl.
NaBr.
Xét phản ứng:
H2 + Cl2 → 2HCl.
Nghiên cứu sự thay đổi nồng độ một chất trong phản ứng theo thời gian, thu được đồ thị sau:
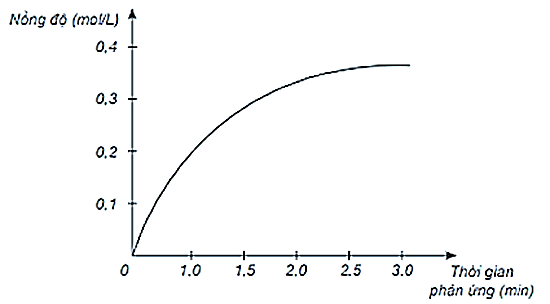
Đồ thị mô tả sự thay đổi nồng độ theo thời gian của H2.
Đồ thị mô tả sự thay đổi nồng độ theo thời gian của Cl2.
Biểu thức tốc độ trung bình của phản ứng là ν ¯ = − Δ C H 2 Δ t = − Δ C C l 2 Δ t = Δ C H C l 2 Δ t .
Phản ứng trên có thể xảy ra ngay trong bóng tối.
Cho hình vẽ mô tả thí nghiệm điều chế chlorine từ MnO2 và dung dịch HCl:
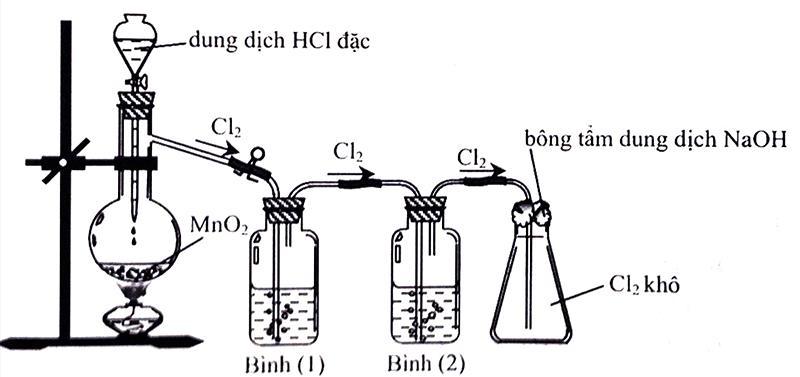
Để thu được khí chlorine khô thì bình (1) và bình (2) lần lượt đựng dung dịch NaCl bão hòa và dung dịch H2SO4 đặc.
Bông tẩm dung dịch NaOH dùng để ngăn không cho khí chlorine thoát ra ngoài.
Có thể thay acid HCl đặc bằng acid H2SO4 đặc.
Có thể thu khí chlorine bằng phương pháp đẩy nước.
Cho các phương trình nhiệt hóa học của các phản ứng sau:
(1) 3Fe(s) + 4H2O(l) → Fe3O4(s) + 4H2(g) Δ r H 2 9 8 o = +26,32 kJ
(2) N2(g) + O2(g) → 2NO(g) Δ r H 2 9 8 o = +179,20 kJ
(3) Na(s) + 2H2O(l) → NaOH(aq) + H2(g) Δ r H 2 9 8 o = ‒ 367,50 kJ
(4) 2ZnS(s) + 3O2(g) → 2ZnO(s) + 2SO2(g) Δ r H 2 9 8 o = ‒285,66 kJ
(5) ZnSO4(s) → ZnO(s) + SO3(g) ; Δ r H 2 9 8 o = + 235,21 kJ
Có bao nhiêu phản ứng thuộc loại phản ứng tỏa nhiệt?
2
Khi nhiệt độ tăng lên 10 oC, tốc độ của một phản ứng hóa học tăng lên 3 lần. Hỏi tốc độ của phản ứng đó tăng lên bao nhiêu lần khi nâng nhiệt độ lên từ 30 oC đến 50 oC?
9
Thực hiện các thí nghiệm sau:
(a) H 2 O + F 2
(b) Dung dịch N a O H + C l 2 → t o
(c) Dung dịch N a B r + I 2
(d) Dung dịch N a I + C l 2
Ở điều kiện thích hợp, có bao nhiêu phản ứng tạo ra đơn chất?
2
Cho 13,05 gam M n O 2 tác dụng với acid HCl đặc, dư. Khí chlorine sinh ra tác dụng vừa đủ với bao nhiêu gam sắt?
5,6
(1 điểm). Butane là một trong hai thành phần chính của khí LPG - Khí dầu mỏ hóa lỏng. Phản ứng đốt cháy butane sau:
C 4 H 1 0 ( g ) + O 2 ( g ) → C O 2 ( g ) + H 2 O ( g )
Biết năng lượng liên kết trong các hợp chất cho trong bảng sau:
| Liên kết | Phân tử | Eb (kJ/mol) | Liên kết | Phân tử | Eb (kJ/mol) |
| C – C | C 4 H 1 0 | 346 | C = O | C O 2 | 799 |
| C – H | C 4 H 1 0 | 418 | O – H | H 2 O | 467 |
| O = O | O 2 | 495 |
Giả thiết mỗi ấm nước chứa 2 L nước ở 2 5 o C , nhiệt dung của nước là 4,2 J/g.K, có 40% nhiệt đốt cháy butane bị thất thoát ra ngoài môi trường. Một bình gas chứa 12 kg butane có thể đun sôi bao nhiêu ấm nước?
(1 điểm). Cho phản ứng sau:
B r O 3 − + 5 B r − + 6 H + → 3 B r 2 + 3 H 2 O
Sau một thời gian t đo được: − Δ C B r − Δ t = 2 , 0 . 1 0 − 3 ( M s − 1 ) .
Tốc độ trung bình của phản ứng trên trong khoảng thời gian t là bao nhiêu?
(1 điểm). Bằng phương pháp hóa học, hãy phân biệt các dung dịch sau chứa trong các lọ riêng biệt mất nhãn: HCl, NaCl, NaI.








