Bộ 3 đề thi giữa kì 2 Hóa 10 Chân trời sáng tạo có đáp án - Đề 3
32 câu hỏi
Số oxi hóa của nguyên tử trong đơn chất luôn bằng
0.
+1.
-2.
-1.
Trong một phân tử, tổng số oxi hoá của các nguyên tử bằng
0.
điện tích ion.
hoá trị của kim loại.
hoá trị của phi kim.
Phản ứng nào sau đây là phản ứng oxi hóa – khử?
2 C a + O 2 → t 0 2 C a O .
C a C O 3 → t 0 C a O + C O 2 .
C a O + H 2 O → t 0 C a ( O H ) 2 .
C a ( O H ) 2 + C O 2 → C a C O 3 + H 2 O .
Cho quá trình S + 6 + 2 e → S + 4 , đây là
quá trình oxi hóa.
quá trình khử.
quá trình nhận proton.
quá trình nhường electron.
Phản ứng oxi hóa – khử là phản ứng có sự nhường và nhận
electron.
neutron.
proton.
cation.
Khi tham gia các phản ứng đốt cháy nhiên liệu, oxygen đóng vai trò là
chất khử.
chất oxi hóa.
acid.
base.
Áp suất đối với chất khí ở điều kiện chuẩn là
1 bar.
1 atm.
760 mmHg.
1 Pa.
Phản ứng nào sau đây là phản ứng toả nhiệt?
Phản ứng nhiệt phân muối KNO3.
Phản ứng phân hủy khí NH3.
Phản ứng oxi hoá glucose trong cơ thể.
Phản ứng hoà tan NH4Cl trong nước.
Enthalpy tạo thành chuẩn (nhiệt tạo thành chuẩn) của một chất có kí hiệu là
Δ r H 2 9 8 0 .
Δ f H 2 9 8 0 .
∆S.
∆T.
Cho các chất sau, chất nào có nhiệt tạo thành chuẩn bằng 0?
CO2(g).
Na2O(g).
O2(g).
H2O(l).
Nhiệt lượng tỏa ra hay thu vào của phản ứng ở điều kiện áp suất không đổi gọi là
biến thiên nhiệt độ của phản ứng.
biến thiên enthalpy của phản ứng.
enthalpy của phản ứng.
biến thiên năng lượng chuẩn của phản ứng.
Ở điều kiện chuẩn. Khi phản ứng thu nhiệt thì
Δ r H 2 9 8 0 > 0 .
Δ r H 2 9 8 0 = 0 .
Δ r H 2 9 8 0 < 0 .
Δ r H 2 9 8 0 ≥ 0 .
Nhiệt độ thường được chọn ở điều kiện chuẩn là
20oC.
25oC.
24oC.
22oC.
Trong phản ứng thu nhiệt, sự so sánh nào sau đây đúng về ∑ Δ f H 2 9 8 0 ( c d ) và ∑ Δ f H 2 9 8 0 ( s p ) ?
∑ Δ f H 2 9 8 0 ( c d ) = ∑ Δ f H 2 9 8 0 ( s p ) .
∑ Δ f H 2 9 8 0 ( c d ) > ∑ Δ f H 2 9 8 0 ( s p ) .
∑ Δ f H 2 9 8 0 ( c d ) + ∑ Δ f H 2 9 8 0 ( s p ) = 0 .
∑ Δ f H 2 9 8 0 ( c d ) < ∑ Δ f H 2 9 8 0 ( s p ) .
Cho phản ứng tổng quát: aA + bB → mM + nN. Hãy chọn phương án tính đúng Δ r H 2 9 8 o của phản ứng:
Δ r H 2 9 8 K o = m × Δ f H 2 9 8 o ( M ) + n × Δ f H 2 9 8 o ( N ) + a × Δ f H 2 9 8 o ( A ) + b × Δ f H 2 9 8 o ( B )
Δ r H 2 9 8 K o = a × Δ f H 2 9 8 o ( A ) + b × Δ f H 2 9 8 o ( B ) − m × Δ f H 2 9 8 o ( M ) − n × Δ f H 2 9 8 o ( N )
Δ r H 2 9 8 K o = m × E b ( M ) + n × E b ( N ) − a × E b ( A ) − b × E b ( B )
Δ r H 2 9 8 K o = a × E b ( A ) + b × E b ( B ) − m × E b ( M ) − n × E b ( N )
Cho phản ứng hoá học: Cu + HNO3 → Cu(NO3)2 + NO + H2O.
Tổng hệ số cân bằng (nguyên, tối giản) của phản ứng là
18.
20.
19.
17.
Số oxi hóa của carbon trong HCO3- và CO32- lần lượt là
+2, +4.
-2, -4.
-1, -2.
+4, +4.
Số oxi hóa của manganese (Mn) trong KMnO4 là
+1.
+5.
+7.
-2.
Cho các phản ứng sau:
(1) 2SO2 + O2 ⇄ 2SO3.
(2) SO2 + 2H2S → 3S + 2H2O.
(3) SO2 + Br2 + 2H2O → 2HBr + H2SO4.
Các phản ứng mà SO2 có tính khử là?
(1), (2).
(1), (3).
(2), (3).
(1).
Trong giai đoạn đầu sản xuất nitric acid từ ammonia. Ammonia bị oxi hóa bởi oxygen ở nhiệt độ cao khi có chất xúc tác.
NH3+ O2→pxt,t0NO + H2O
Tổng hệ số cân bằng (tối giản) của phản ứng là?
18.
19.
20.
21.
Trong quá trình sản xuất nitric acid xảy ra những quá trình sau đối với nitrogen
N 2 → ( 1 ) N H 3 → ( 2 ) N O → ( 3 ) N O 2 → ( 4 ) H N O 3
Số phản ứng nguyên tố nitrogen đóng vai trò chất khử là?
1.
2.
3.
4.
Cho phương trình nhiệt hoá học của phản ứng.
2H2(g) + O2(g) → 2H2O(l) Δ r H 2 9 8 0 = - 571,68 kJ
Phản ứng trên là phản ứng
thu nhiệt và hấp thu 571,68 kJ nhiệt.
không có sự thay đổi năng lượng.
toả nhiệt và giải phóng 571,68 kJ nhiệt.
có sự hấp thụ nhiệt lượng từ môi trường xung quanh.
Dựa vào phương trình nhiệt hoá học của phản ứng sau:
N2(g) + 3H2(g) → 2NH3(g) Δ r H 2 9 8 0 = – 91,8 kJ
Giá trị Δ r H 2 9 8 0 của phản ứng: 2NH3(g) → N2(g) + 3H2(g) là
-45,9 kJ.
+45,9 kJ.
– 91,8 kJ
+91,8 kJ.
Đồ thị nào sau đây thể hiện đúng sự thay đổi nhiệt độ khi dung dịch hydrochloric acid được cho vào dung dịch sodium hydroxide tới dư?
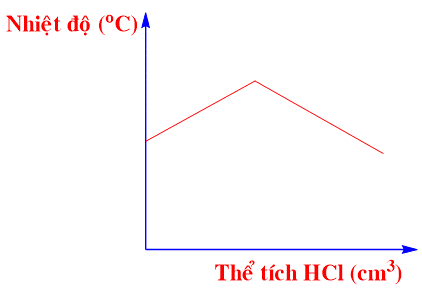
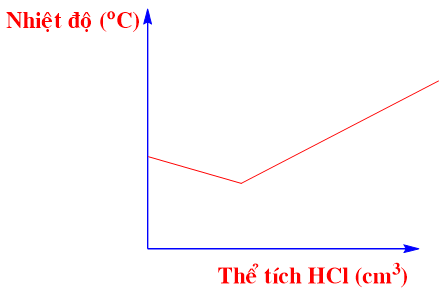
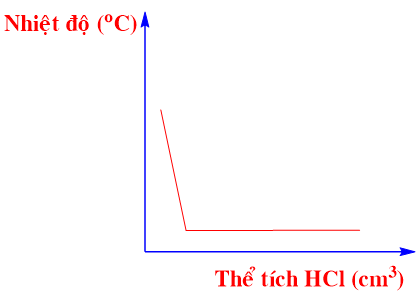
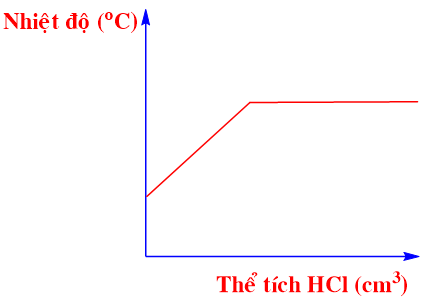
Cho hai phương trình nhiệt hóa học sau:
C(s) + H2O(g) → t o CO(g) + H2(g) Δ r H 2 9 8 0 = +131,25 kJ (1)
CuSO4(aq) + Zn(s) → ZnSO4(aq) + Cu(s) Δ r H 2 9 8 0 = -231,04 kJ (2)
Nhận xét nào sau đây là đúng?
Phản ứng (1) tỏa nhiệt và phản ứng (2) thu nhiệt.
Cả 2 phản ứng đều tỏa nhiệt.
Cả 2 phản ứng đều thu nhiệt.
Phản ứng (1) thu nhiệt và phản ứng (2) tỏa nhiệt.
Cho các phát biểu sau:
(1) Phản ứng phân huỷ Fe(OH)3(s) không cần cung cấp nhiệt độ liên tục.
(2) Số oxi hóa của hydrogen trong các hydride kim loại bằng +1.
(3) Hoà tan NH4Cl(s) vào nước là quá trình thu nhiệt.
(4) Để giữ ấm cơ thể, trước khi lặn, người ta thường uống nước mắm cốt.
Số phát biểu đúng là
2.
3.
1.
4.
Ở điều kiện chuẩn, cần phải cung cấp 26,48 kJ nhiệt lượng cho quá trình 0,5 mol H2(g) phản ứng với 0,5 mol I2(s) để thu được 1 mol HI(g). Ta nói enthalpy tạo thành của HI(g) ở điều kiện chuẩn là 26,48 kJ/mol. Phản ứng trên được biểu diễn như sau:
1 2 H2(g) + 1 2 I2(g) → HI(g) Δ f H 2 9 8 0 = 2 6 , 4 8 k J / m o l
Ở cùng điều kiện phản ứng, nếu thu được 3 mol HI thì lượng nhiệt cần thu vào là
26,48 kJ.
52,96 kJ.
79,44 kJ.
794,4 kJ.
(1 điểm): Cân bằng phản ứng sau bằng phương pháp thăng bằng electron, nêu rõ chất oxi hóa, chất khử trong mỗi trường hợp sau:
(a) H2S + SO2 → S + H2O.
(b) Cu + H2SO4 → CuSO4 + SO2 + H2O.
(1 điểm): Cho phản ứng xảy ra trong quá trình luyện gang như sau:
Fe2O3(s) + 3CO(g) → 2Fe(s) + 3CO2(g)
Tính biến thiên enthalpy chuẩn của phản ứng. Biết:
| Chất | CO (s) | Fe2O3 (s) | Fe (s) | CO2 (g) |
| Δ f H 2 9 8 0 (kJmol-1) | -110,5 | -824,2 | 0 | -393,5 |
(0,5 điểm): Viết phương trình nhiệt hóa học của phản ứng tạo thành 2 mol NH3(g) từ N2(g) và H2(g), biết khi sử dụng 7 g khí N2 sinh ra 22,95 kJ nhiệt.
(0,5 điểm): Trong công nghiệp, sulfuric acid được sản xuất từ quặng pirite sắt có thành phần chính là FeS2, theo sơ đồ sau:
FeS2 → SO2 → SO3 → H2SO4
(a) Có bao nhiêu phản ứng oxi hoá – khử trong sơ đồ trên?
(b) Tính khối lượng H2SO4 98% điều chế được từ 1 tấn quặng chứa 60% FeS2. Biết hiệu suất cả quá trình là 80%.
Số oxi hoá của fluorine trong các hợp chất là
0.
+1.
+7.
-1.








