Bộ 5 đề thi cuối kì 1 Hóa 10 Cánh diều (2022-2023) có đáp án - Đề 5
32 câu hỏi
Hạt nhân của hầu hết các nguyên tử (trừ 1 1 H) được tạo nên từ
proton và electron.
electron và neutron.
proton và neutron.
proton.
Hình bên là mô phỏng của AO
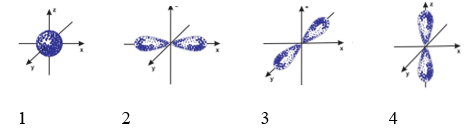
Đâu là hình mô phỏng của AOp
1; 2; 3.
2; 3; 4.
1; 3; 4.
1; 2; 4.
Số phân lớp electron tối đa trong các lớp K, L, M, N lần lượt là
1, 4, 9 và 16.
1, 2, 3 và 4.
2, 6, 10 và 14.
2, 8, 18 và 32.
Số nguyên tố trong chu kì 3 và 5 của bảng tuần hoàn lần lượt là
8 và 18.
2 và 8.
8 và 8.
18 và 32.
Trong một chu kì, đại lượng nào sau đây không biến đổi tuần hoàn theo chiều tăng của điện tích hạt nhân?
Bán kính nguyên tử.
Hóa trị trong công thức oxide cao nhất.
Độ âm điện của nguyên tử.
Số lớp electron trong nguyên tử.
Trong một nhóm A (trừ nhóm VIIIA), theo chiều tăng của điện tích hạt nhân nguyên tử thì
tính kim loại tăng dần, độ âm điện tăng dần.
tính phi kim giảm dần, bán kính nguyên tử tăng dần.
tính acid giảm dần, tính phi kim tăng dần.
tính kim loại tăng dần, tính base giảm dần.
Cho mô hình nguyên tử của X.
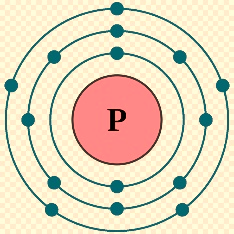
Công thức hợp chất khí của X với hydrogen là
XH2.
XH4.
XH.
XH3.
Nguyên tố X thuộc nhóm VIIIA của bảng tuần hoàn. Cấu hình electron lớp ngoài cùng của nguyên tử nguyên tố X là
ns2np5.
ns2np3.
ns2np1.
ns2np6.
Theo quy tắc octet, khi hình thành liên kết hóa học, các nguyên tử có xu hướng nhường, nhận hoặc góp chung electron để đạt cấu hình electron bền vững giống với
kim loại kiềm gần kề.
kim loại kiềm thổ gần kề.
nguyên tử halogen gần kề.
nguyên tử khí hiếm gần kề.
Tính chất nào sau đây không là tính chất của hợp chất ion?
Nhiệt độ nóng chảy cao.
Tan nhiều trong nước.
Khó bay hơi.
Nhiệt độ sôi thấp.
Liên kết cọng hóa trị là liên kết được tạo thành bằng
lực hút tĩnh điện giữa các electron tự do với ion dương kim loại.
cặp electron chung giữa hai nguyên tử.
lực hút tĩnh điện giữa các ion mang điện trái dấu.
cặp electron chung chỉ do một nguyên tử đóng góp.
Phân tử nào dưới đây chỉ không chứa ion đa nguyên tử?
Na2SO4.
NH4HCO3.
CaCl2.
Al(NO3)3.
Chất nào sau đây có liên kết cộng hóa trị phân cực?
K2O.
NaCl.
AlCl3.
H2S.
Cho cấu hình electron của nguyên tử oxygen là 1s22s22p4. Để hình thành phân tử O2, mỗi nguyên tử O góp chung n electron. Giá trị của n là
1.
4.
3.
2.
Liên kết ion là liên kết được hình thành
giữa kim loại điển hình và phi kim điển hình.
bởi lực hút tĩnh điện giữa hai lưỡng cực tạm thời.
giữa ion kim loại với electron tự do.
giữa hai nguyên tử bằng một hay nhiều cặp electron chung.
Tương tác van der Waals tồn tại giữa những
ion.
hạt proton.
hạt neutron.
nguyên tử khí hiếm.
Nguyên tử nguyên tố oxygen có 16 hạt mang điện và 10 hạt không mang điện. Số khối hạt nhân nguyên tử oxygen là
10.
16.
18.
26.
Nguyên tử X có phân mức năng lượng cao nhất là 4s1. Điện tích hạt nhân của X là
+24.
+11.
+29.
+19.
Nguyên tử của nguyên tố X có cấu hình electron ở trạng thái cơ bản là 1s22s22p63s23p63d54s1. Trong bảng tuần hoàn X thuộc
chu kỳ 3, nhóm IA.
chu kỳ 4, nhóm IB.
chu kỳ 4, nhóm VIB.
chu kỳ 3, nhóm VIA.
Cho bản tuần hoàn các nguyên tố hóa học:
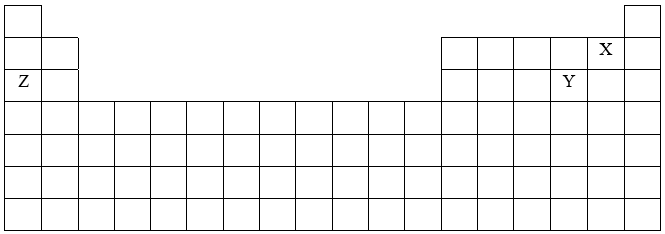
Dãy gồm các nguyên tố được sắp xếp theo chiều tăng dần bán kính nguyên tử từ trái sang phải là
Z, Y, X.
Y, Z, X.
X, Y, Z.
Y, X, Z.
Ba nguyên tố với số hiệu nguyên tử lần lượt là 11, 12, 13 có hydroxide tương tứng là X, Y, T. Chiều tăng dần tính acid của hydroxide này là
X, Y, T.
X, T, Y.
T, X, Y.
T, Y, X.
Nguyên tử nguyên tố X có phân lớp electron ngoài cùng là 2p2. Công thức oxide cao nhất của X, hydroxide tương ứng và tính chất của các hợp chất lần lượt là
X2O3, X(OH)3, tính lưỡng tính.
XO3, H2XO4, tính acid.
XO2, H2XO3, tính acid.
XO, X(OH)2, tính base.
Khi hình thành liên kết hóa học, nguyên tử nào sau đây có xu hướng nhận 1 electron để đạt cấu hình electron bền vững của khí hiếm theo quy tắc octet?
X (Z=20).
Y (Z=35).
Z (Z=19).
T (Z=16).
Cho cấu hình electron nguyên tử của các nguyên tố sau: X ([Xe]6s2), Y ([Ar]3d104s24p5). Hợp chất được tạo thành từ X và Y có công thức là
XY2, hợp chất ion.
X2Y3, hợp chất cộng hóa trị.
X2Y, hợp chất ion.
X3Y2, hợp chất cộng hóa trị.
Liên kết trong phân tử nào sau đây mang nhiều đặc tính ion nhất?
Rb2O.
Li2O.
K2O.
Na2O.
Cho biết: H (Z=1), C (Z=6), O (Z=8). Trong phân tử C2H2 và H2O, tổng số cặp electron chưa tham gia liên kết lần lượt là
0 và 2.
5 và 2.
4 và 3.
2 và 2.
Dãy chất nào sau đây chỉ có liên kết cộng hóa trị phân cực?
H2S, Na2O, AlCl3.
NH4NO3, H2O, HCl.
H2, H2O, NH3.
H2O, CO2, Al2S3.
Chất nào sau đây tan nhiều trong nước?
O2.
C3H4.
CH3NH2.
H2S.
(1 điểm) X có Z = 12, được sử dụng để làm cho hợp kim nhẹ bền, đặc biệt là cho ngành công nghiệp hàng không vũ trụ, và cũng được sử dụng trong flashbulbs và pháo hoa bởi vì nó đốt cháy với một ngọn lửa trắng rực rỡ.
(a) Viết cấu hình electron và xác định vị trí của X trong bản hệ thống tuần hoàn.
(b) Cho biết xu hướng cơ bản của nguyên tử X khi hình thành liên kết hóa học. Hãy vẽ sơ đồ minh họa quá trình đó.
(1 điểm) Cho các chất sau: HCl, N2.
(a) Phân loại các chất trên theo liên kết (ion, cộng hóa trị phân cực, cộng hóa trị không phân cực).
(b) Biểu diễn sự hình thành liên kết ion đối với hợp chất ion; viết công thức electron, công thức Lewis, công thức cấu tạo đối với hợp chất cộng hóa trị.
(0,5 điểm) Hãy giải thích sự biến đổi về nhiệt độ nóng chảy của dãy các chất sau:
| Chất | C2H6 | HF | K2O |
| Nhiệt độ nóng chảy | -182,76 °C | -83,6 °C | 740 °C |
(0,5 điểm) Một hợp chất có công thức MX. Tổng số các hạt trong hợp chất là 84, trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 28. Nguyên tử khối của X lớn hơn của M là 8. Tổng số các hạt trong X2- nhiều hơn M2+ là 16. Tìm số proton của nguyên tử M và X.








