Bộ 5 đề thi cuối kì 1 Hóa 10 Cánh diều (2022-2023) có đáp án - Đề 2
32 câu hỏi
Cho biết cấu hình electron của X: 1s2 2s2 2p6 3s2 của Y là 1s2 2s2 2p6 3s2 3p6 4s2. Nhận xét nào sau đây là đúng?
X và Y đều là các phi kim.
X là phi kim, Y là kim loại.
X và Y đều là các kim loại.
X và Y đều là các khí hiếm.
Liên kết ion là liên kết hóa học được hình thành bằng lực hút tĩnh điện giữa
cation và electrong tự do.
cation và anion.
electron và hạt nhân nguyên tử.
các ion mang điện tích dương.
Lớp thứ 3 (lớp M) gồm những phân lớp là:
3p, 3d, 3f.
3s, 3p.
3s, 3d, 3f.
3s, 3p, 3d.
Hợp chất nào sau đây có liên kết ion?
H2O.
HCl.
NaCl.
NH3.
Cho các nguyên tử X, Y, Z, T có các đặc điểm như sau:
(1) nguyên tử X có 17 proton và số khối bằng 35.
(2) nguyên tử Y có 16 neutron và số khối 33.
(3) nguyên tử Z có 17 neutron và 15 proton.
(4) nguyên tử T có 20 neutron và số khối bằng 36.
Những nguyên tử là đồng vị của cùng một nguyên tố hóa học là
Z và Y.
X và Y.
Y và T.
X và T.
Các nguyên tố nào sau đây thường tạo được liên kết hydrogen?
S, O, N.
O, N, P.
F, O, N.
F, Cl, N.
Kí hiệu của orbital chứa 2 electron là:
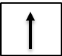 .
.
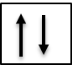 .
.
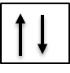 .
.
 .
.
Nguyên tố hóa học là những nguyên tử có cùng
số proton.
số khối.
số neutron và số proton.
số neutron.
Bảng tuần hoàn hiện nay có số cột, số nhóm A và số nhóm B lần lượt là
18, 8, 10.
18, 10, 8.
18, 8, 8.
16, 8, 8.
Theo quy tắc octet, khi hình thành liên kết hoá học, các nguyên tố có xu hướng nhường, nhận hoặc góp chung electron để đạt tới cấu hình electron bền vững giống như
nguyên tử halogen gần kề.
kim loại kiềm gần kề.
nguyên tử khí hiếm gần kề.
kim loại kiềm thổ gần kề.
Số hiệu nguyên tử của nguyên tố hoá học bằng
số thứ tự của nhóm.
so electron lớp ngoài cùng của nguyên tử.
số thứ tự của ô nguyên tố.
số thứ tự của chu kỉ,
Nhận định nào sau đây là đúng khi nói về ba nguyên tử: 1 3 2 6 X , 2 6 5 5 Y và 1 2 2 6 Z ?
X, Y thuộc cùng một nguyên tố hóa học.
X, Z là hai đồng vị của cùng một nguyên tố hóa học.
X và Y cùng số neutron.
X và Z có cùng số khối.
Chu kì là dãy các nguyên tố được sắp xếp theo chiều điện tích hạt nhân tăng dần, nguyên tử của chúng có cùng
Số electron.
Số electron hóa trị.
Số electron ở phân lớp ngoài cùng.
Số lớp electron.
Chất nào sau đây không thể tạo được liên kết hydrogen?
HF.
NH3.
C2H5OH.
C2H6.
Nguyên tố hoá học X thuộc chu kỳ 3 nhóm VIA. Cấu hình electron của nguyên tử X là
1s22s22p63s23p4.
1s22s22p63s23p2.
1s22s22p63s23p3.
1s22s22p63s23p5.
Để đạt quy tắc octet, nguyên tử của nguyên tố potassium (Z = 19) phải nhường đi
1 electron.
3 electron.
2 electron.
4 electron.
Hợp chất ion thường có đặc điểm nào sau đây?
Dẫn điện ở trạng thái rắn.
Dễ tan trong dung môi hữu cơ.
Nhiệt độ nóng chảy và nhiệt độ sôi cao.
Khó tan trong nước.
Các hạt cấu tạo nên hầu hết các nguyên tử là
electron và proton.
electron, proton và neutron.
neutron và electron.
proton và neutron.
Hiện tượng hóa học là
Hiện tượng chất bến đổi mà vẫn giữ nguyên là chất ban đầu.
Nước hóa đá dưới 0 oC.
Hiện tượng chất biến đổi có tạo ra chất khác.
Cho đường hòa tan với nước muối.
Các đồng vị của cùng một nguyên tố hóa học là những nguyên tử có
cùng số proton nhưng khác nhau về số neutron.
cùng số neutron nhưng khác nhau về số proton.
cùng tổng số proton và neutron nhưng khác nhau về số electron.
cùng số electron nhưng khác nhau về tổng số proton và neutron.
Các chất trong dãy nào sau đây đều có liên kết ion?
KBr, MgO, K2O.
CH4, HBr, CO2.
H2O, K2O, CO2.
KBr, CS2, MgS.
Nguyên tử của nguyên tố X có cấu hình electron 1s22s22p4, nguyên tử của nguyên tố Y có cấu hình electron 1s1. Liên kết hoá học giữa nguyên tử X và nguyên tử Y thuộc loại liên kết
kim loại.
cho – nhận.
ion.
cộng hoá trị.
Phát biểu nào sau đây đúng?
Liên kết bội là liên kết đôi.
Liên kết bội có hai liên kết ().
Liên kết ba gồm 2 liên kết () và một liên kết ().
Liên kết đơn bao giờ cũng là liên kết ().
Dãy sắp xếp các chất theo chiều tính acid giảm dần từ trái sang phải
H3PO4, H2SiO3, H2SO4, HClO4.
H2SO4, H3PO4, HClO4, H2SiO3.
HClO4, H2SO4, H3PO4, H2SiO3.
H2SiO3, H3PO4, H2SO4, HClO4.
Cho các hydroxide: Mg(OH)2, Al(OH)3, KOH, NaOH. Dãy nào được sắp xếp theo chiều tăng dần tính base của chúng?
Al(OH)3 < Mg(OH)2 < NaOH < KOH.
Mg(OH)2 < Al(OH)3 < NaOH < KOH.
KOH < NaOH < Al(OH)3 < Mg(OH)2.
Al(OH)3 < NaOH < KOH < Mg(OH)2.
Cho các ion sau: K+, Na+, Mg2+, S2-,P3-, Ca2+. Số ion có 18 electron là
5.
3.
2.
4.
Phân tử sodium oxide được hình thành do sự kết hợp giữa
ion Na+ và ion O2-.
nguyên tử Na và nguyên tử O.
ion Na- và ion O+.
ion Na và ion O2-.
Dãy chất nào sau đây gồm các chất chỉ có liên kết cộng hoá trị phân cực?
H2O, HCl, NH3.
O2, H2O, NH3.
HCl, N2, H2S.
HCl, Cl2, H2O.
(0,75 điểm): Hoàn thành bảng sau cho H(Z=1), O(Z=8), C (Z=6), N(Z=7).
| Công thức phân tử | Công thức electron | Công thức Lewis |
| HCl | ||
| N2 | ||
| CO2 |
(0,75 điểm): Xác định vị trí của sulphur (S có Z=16) trong bảng tuần hoàn, viết công thức oxide cao nhất và công thức hydroxide của S?
(0,75 điểm): Vận dụng quy tắc octet để giải thích sự tạo thành liên kết ion trong phân tử calcium oxide (CaO). Biết Ca (Z = 20); H (Z = 8).
(0,75 điểm)
(a) Vì sao nước đá ở thể rắn lại nổi trong ly nước lỏng?
(b) Khối lượng phân tử (amu) của nước, ammonia (NH3) và methane (CH4) lần lượt bằng 18, 17 và 16. Nước sôi ở 100 oC, ammonia sôi ở –33,35 oC và methane sôi ở –161,58 oC. Giải thích vì sao các chất trên có khối lượng phân tử xấp xỉ nhau nhưng nhiệt độ sôi của chúng lại chênh lệch nhau?
Giải thích vì sao các chất trên có khối lượng phân tử xấp xỉ nhau nhưng nhiệt độ sôi của chúng lại chênh lệch nhau?








