Bộ 5 đề thi cuối kì 1 Hóa 10 Cánh diều (2022-2023) có đáp án - Đề 1
30 câu hỏi
Trong nguyên tử, các electron
không mang điện tích.
mang điện tích dương.
mang điện tích âm.
trung hòa về điện.
Nguyên tố hóa học là những nguyên tử có cùng
điện tích hạt nhân.
số khối.
khối lượng.
số neutron.
Nguyên tử có kí hiệu 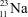 thì điện tích hạt nhân là
thì điện tích hạt nhân là
+11.
+23.
12+.
34+.
Li trong tự nhiên có 2 đồng vị: 3 7 L i (94% ); 3 6 L i (6% ). Nguyên tử khối trung bình của Li là
9,64.
6,94.
6,18.
13.
Kí hiệu nào trong số các kí hiệu của các phân lớp sau là sai?
4s, 4f.
2d, 3f.
2p, 3d.
1s, 2p.
Số electron tối đa có thể phân bố trên lớp M là
32.
18.
8.
16.
Sự phân bố electron trong một orbital dựa vào nguyên lí hay quy tắc nào sau đây?
Nguyên lí vững bền.
Quy tắc Hund.
Quy tắc Hund và nguyên lí Pauli.
Nguyên lí Pauli.
Số electron ở lớp ngoài cùng của nguyên tử các nguyên tố kim loại thường là
1, 2, 3 electron.
4 electron.
5, 6, 7 electron.
8 electron.
Nguyên tử của nguyên tố X có tổng số electron trên các phân lớp p là 10. Ở trạng thái cơ bản, nguyên tử X có số electron độc thân là
1.
2.
3.
4.
Các nguyên tố trong bảng tuần hoàn được sắp xếp theo nguyên tắc?
Tăng dần độ âm điện
Tăng dần bán kính nguyên tử
Tăng dần điện tích hạt nhân nguyên tử.
Tăng dần khối lượng
Số nguyên tố trong chu kì 3 và 5 là
8 và 18.
18 và 8.
8 và 8.
18 và 18.
Những nguyên tố khí hiếm có cấu hình electron chung là
ns1
ns2
ns2np5
ns2np6
Nguyên tố Y ở chu kì 3 nhóm IVA. Cấu hình electron nguyên tử của Y là
1s22s22p63s23p4.
1s22s22p63s23p2.
1s22s22p63s23p6.
1s22s22p63s23p63d24s2.
Hai nguyên tố X và Y là hai nguyên tố ở hai nhóm A kế tiếp nhau có tổng số hạt mang điện tích dương bằng 23 và cùng thuộc một chu kì. Vị trí của X và Y trong bảng tuần hoàn là
X thuộc chu kì 2 nhóm IIIA, Y thuộc chu kì 3 nhóm IIA.
X thuộc chu kì 3 nhóm IA, Y thuộc chu kì 2 nhóm IIIA.
X thuộc chu kì 2 nhóm VA, Y thuộc chu kì 3 nhóm VIA.
X thuộc chu kì 3 nhóm IA, Y thuộc chu kì 3 nhóm IIA.
Tính chất nào sau đây không biến đổi tuần hoàn?
bán kính nguyên tử.
số electron của nguyên tử
số electron lớp ngoài cùng
tính acid và base của các oxide và hidroxide tương ứng
Nguyên tử của nguyên tố nào sau đây có tính kim loại mạnh nhất ?
Potassium.
Sodium.
Caesium.
Fluorine.
Dãy nguyên tố nào sau đây được sắp xếp theo chiều giảm dần của tính phi kim?
8O, 9F, 7N, 6C.
9F, 8O, 7N, 6C.
9F, 7N, 8O, 6C.
7N, 9F, 8O, 6C.
Cho nguyên tố R thuộc nhóm IVA. Trong oxide cao nhất, R chiếm 46,67% về khối lượng. Số khối của R là
31.
28.
32.
14.
Oxide và hydroxide tương ứng của nguyên tố sulfur (Z=16) có tính chất gì?
Base mạnh.
Acid mạnh.
Base yếu.
Acid yếu.
Trong các hợp chất, các nguyên tử của nguyên tố nhóm IIA đã đạt được cấu hình bền của khí hiếm gần nhất bằng cách
cho 2 electron.
nhận 1 electron.
cho 1 electron.
nhận 2 electron.
Liên kết hoá học trong phân tử NaCl là
liên kết ion.
liên kết cộng hoá trị không phân cực.
liên kết cộng hóa trị phân cực.
liên kết cho − nhận
Liên kết ion tạo thành giữa hai nguyên tử
Kim loại điển hình.
Phi kim điển hình.
Kim loại và phi kim.
Kim loại điển hình và phi kim điển hình.
Cho các ion: Na+, Al3+, SO 4 2 − , NH 4 + , NO 3 − , Cl-, Mg2+. Hỏi có bao nhiêu anion?
2.
3.
4.
5.
Tổng số hạt electron trong ion SO42– là (Cho ZS=16; ZO=8)
26.
48.
50.
46.
Công thức cấu tạo đúng của N2 là
N≡N.
N=N.
N-N.
N:::N.
Liên kết cộng hóa trị phân cực là liên kết cộng hóa trị mà trong đó cặp electron chung
ở giữa 2 nguyên tử.
lệch về phía nguyên tử có độ âm điện lớn hơn.
có sự cho và nhận electron.
có sự tạo thành ion dương và ion âm.
Cho các chất: CH4, HCl, H2O, NH3. Hợp chất có độ phân cực mạnh yếu nhất là (Cho độ âm điện của H: 2,2; Cl: 3,16; C: 2,55; N: 3,04; O: 3,44)
CH4.
NH3.
H2O.
HCl.
Hợp chất nào sau đây tạo được liên kết hydrogen liên phân tử?
H2S.
PH3.
CH4.
H2O.
Nguyên tử Fe có kí hiệu 2 6 5 6 F e . Cho các phát biểu sau về Fe:
(1) Nguyên tử của nguyên tố Fe có 8 electron ở lớp ngoài cùng.
(2) Nguyên tử của nguyên tố Fe có 30 neutron trong hạt nhân.
(3) Fe thuộc chu kì 4, nhóm VIIIB.
(4) Fe là nguyên tố s.
(5) Ion Fe3+ không có cấu hình electron của khí hiếm gần nhất.
Trong các phát biểu trên, phát biểu đúng là
1.
2.
3.
4.
R, T, X, Y, Z lần lượt là năm nguyên tố liên tiếp trong bảng tuần hoàn, có tổng số hạt mang điện trong nguyên tử là 180. Kết luận nào sau đây đúng?
Năm nguyên tố này thuộc cùng một chu kì.
Nguyên tử của nguyên tố Z có bán kính lớn nhất trong số các nguyên tử của năm nguyên tố trên.
X là phi kim.
R thuộc nhóm VIA.








