Bộ 3 đề thi cuối kì 2 Hóa 10 Chân trời sáng tạo cấu trúc mới có đáp án - Đề 3
28 câu hỏi
PHẦN I. Câu trắc nghiệm nhiều phương án lựa chọn. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
Cho phản ứng tổng quát sau:
aA + bB → mM + nN
Tốc độ trung bình của phản ứng tính theo chất A là
\[\overline v = \frac{{\Delta {C_A}}}{{\Delta t}}.\]
\[\overline v = - \frac{{\Delta {C_A}}}{{\Delta t}}.\]
\[\overline v = \frac{1}{a}.\frac{{\Delta {C_A}}}{{\Delta t}}.\]
\[\overline v = - \frac{1}{a}.\frac{{\Delta {C_A}}}{{\Delta t}}.\]
Thông thường đối với các phản ứng có chất khí tham gia, khi tăng áp suất, tốc độ phản ứng
giảm.
không đổi.
tăng.
không xác định được.
Hình ảnh dưới đây minh họa ảnh hưởng của yếu tố nào tới tốc độ phản ứng: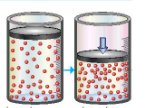
Diện tích bề mặt tiếp xúc.
Nhiệt độ.
Áp suất.
Chất xúc tác.
Khi cho cùng một lượng aluminium (Al) vào cốc đựng dung dịch acid HCl 0,1M, tốc độ phản ứng sẽ lớn nhất khi dùng nhôm ở dạng nào sau đây?
Dạng viên nhỏ.
Dạng bột mịn, khuấy đều.
Dạng tấm mỏng.
Dạng nhôm dây.
Cho phản ứng hóa học sau: C(s) + O2(g) → CO2(g)
Yếu tố nào sau đây không ảnh hưởng đến tốc độ phản ứng trên?
Nhiệt độ.
Nồng độ O2.
Hàm lượng carbon.
Diện tích bề mặt carbon.
Cho các phản ứng sau:
(a) 2Al(s) + Fe2O3(s) → Al2O3(s) + 2Fe(s).
(b) 2H2(g) + O2(g) → 2H2O(l).
(c) C(s) + O2(g) → CO2(g).
(d) CaCO3(s) + 2HCl(aq) CaCl2(aq) + H2O(l) + CO2(g).
Số phản ứng khi tăng áp suất của hệ phản ứng, tốc độ bị thay đổi là
1.
2.
3.
4.
Cho phản ứng \[3{O_2}(g) \to 2{O_3}(g)\]
Ban đầu nồng độ oxygen là 0,024M. Sau 5s thì nồng độ của oxygen là 0,02M. Tốc độ trung bình của phản ứng trên trong 5s đầu tiên là
2,67.104 M.
2,67.104 M/s.
2,67.10-4 M.
2,67.10-4 M/s.
Halogen nào sau đây ở điều kiện thường là chất rắn, có màu đen tím?
Chlorine.
Bromine.
Fluorine.
Iodine.
Phản ứng nào dưới đây sai?
2Fe + 3Cl2 2FeCl3.
H2 + I2 2HI.
Br2 + H2O ⇌ HBr + HBrO.
F2 + H2O ⇌ HF + HFO.
Phản ứng giữa đơn chất halogen nào sau đây với hydrogen diễn ra mãnh liệt, nổ ngay cả trong bóng tối hoặc ở nhiệt độ thấp?
I2.
F2.
Cl2.
Br2.
Số oxi hoá của fluorine trong hợp chất là
0.
-1.
+1.
+2.
Liên kết trong hợp chất hydrogen halide là
liên kết cộng hóa trị có cực.
liên kết cho – nhận.
liên kết ion.
liên kết cộng hóa trị không cực.
Hydrogen halide nào sau đây là chất khử phổ biến trong các phản ứng hoá học?
HF.
HI.
HBr.
HCl.
Kim loại nào sau đây không phản ứng với dung dịch HCl?
Mg.
Al.
Ag.
Fe.
Cho biết phản ứng tạo thành 2 mol HCl(g) ở điều kiện chuẩn sau đây tỏa ra 184,6 kJ: H2(g) + Cl2(g) → 2HCl(g) (*)
Cho các phát biểu sau:
(a) Nhiệt tạo thành chuẩn của HCl là –184,6 kJ/mol.
(b) Biến thiên enthalpy của phản ứng (*) là –184,6 kJ.
(c) Nhiệt tạo thành của HCl là –92,3 kJ/mol.
(d) Biến thiên enthalpy của phản ứng (*) là –92,3 kJ.
Số phát biểu đúng là
1.
2.
3.
4.
Cho sơ đồ chuyển hoá sau:
X(aq) →co mang ngandien phan dung dich Cl2(g) →to+FeY(s) →+NaOH Z(s).
Phát biểu nào sau đây là đúng?
X có thể tác dụng với dung dịch Fe2(SO4)3 tạo ra Y.
Y và Z có thể lần lượt là FeCl3 và Fe(OH)2.
X và Z không phản ứng với nhau.
X, Y và Z đều là hợp chất của chlorine.
Cho giá trị bán kính nguyên tử (pm) không theo thứ tự của các halogen (từ chu kì 2 đến chu kì 4): 94; 42; 79. Nguyên tố có bán kính nguyên tử 94 pm là
Fluorine.
Chlorine.
Bromine.
Iodine.
Để trung hòa 200 ml dung dịch NaOH 1M thì thể tích dung dịch HCl 0,5M cần dùng là
0,5 lít.
0,4 lít.
0,3 lít.
0,6 lít.
PHẦN II. Câu trắc nghiệm đúng sai. Thí sinh trả lời từ câu 1 đến câu 4. Trong mỗi ý a), b), c), d) ở mỗi câu, thí sinh chọn đúng hoặc sai. (Đ – S)
Phản ứng oxi hóa – khử là loại phản ứng xảy ra phổ biến trong tự nhiên, đời sống và sản xuất, trong phản ứng oxi hoá khử:
Chất khử là chất nhường electron.
Chất oxi hóa là chất nhận electron.
Quá trình oxi hóa là quá trình chất khử nhận electron.
Quá trình khử là quá trình chất oxi hóa nhường electron.
Ở áp suất 1 bar và nhiệt độ 25oC, phản ứng giữa 1 mol sulfur với oxygen xảy ra theo phương trình “S(s) + O2(g) → SO2(g)” và tỏa ra một lượng nhiệt là 296,9 kJ.
Biến thiên enthalpy chuẩn của phản ứng là 296,9 kJ.
Enthalpy tạo thành chuẩn của sulfur dioxide bằng -296,9 kJ mol-1.
Sulfur vừa có thể là chất khử vừa có thể là chất oxi hóa, tùy thuộc vào phản ứng mà nó tham gia.
0,5 mol sulfur tác dụng hết với oxygen giải phóng 148,45 kJ năng lượng dưới dạng nhiệt.
Tốc độ của một phản ứng hóa học:
là đại lượng đặc trưng cho sự thay đổi nồng độ của chất phản ứng hoặc sản phẩm trong một đơn vị thời gian.
được kí hiệu là n và có đơn vị là mol/L.
phụ thuộc vào nồng độ, áp suất, diện tích bề mặt, nhiệt độ và chất xúc tác.
là tốc độ tức thời của một phản ứng tại một thời điểm.
Nhóm VIIA trong bảng tuần hoàn các nguyên tố hóa học còn gọi là nhóm halogen, gồm 6 nguyên tố: fluorine (F); chlorine (Cl); bromine (Br); iodine (I); astatine (At) và tennessine (Ts). Bốn nguyên tố F, Cl, Br, I tồn tại trong tự nhiên; còn At và Ts là các nguyên tố phóng xạ.
Số oxi hóa của các halogen trong hợp chất là -1.
Nhiệt độ nóng chảy, nhiệt độ sôi giảm từ F2 đến I2
Liên kết trong phân tử hydrogen halide (HX) là liên kết cộng hóa trị.
Có thể phân biệt các ion F−; Cl−; Br−; I− trong dung bằng dung dịch silver nitrate.
Phần III. Câu hỏi trắc nghiệm yêu cầu trả lời ngắn. Thí sinh trả lời từ câu 1 đến câu 6.
Viết phương trình hoá học của phản ứng minh hoạ hiện tượng: nhỏ 1-2 giọt dung dịch hydrochloric acid vào mẩu đá vôi thấy xuất hiện sủi bọt khí.
Hình vẽ dưới đây mô tả thí nghiệm điều chế và thu khí chlorine trong phòng thí nghiệm. Vai trò của bình chứa dung dịch NaCl và bông tẩm dung dịch NaOH lần lượt là?
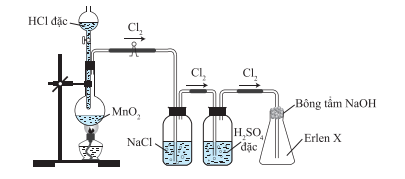
Viết 1 phương trình hoá học chứng minh chlorine vừa có tính oxi hoá, vừa có tính khử.
Cho 24,48 gam hỗn hợp X gồm (Fe, Zn, Al) tác dụng với dung dịch HCl dư thu được 0,54 mol khí H2. Mặt khác, 0,24 mol X tác dụng vừa đủ với 0,33 mol khí chlorine (nung nóng). Xác định khối lượng mỗi kim loại trong 24,48 gam X.
Cho m gam KClO3 tác dụng với HCl đến khi phản ứng xảy ra hoàn toàn thấy thoát ra V lít khí Cl2 ở đkc. Biết lượng Cl2 sinh ra phản ứng vừa đủ với 0,56 gam Fe. Xác định m và V.
Dẫn một lượng dư khí chlorine vào dung dịch chứa hỗn hợp muối NaBr và KBr sau phản ứng thu được hỗn hợp hai muối, đồng thời thấy khối lượng muối giảm 4,45 gam.
Tính số mol chlorine đã tham gia phản ứng.








