Đề thi thử Tốt nghiệp THPT 2025 - Cấu trúc mới - Môn Hóa Học - Đề 5
40 câu hỏi
Tiến hành thí nghiệm (như hình vẽ): Rót dung dịch NaCl bão hòa vào cốc 1, cốc 2, cốc 3; cho dầu nhờn vào cốc 4. Cho vào cốc 1 và cốc 4 một đinh sắt sạch, cho vào cốc 2 đinh sắt sạch được quấn bởi dây Zn, cho vào cốc 3 đinh sắt sạch được quấn bởi dây Cu. Để 4 cốc trong không khí khoảng 5 ngày.
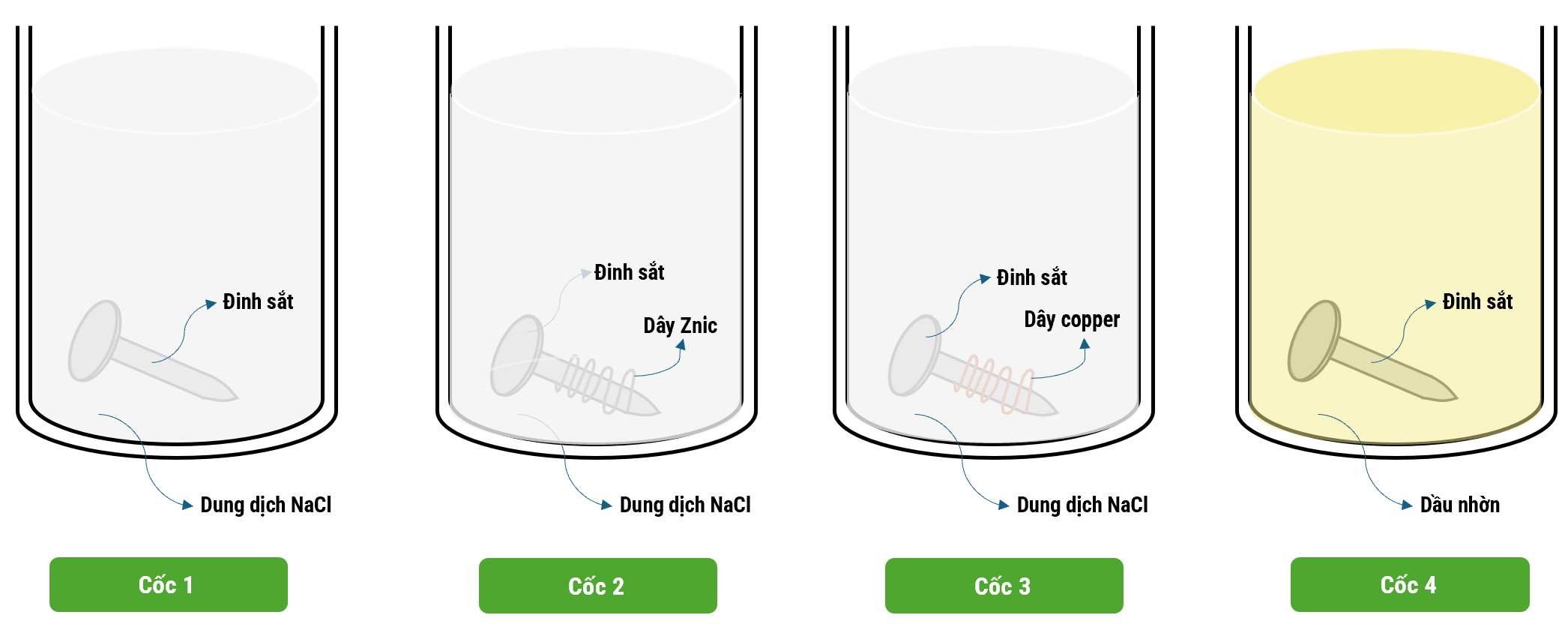
Cho các phát biểu về hiện tượng quan sát được trong 4 cốc như sau:
(1). Ở cốc 4, đinh sắt không bị gỉ (không bị ăn mòn).
(2). Ở cốc 2, đinh sắt không bị gỉ, dây Zn bị ăn mòn và có khí thoát ra.
(3). Ở cốc 3, đinh sắt bị gi nhiều nhất và dây đồng không bị ăn mòn.
(4). Ở cốc 1, đinh sắt bị gỉ và dung dịch có màu vàng của FeCl2
Số phát biểu đúng là
1.
2.
3.
4.
Ở một số quốc gia, khoáng vật trona là nguyên liệu chính để sản xuất soda. Thành phần hóa học chính của trona là
3NaF.AlF3.
NaCl.KCl.
Na2CO3.NaHCO3.2H2O.
NaNO3.
Hình dưới đây là ký hiệu của 6 polymer nhiệt dẻo phổ biến có thể tái chế:
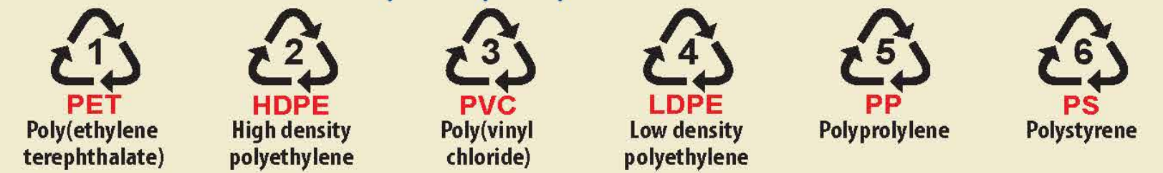
Các ký hiệu này thường được in trên bao bì, vỏ hộp, đồ dùng,…để giúp nhận biết vật liệu polymer cũng như thuận lợi cho việc thu gom, tái chế. Polymer có ký hiệu số 5 được điều chế bằng phản ứng trùng hợp monomer nào dưới đây?
CH2=CH2.
CH2=CH–CH3.
CH2=CH–C6H5.
CH2=CH–Cl.
Hình dưới đây mô tả tính chất vật lí nào của kim loại? (hình tròn to mô tả ion kim loại, hình tròn nhỏ mô tả electron tự do) 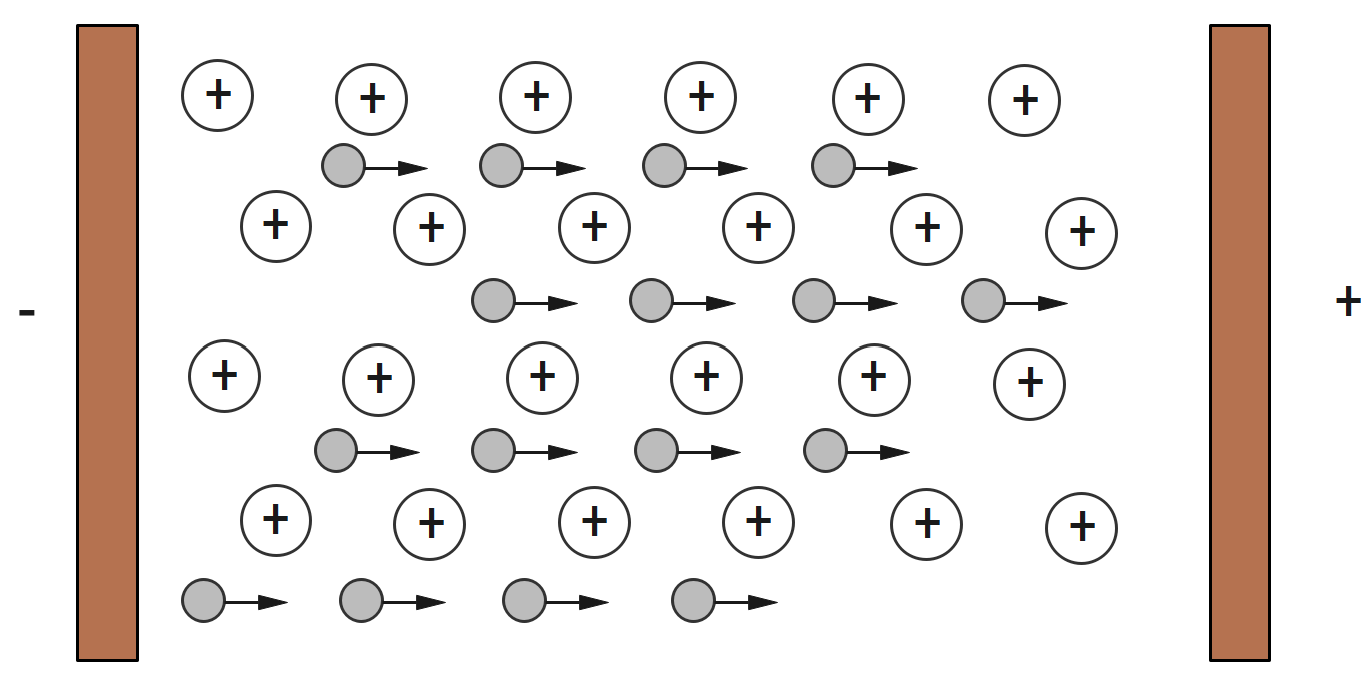
Tính dẻo.
Tính dẫn điện.
Tính dẫn nhiệt.
Tính cứng.
X và Y là các hợp chất vô cơ của một kim loại kiềm, có nhiều ứng dụng trong thực tế và khi đốt nóng ở nhiệt độ cao trên đèn khí cho ngọn lửa màu vàng.
Biết chúng thoả mãn các phương trình sau:
+ X tác dụng NaOH sẽ tạo thành Y và H₂O;
+ Nung nóng X thì sẽ cho sản phẩm là Y, khí và H2O
Công thức của hợp chất Y là
NaOH.
K2CO3.
Na2CO3.
NaHCO3.
Cách nào sau đây không sử dụng để làm mềm nước có tính cứng vĩnh cửu?
Dùng dung dịch Na2CO3.
Đun sôi nước.
Dùng dung dịch Na3PO4.
Dùng phương pháp trao đổi ion.
Điểm chớp cháy là nhiệt độ thấp nhất ở áp suất của khí quyển mà một chất lỏng hoặc vật liệu dễ bay hơi tạo thành lượng hơi đủ để bốc cháy trong không khí khi tiếp xúc nguồn lửa.
- Điểm chớp cháy được sử dụng để phân biệt chất lỏng dễ cháy với chất lỏng có thể gây cháy:
+ Chất lỏng có điểm chớp cháy <37,8oC gọi là chất lỏng dễ cháy.
+ Chất lỏng có điểm chớp cháy >37,8oC gọi là chất lỏng có thể gây cháy.
Cho bảng số liệu sau:
Nhiên liệu | Điểm chớp cháy (℃) | Nhiên liệu | Điểm chớp cháy (℃) |
Propane | –105 | Ethylene glycol | 111 |
Pentane | –49 | Diethyl ether | –45 |
n–Hexane | –22 | Acetaldehyde | –39 |
Ethanol | 13 | Stearic acid | 196 |
Methanol | 11 | Trimethylamine | –7 |
Số chất lỏng dễ cháy trong bảng trên là
6.
7.
8.
9.
Trong nông nghiệp, nếu bón nhiều phân superphosphate đơn sẽ làm đất chai cứng. Chất nào sau đây trong phân superphosphate đơn là nguyên nhân chính gây nên hiện tượng chai cứng đất?
Ca(H₂PO₄)₂.
Ca(H₂PO₄)₂ + CaSO₄.
CaSO₄.
Ca₃(PO₄)₂.
Cho biểu đồ nhiệt độ sôi (°C) của một số chất như sau:
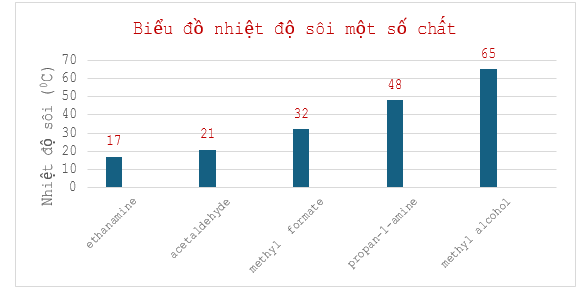
Số chất tồn tại dạng khí ở điều kiện chuẩn (25 °C, 1 bar) là
1.
2.
4.
5.
Heptanoic acid được ứng dụng trong mĩ phẩm, nước hoa và các ứng dụng tạo mùi thơm. Phổ hồng ngoại của heptanoic acid như sau:
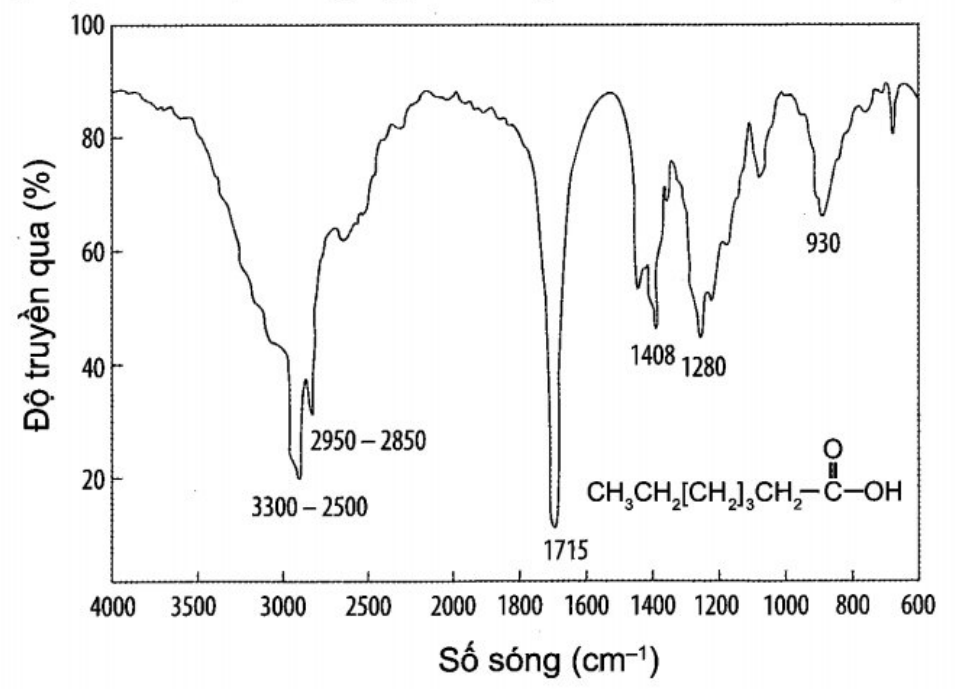
Peak nào giúp dự đoán được trong hợp chất này có nhóm chức carboxyl?
peak 3300-2500 cm-1.
peak 2950-2850 cm-1.
peak 1715 cm-1.
peak 1408 cm-1.
Palmitic acid là một acid béo bão hoà phổ biến trong động vật và thực vật. Công thức nào sau đây là của palmitic acid?
C17H33COOH.
НСООН.
C15H31COOH.
CH3COOH
Trong y học, dung dịch glucose 5% (G-5) là dịch truyền tĩnh mạch cho những trường hợp bệnh nhân thiếu nước và năng lượng theo chỉ định của bác sĩ. Một chai chứa 600 gam dịch truyền G-5 cung cấp được tối đa m kJ năng lượng. Giá trị của m là (Biết 1 g glucose có thể cung cấp 10 kJ năng lượng).
500.
300.
400.
200.
Ethylene là một trong những hóa chất quan trọng, có nhiều ứng dụng trọng đời sống: kích thích quả mau chín, điều chế nhựa làm sản phẩm gia dụng,… Phản ứng hóa học của ethylene với dung dịch Br2 như sau:
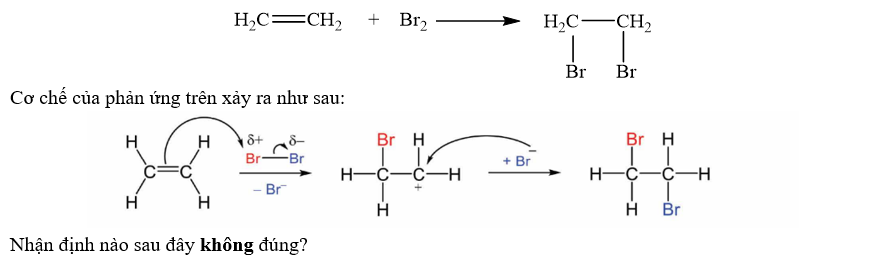
Phản ứng trên thuộc loại phản ứng cộng.
Giai đoạn 1, liên kết đôi phản ứng với tác nhân Br−δtạo thành phần tử mang điện dương.
Giai đoạn 2, phần tử mang điện dương kết hợp với anion Br−tạo thành sản phẩm.
Hiện tượng của phản ứng là dung dịch bromine bị mất màu.
Ester X được tạo bởi methyl alcohol và acetic acid. Công thức của X là
HCOOC2H5.
CH3COOC2H5.
CH3COOCH3.
HCOOCH3
Insulin là hocmon có tác dụng điều tiết lượng đường trong máu. Thủy phân một phần insulin thu được heptapeptide X mạch hở. Khi thủy phân không hoàn toàn X, thu được hỗn hợp chứa các peptide:
Phe-Phe-Tyr, Pro-Lys-Thr, Tyr-Thr-Pro, Phe-Tyr-Thr. Nếu đánh số thứ tự đầu N là số 1, thì amino acid ở vị trí số 5 trong X có kí hiệu là
Thr.
Pro.
Tyr.
Lys.
Tùy thuộc vào pH của dung dịch, alanine tồn tại một số dạng như sau:
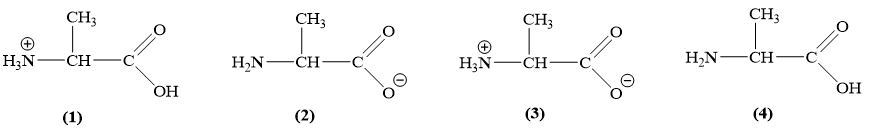
Khi pH = 11 thì alanine sẽ tồn tại dạng nào trong các dạng trên? Cho biết pHI của alanine là 6,01.
(l).
(2).
(3).
(4).
Cho thế điện cực chuẩn của các cặp oxi hóa – khử sau: EMnO4−/Mn2+o=+1,51 V và EFe3+/Fe2+o=+0,77 V
Phát biểu nào sau đây sai?
Ion MnO4- có tính oxi hóa mạnh hơn Fe3+.
Ion Fe2+ có thể bị oxi hóa bởi ion MnO4-.
Khi cho Fe(NO3)3 vào dung dịch KMnO4, quá trình oxi hóa xảy ra là: Fe3+(aq)+1e→Fe2+(aq).
ion MnO4- có khả năng oxi hóa ion Fe2+ trong dung dịch thành ion Fe3+.
Điện phân dung dịch CuSO4 với điện cực Pt. Theo thời gian, màu xanh của dung dịch CuSO4 nhạt dần và mất hẳn đồng thời có khí thoát ra ở 2 điện cực. Khí thoát ra ở cathode và anode lần lượt là
O2 và H2.
H2 và O2.
SO2 và O2.
H₂ và SO2.
PHẦN II. Thí sinh trả lời từ câu 1 đến câu 4 . Trong mỗi ý a), b), c), d) ở mỗi câu, thí sinh chọn đúng hoặc sai.
Thí nghiệm điện phân dung dịch copper (II) sulfate với các điện cực trơ (graphite) được mô phỏng như hình vẽ sau đây:
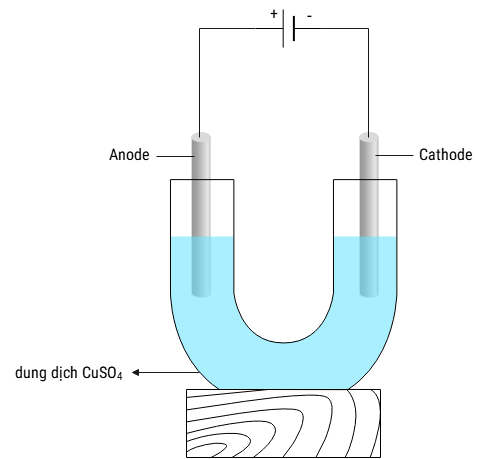
a. Tại anode, xuất hiện bọt khí hydrogen trên bề mặt điện cực.
b. Tại cathode, trước tiên xảy ra sự oxi hóa nước sau đó xảy ra tiếp sự oxi hóa Cu2+.
c. Dung dịch sau điện phân có giá trị pH tăng lên.
d. Nếu tiến hành điện phân dung dịch chứa 0,15 mol copper (II) sulfate trong thời gian 38 phút 36 giây với cường độ dòng điện 10A thì khối lượng dung dịch sau phản ứng giảm là 9,6 gam .
Theo Tiêu chuẩn Việt Nam TCVN 7624 : 2007, khi chế tạo gương, chiều dày lớp bạc (siliver) phủ trên bề mặt tấm kính (quy ra tổng lượng bạc trên một đơn vị m2 kính) phải đạt tối thiểu 0,7 g.m-2. Một công ty cần sản xuất 30000 m2 gương có độ dày lớp bạc (siliver) phủ ở mức 0,72 g.m-2. Để tạo ra bạc (siliver), người ta tiến hành theo sơ đồ phản ứng như sau:
Saccharose →+H2O (xt H+; t0)Dung dịch A →trung hòa acidDung dịch B →+d d [Ag(NH3)2]OH; t0 du Ag.
Biết hiệu suất cả quá trình là 80%.
Cho các phát biểu sau:
a. Lượng bạc được tráng lên 30000m2 gương với độ dày lớp bạc (siliver) phủ ở mức 0,72 g.m-2 là 21,6 kg.
b. Trong dung dịch A có hai loại monosaccharide.
c. Trong quá trình thủy phân saccharose có thể thay xúc tác acid bằng xúc tác base.
d. Để sản xuất lượng gương với độ phủ bạc như trên, công ty đó cần sử dụng lượng saccharose ít nhất là 21,375 kg.
Khảo sát một số tính chất của 3 chất X, Y, Z được ghi lại trong bảng sau:
| Nhiệt độ nóng chảy (oC) | Quỳ tím |
X | -6,3 | Không đổi màu |
Y | 233 | Không đổi màu |
Z | 247 | Màu hồng |
Biết X, Y, Z là một trong 3 chất: Glycine, Aniline, Glutamic acid. Cho các phát biểu sau :
a. Dựa vào nhiệt độ nóng chảy thì chất Y, Z là chất rắn ở nhiệt độ thường.
b. Tên bán hệ thống của glutamic acid là α–amino pentane-1,5-dioic.
c. X, Y, Z lần lượt là Aniline, Glycine, Glutamic acid.
d. Nếu hexapeptide T được tạo bởi Y và Z có phân tử khối là 504 amu thì số gốc Glu trong peptide là 4.
Hai ống nghiệm (1) và (2) đều chứa 1 mL dung dịch copper(II) sulfate 0,5% màu xanh nhạt. Tiến hành hai thí nghiệm sau ở 20 °C:
Thí nghiệm 1: Thêm từ từ cho đến hết 2 mL dung dịch hydrochloric acid đặc (nồng độ khoảng 11 M) không màu vào ống nghiệm (1) thu được dung dịch có màu vàng chanh, do có quá trình:
[Cu(OH2)6]2+(aq) + 4Cl−(aq) ⇌ [CuCl4]2−(aq) + 6H2O(l) KC = 4,18.105
Thí nghiệm 2: Thêm từ từ cho đến hết 2 mL dung dịch sodium chloride bão hòa (nồng độ khoảng 5,3 M) không màu vào ống nghiệm (2) thu được dung dịch có màu xanh nhạt hơn so với ban đầu.
Cho các phát biểu sau:
a. Trong thí nghiệm 1, phức chất [Cu(OH2)6]2+ bền hơn phức chất [CuCl4]2−.
b. Khi cho dung dịch HCl có nồng độ khoảng 5,3 M vào dung dịch copper(II) sulfate 0,5% thì không quan sát thấy dấu hiệu của phản ứng tạo phức chất [CuCl4]2−.
c. Biểu thức tính hằng số cân bằng của phản ứng ở thí nghiệm 1 là: KC=[[CuCl4]2−(aq)].[H2O(l)]6[[Cu(OH2)6]2+(aq)].[Cl−(l)]4
d. Trong thí nghiệm 2, không có dấu hiệu của phản ứng hình thành phức chất.
PHẦN III. Thí sinh trả lời từ câu 1 đến câu 6 .
Một chiếc khuyên tai dạng đĩa tròn mỏng có đường kính 5,00 cm được mạ với lớp phủ Au dày 0,02 mm từ dung dịch Au3+.
Cho: - Khối lượng riêng của Au là D = 19,7 g/cm3, π=3,14.
- F = 96500 C/mol; I = 0,10 A.
Thời gian để mạ vàng cho chiếc khuyên tai là bao nhiêu giờ? (làm tròn đến hàng phần trăm)
Chất béo triolein(C17H33COO)3C3H5) là chất béo thường ở thể lỏng vì trong phân tử chất béo chứa nhiều gốc acid béo không no.Vậy trong chất béo triolein có chứa mấy liên kết π trong phân tử.
Cho các carbohydrate sau: glucose, fructose, saccharose và maltose. Có bao nhiêu carbohydrate có khả năng mở vòng trong dung môi nước?
Hợp chất hữu cơ X (C8H15O4N) tác dụng với dung dịch NaOH dư, đun nóng, thu được sản phẩm hữu cơ gồm muối disodium glutamate và alcohol. X có bao nhiêu công thức cấu tạo thỏa mãn?
Các muối carbonate của kim loại nhóm IIA đều bị phân hủy bởi nhiệt:
MCO3(s) → MO (s) + CO2 (g) ΔrH298o
Biến thiên enthalpy chuẩn của quá trình trên được cho trong bảng sau:
Muối | MgCO3 (s) | CaCO3 (s) | SrCO3 (s) | BaCO3 (s) |
ΔrH298o (kJ) | 100,70 | 179,20 | 234,60 | 271,50 |
Để sản xuất 1 tấn vôi bột theo phương pháp thủ công, người ta nung đá vôi (có hàm lượng CaCO3 là 72%, còn lại là tạp chất trơ) với than đá (giả sử chỉ chứa carbon và tạp chất trơ).
Biết ΔrH298o(CO2) = -393,50 kJ/mol. Tính thể tích khí CO2 tối thiểu đã thải ra môi trường ở điều kiện chuẩn (làm tròn đáp án đến hàng phần mười)
Để xác định hàm lượng muối Fe(II) trong 1 mẫu dung dịch A có thể dùng dung dịch thuốc tím KMnO4, phương trình ion như sau:
MnO4−+5Fe2++8H+→Mn2++5Fe3++4H2O
+ Người ta lấy 25,00 mL dung dịch A cho vào bình định mức, thêm nước cất cho đủ 100 mL, dung dịch thu được gọi là dung dịch X.
+ Lấy 10,00 mL từ dung dịch X chuyển vào bình tam giác. Thêm khoảng 5mL dung dịch H2SO4 2M.
+ Tiến hành chuẩn độ 3 lần bằng dung dịch KMnO4 0,02M.
Kết quả thể tích KMnO4 sau 3 lần chuẩn độ lần lượt là 20,50 mL; 20,55 mL; 20,55 mL. Tính hàm lượng muối Fe2+ (g/L) trong dung dịch A (làm tròn đáp án đến hàng phần mười)








