Đề minh họa tốt nghiệp THPT môn Hóa có đáp án năm 2025 (Đề 10)
40 câu hỏi
PHẦN I. Câu trắc nghiệm nhiều phương án lựa chọn. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
Kim loại nào sau đây là kim loại kiềm?
K.
Cu.
Fe.
Ca.
Kim loại nào sau đây có nhiệt độ nóng chảy thấp nhất?
Ag.
Hg.
W.
Cr.
Chất nào sau đây thuộc loại polysaccharide?
Maltose.
Saccharose.
Fructose.
Cellulose.
Chất nào sau đây là amine bậc một?
C2H5OH.
CH3NHC2H5.
H2NCH2COOH.
C2H5NH2
Trong công nghiệp, quặng bauxite dùng để sản xuất kim loại nhôm. Thành phần chính của quặng bauxite là
Al2O3.2H2O.
FeS2.
Fe2O3.2H2O.
AlOH3.2H2O.
Chất nào sau đây có tính chất lưỡng tính?
Na2SO4.
NaOH.
KHCO3.
Na2CO3.
Để làm mềm một loại nước có tính cứng tạm thời ta dùng hóa chất nào sau đây?
HCl.
Na3PO4.
NaNO3.
NaCl.
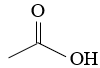
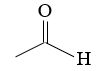
Cho chất X tác dụng với NaOH, thu được CH3COONa và H2O. Chất X có công thức cấu tạo là
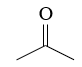
![]()
Triolein là chất béo có trong dầu lạc, dầu vừng, dầu cọ. Công thức cấu tạo của trioelin là
C17H31COO3C3H5.
C17H33COO3C3H5.
C17H35COO3C3H5.
C15H31COO3C3H5.
Trong dung dịch, ion nào sau đây oxi hóa được kim loại Cu?
Zn2+.
Fe2+.
Ag+.
Mg2+.
Kim loại Li nên được bảo quản trong
dầu hoả khan.
phenol.
khí trơ.
bình hút ẩm.
Polypropylene (hay PP) là chất dẻo thường được sử dụng để sản xuất các sản phẩm thiết bị y tế, đồ gia dụng,... PP được tổng hợp từ monomer nào sau đây?
CH2=CH2.
CH2=CHCN.
CH2=CHCH3.
CH2=CHCl.
Nhận định nào sau đây là sai?
Poly(phenol formaldehyde) được dùng làm chất dẻo.
Ethylamine tác dụng với nitric acid thu được ethyl alcohol và khí nitrogen.
Cho giấm ăn vào dung dịch albumin sẽ xảy ra đông tụ protein.
Hemoglobin là protein dạng hình cầu, tan được trong nước.
Cho sơ đồ chuyển hóa:
BaO→X→BaCO3→Y→BaCO3.
Biết mỗi mũi tên ứng với một phương trình hóa học của phản ứng xảy ra. Các chất X, Y thỏa mãn sơ đồ trên lần lượt là
BaCl2, BaSO4.
Ba(OH)2, BaSO4.
BaCl2, BaOH2.
BaOH2, BaHCO32.
Cho các polymer sau: polyethylene, polybuta-1,3-diene, poly(vinyl chloride), poly(hexamethylene adipamide), poly(methyl metacrylate). Số polymer dùng làm chất dẻo là
2.
5.
4.
3.
Cho các phát biểu sau:
(a) Dùng dung dịch HCl để rửa sạch aniline dính trong ống nghiệm.
(b) Trong cơ thể, chất béo bị oxi hóa chậm thành carbon dioxide, nước và cung cấp năng lượng cho cơ thể.
(c) ω-aminoenanthic acid có khả năng trùng ngưng tạo polymer.
(d) Ở nhiệt độ thấp 0–5oC, aniline tác dụng được với nitrous acid.
(e) Các tetrapeptide đều cho được phản ứng màu biuret.
Số phát biểu đúng là
2.
5.
3.
4.
Trong phòng thí nghiệm, một bạn học sinh khi nhỏ từ từ dung dịch thuốc tím vào dung dịch Fe2+ trong môi trường acid đã quan sát thấy thuốc tím mất màu và dung dịch chuyển dần từ không màu sang màu vàng nhạt. Phản ứng được thực hiện ở điều kiện chuẩn. Phương trình hóa học xảy ra trong thí nghiệm trên là
5Fe2+aq + MnO4−aq + 8H+aq→Mn2+aq + 5Fe3+aq + 4H2Ol
Cho các phát biểu sau:
(a) Màu vàng nhạt là màu của ion Mn2+.
(b) Chất oxi hóa trong phản ứng trên là Fe2+.
(c) Hai cặp oxi hóa - khử liên quan đến phản ứng trên là H+/H2O và Fe3+/Fe2+.
(d) Thế điện cực chuẩn của cặp MnO4−/Mn2+ lớn hơn cặp Fe3+/Fe2+.
Số phát biểu đúng là
2.
1.
3.
4.
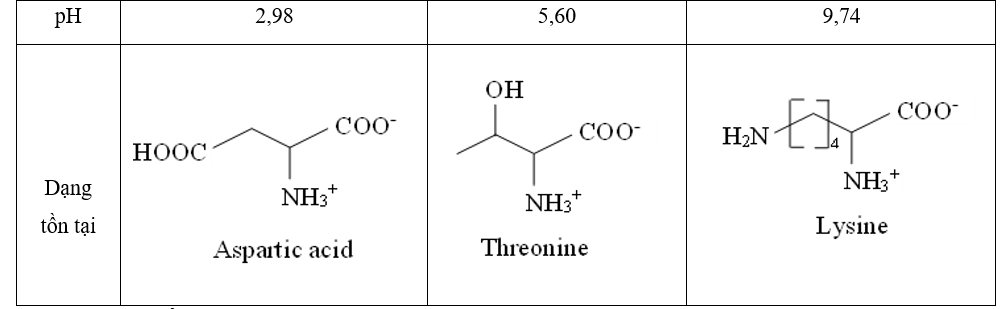
Với mỗi môi trường pH khác nhau, các amino acid tồn tại ở các dạng như sau:
Cho các phát biểu sau:
(a) Với môi trường pH = 2,98 thì threonine tồn tại chủ yếu dưới dạng cation.
(b) Với môi trường pH = 5,60 thì aspartic acid tồn tại chủ yếu dưới dạng anion.
(c) Với môi trường pH = 5,60 thì lysine tồn tại chủ yếu dưới dạng anion.
(d) Với môi trường pH = 9,74 thì aspartic acid bị di chuyển về phía cực dương của điện trường.
Số nhận định đúng là
4.
1.
3.
2.
PHẦN II. Câu trắc nghiệm đúng sai. Thí sinh trả lời từ câu 1 đến câu 4. Trong mỗi ý a), b), c), d) ở mỗi câu, thí sinh chọn đúng hoặc sai.
Eicosapentaenoic acid (EPA) là loại acid béo quan trọng cho sức khỏe con người, được tìm thấy nhiều trong cá hồi. Công thức cấu tạo của EPA như sau:
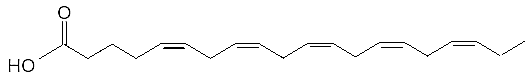
a). EPA là acid béo thuộc nhóm omega-6.
b). EPA có phân tử khối là 320.
c). Triglyceride được tạo bởi EPA và glycerol có dạng lỏng ở nhiệt độ thường.
d). Trong phân tử của EPA có 6 liên kết pi (π).
Pin Galvani được tạo nên từ hai cặp oxi hoá – khử Fe2+/Fe và Cu2+/Cu. Biết EFe2+/Feo=−0,44V và ECu2+/Cuo=+0,34V.
a). Phản ứng xảy ra trong pin: Cu s+ Fe2+aq→Cu2+aq+ Fes.
b). Fe đóng vai trò là cực âm (anode) của pin.
c). Khi pin hoạt động, ở cực âm, Fe sẽ nhường electron chuyển thành Fe2+ tan vào trong dung dịch; ở cực dương, ion Fe2+ sẽ nhận electron chuyển thành Fe.
d). Sức điện động chuẩn của pin bằng +1,56V.
Alcohol là loại hợp chất hữu cơ có nhiều ứng dụng: ethanol là chất dùng để sản xuất ethylene glycol, glycerol dùng làm chất chống đông động cơ ô tô ở các nước xứ lạnh, làm dung môi; sản xuất đồ uống có cồn,...
a). Alcohol no, đơn chức, mạch hở có công thức phân tử chung CnH2n+2O, n≥1.
b). Trong phòng thí nghiệm, có thể điều chế một lượng nhỏ ethylene bằng cách đun ethyl alcohol với dung dịch sulfuric acid đặc ở 170 °C.
c). Alcohol bậc hai bị oxi hoá không hoàn toàn thành hợp chất aldehyde.
d). Hợp chất no, mạch hở X có phần trăm khối lượng carbon, hydrogen và oxygen lần lượt bằng 37,5%, 12,5% và 50,0% là alcohol.
Các muối carbonate của kim loại nhóm IIA đều bị phân hủy bởi nhiệt:
MCO3s→toMOs + CO2g ΔrH2980
Biến thiên enthalpy chuẩn của quá trình trên được cho trong bảng sau:
Muối | MgCO3 (s) | CaCO3 (s) | SrCO3 (s) | BaCO3 (s) |
ΔrH2980 (kJ) | 100,7 | 179,2 | 234,6 | 271,5 |
Nhiệt độ bắt đầu xảy ra phản ứng nhiệt phân (sắp xếp ngẫu nhiên) các muối carbonate là 882oC; 1360oC; 542oC; 1155oC.
a). Độ bền nhiệt của các muối giảm dần từ MgCO3 đến BaCO3.
b). Các phản ứng nhiệt phân trên đều là phản ứng thu nhiệt.
c). Ở nhiệt độ 1360oC, phản ứng nhiệt phân BaCO3 bắt đầu xảy ra.
d). Nung hỗn hợp gồm MgCO3 và SrCO3 ở 880oC thu được hỗn hợp rắn gồm MgO và SrO.
PHẦN III. Câu trắc nghiệm yêu cầu trả lời ngắn. Thí sinh trả lời từ câu 1 đến câu 6.
Xét phản ứng của acetone với iodine:
CH3COCH3 + I2 →CH3COCH2I + HI
Phản ứng có hệ số nhiệt độ γ trong khoảng từ 30oC đến 50oC là 2,5. Nếu ở 35oC, phản ứng có tốc độ 0,036 mol/(L.h) thì ở 45oC, phản ứng có tốc độ là bao nhiêu mol/(L.h)?
Cho các dung dịch sau: albumin, ethylamine, fructose, saccharose. Có bao nhiêu dung dịch hòa tan đượcCuOH2 ?
Số hợp chất hữu cơ X đơn chức, mạch hở có công thức phân tử C4H8O2 tác dụng được với dung dịch NaOH, đun nóng là bao nhiêu?
Cho 15 mL dung dịch HNO3xM tác dụng với lượng dư dung dịch KI. Lượng I2∩i=1nXi sinh ra phản ứng vừa đủ với 12 mL dung dịch Na2S2O30,15M. Biết các phương trình phản ứng xảy ra như sau:
KI + HNO3→KNO3+ NO + I2+ H2O
I2+ Na2S2O3→NaI + Na2S4O6
Các phản ứng xảy ra hoàn toàn. Giá trị của x là bao nhiêu?
Một nhà máy sản xuất túi nilon tử PE cần sản xuất túi đựng hình chữ nhật có kích thước là 20 × 30 cm (hình dưới), bề dày của lớp nylon là 0,02 cm. Biết hiệu suất phản ứng trùng hợp ethylene để điều chế PE là 60%, quá trình chuyển nhựa thành túi có hiệu suất là 95% và biết khối lượng riêng của nhựa PE là 0,95g/cm3. Tính khối lượng nguyên liệu ethylene dùng để sản xuất đơn hàng 100 000 túi trên (đơn vị: tấn).
Dung dịch X gồm CuSO4 và NaCl. Tiến hành điện phân dung dịch X với điện cực trơ, màng ngăn xốp, cường độ dòng điện 0,5A, hiệu suất điện phân là 100%. Lượng khí sinh ra từ bình điện phân và lượng kim loại Cu sinh ra ở catot theo thời gian điện phân được cho như ở bảng sau:
Thời gian điện phân (giây) | t | t + 17370 | 3t |
Lượng khí sinh ra từ bình điện phân (mol) | a | a + 0,075 | 4,5a |
Lượng kim loại Cu sinh ra ở catot (mol) | 0,06 | 0,075 | 0,075 |
Số mol NaCl trong X là bao nhiêu?








