Bộ 5 đề thi giữa kì 1 Hóa 11 Kết nối tri thức (2023-2024) có đáp án - Đề 5
31 câu hỏi
Cho phản ứng: Fe2O3 (r) + 3CO (g) 2Fe (r) + 3CO2 (g). Khi tăng áp suất của phản ứng này thì
phản ứng dừng lại
cân bằng không bị chuyển dịch
cân bằng chuyển dịch theo chiều thuận
cân bằng chuyển dịch theo chiều nghịch
Khi tác dụng với chất nào sau đây, thể hiện tính oxy hóa
e O
e 2 O 3
e ( O H ) 3
Trong dung dịch nước của acetic acid (CH3COOH) tồn tại cân bằng sau
CH3COOH + H2O CH3COO- + H3O+
Trong phản ứng thuận, theo thuyết Bronsted – Lowry phần tử đóng vai trò base là
2O
CH3COOH
3O+
CH3COO-
Theo thuyết Brønsted – Lowry chất(ion) nào dưới đây là base?
2SO4.
NH3.
.
HClO.
Phản ứng tổng hợp ammonia là : N2(g) + 3H2(g) 2NH3(g) = –92kJ
Yếu tố không giúp tăng hiệu suất tổng hợp ammonia là :
Lấy ammonia ra khỏi hỗn hợp phản ứng.
Tăng nhiệt độ.
Bổ sung thêm khí nitrogen vào hỗn hợp phản ứng.
Tăng áp suất.
Cho cân bằng: 2SO2 (g) + O2 (g) 2SO3 (g). Khi tăng nhiệt độ thì tỉ khối của hỗn hợp khí so với H2 giảm đi. Phát biểu đúng khi nói về cân bằng này là:
Phản ứng nghịch toả nhiệt, cân bằng dịch chuyển theo chiều thuận khi tăng nhiệt độ.
Phản ứng thuận thu nhiệt, cân bằng dịch chuyển theo chiều nghịch khi tăng nhiệt độ.
Phản ứng thuận toả nhiệt, cân bằng dịch chuyển theo chiều nghịch khi tăng nhiệt độ.
Phản ứng nghịch thu nhiệt, cân bằng dịch chuyển theo chiều thuận khi tăng nhiệt độ.
Tính base của ammonia được thể hiện qua phản ứng nào sau đây
2NH3 + 3CuO 3Cu + 2N2↑ + 3H2O
NH3 (g) + HCl (g) → NH4Cl (s)
4NH3 + 3O2 2N2 + 6H2O
4NH3 + 5O2 4NO + 6H2O
Hợp chất nào của nitrogen không được tạo ra khi cho HNO3 tác dụng với kim loại?
NO.
NH4NO3.
NO2
N2O5.
Chất nào sau đây là acid theo Bronsted
CO32-
SO42-
2SO4
Na+
Trong phân tử HNO3,nguyên tử N có số oxi hóa là
+5
+4
-3
+3
Một dung dịch có pH = 12. Môi trường của dung dịch là
trung tính
không xác định
base
acid
Ba(NO3)2 là chất điện li mạnh. Nồng độ mol của ion trong dung dịch Ba(NO3)2 0,01 M là
0,25M
0,005M
0,05M
0,02M
Chuẩn độ 100,0 mL dung dịch NaOH 0,1M bằng dung dịch HCl 1,0 M. Thể tích dung dịch HCl cần thêm để dung dịch thu được có pH = 12 là
8,91 mL.
8,72 mL.
9,01 mL.
8,52 mL.
Chất nào sau đây là chất điện li?
CH4.
Cl2.
MgO.
HNO3.
Chuẩn độ dung dịch NaOH chưa biết chính xác nồng độ (biết nồng độ trong khoảng gần với 0,1 M) bằng dung dịch chuẩn HCl 0,1 M với chỉ thị phenolphtalein. Tại thời điểm tương đương, điều nào sau đây không đúng ?
Phenolphthalein mất màu hồng.
Nếu thêm tiếp NaOH, bình tam giác chứa phenolphtalein không chuyển sang màu hồng.
Các chất phản ứng vừa đủ với nhau.
Số mol ion H+ bằng số mol OH-đã phản ứng.
Dung dịch HCl 0,001M có giá trị pH là
13
1
3
11
Ở nhiệt độ cao, nitrogen thể hiện tính khử khi phản ứng với đơn chất nào sau đây
2
Ca
Mg
O2
Cho ba dung dịch có cùng nồng độ: hydrochloric acid (HCl), ethanoic acid (acetic acid, CH3COOH) và sodium hydroxide (NaOH). Khi chuẩn độ riêng một thể tích như nhau của dung dịch HCl và dung dịch CH3COOH bằng dung dịch NaOH, phát biểu nào sau đây đúng?
Cần dùng một thể tích sodium hydroxide để đạt đến điểm tương đương.
Trước khi chuẩn độ, pH của hai acid bằng nhau.
Giá trị pH của hai acid tăng như nhau cho đến khi đạt điểm tương đương.
Tại các điểm tương đương, dung dịch của cả hai phép chuẩn độ đều có giá trị pH bằng 7.
Chất nào dưới đây không phân li ra ion khi hòa tan trong nước ?
HCl
6H12O6 (glucose)
Ba(OH)2
MgCl2
Phát biểu nào sau đây không đúng?
Hầu hết các muối ammonium đều dễ tan trong nước.
Các muối ammonium đều kém bền với nhiệt, khi đun nóng bị phân huỷ thành ammonia và acid tương ứng.
Muối ammonium tác dụng với dung dịch kiềm giải phóng ammonia.
Dung dịch muối ammonium phân ly hoàn toàn thành ion.
Có thể dùng chất nào sau đây để làm khô khí ammonia
MgO khan
Dung dịch H2SO4 đặc
CaO khan
P2O5 khan
Nhận xét nào sau đây không đúng?
Phản ứng một chiều là phản ứng luôn xảy ra không hoàn toàn.
Phản ứng thuận nghịch là phản ứng xảy ra theo hai chiều trái ngược nhau trong cùng điều kiện.
Trong phản ứng một chiều, chất sản phẩm không phản ứng được với nhau tạo thành chất đầu.
Trong phản ứng thuận nghịch, các chất sản phẩm có thể phản ứng với nhau để tạo thành chất đầu.
Các yếu tố ảnh hưởng đến cân bằng hoá học là
Nồng độ, nhiệt độ và chất xúc tác
Nồng độ, nhiệt độ và áp suất
Áp suất, nhiệt độ và chất xúc tác
Nồng độ, áp suất và diện tích bề mặt
Cho các phát biểu sau :
(1) Nitric acid được dùng để sản xuất phân đạm, thuốc nổ (TNT), thuốc nhuộm, dược phẩm.
(2) Trong công nghiệp, phần lớn lượng nitrogen sản xuất ra được dùng để tổng hợp ammonia.
(3) Khí NH3 nhẹ hơn không khí và ít tan trong nước
(4) Khi nhiệt phân muối ammonium luôn luôn có khí ammonia thoát ra.
(5) Cho vài giọt dung dịch phenolphthalein vào dung dịch NH3, phenolphthalein chuyển sang màu hồng.
Số phát biểu đúng là
6.
4.
3.
5.
Hệ phản ứng sau ở trạng thái cân bằng: H2 (g) + I2 (g) 2HI (g) Biểu thức của hằng số cân bằng của phản ứng trên là
KC =
KC =
KC =
KC =
Trường hợp nào không dẫn điện được
NaOH nóng chảy
NaCl rắn, khan
NaCl nóng chảy
NaCl trong nước
Mưa acid là hiện tượng nước mưa có lẫn các hạt acid làm cho nước mưa có độ pH nhỏ hơn 5. Mưa acid gây ảnh hưởng nghiêm trọng đến môi trường, cây trồng và cả sức khỏe con người. Nguyên nhân chủ yếu gây ra hiện tượng mưa acid là do khí và khí X đã gây ô nhiễm không khí. Khí X có thể là
O 2
Công thức Lewis của phân tử ammonia là
A. 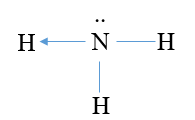 .
.
B. 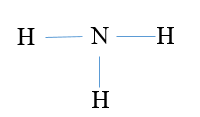 ..
..
C. 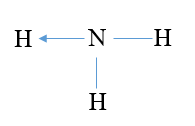 .
.
D. 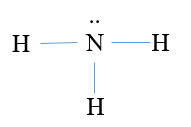 .
.
(1 điểm). Việc sản xuất amonia trong công nghiệp dựa trên phản ứng thuận nghịch sau đây:
N2(g) + 3H2(g) 2NH3(g) = -92 kJ
(1) Cân bằng sẽ chuyển dịch theo chiều nào nếu:
(a) Tăng nhiệt độ.
(b) Lấy NH3 ra khỏi hệ.
(2) Ở toC, nồng độ các chất ở trạng thái cân bằng là .
Tính hằng số cân bằng của phản ứng trên tại .
(1 điểm). Cho 9,6 gam Cu vào dung dịch HNO3 loãng, dư thu được V lít khí NO (đkc) là sản phẩm khử duy nhất. Tính V.(Cu = 64)
(1 điểm). Sự thay đổi màu của hoa cẩm tú cầu đã tạo nên vẻ đẹp kì diệu của loài hoa này. Màu của loài hoa này có thể thay đổi tùy thuộc vào pH của đất trồng nên có thể điểu chỉnh màu hoa thông qua việc điều chỉnh độ pH của đất
| pH đất trồng | < 7 | = 7 | > 7 |
| Hoa sẽ có màu | Lam | Trắng sữa | Hồng |
Khi trồng loài hoa trên, nếu ta bón thêm 1 ít vôi (CaO) hoặc đạm 2 lá (NH4NO3) và chỉ tưới nước thì khi thu hoạch hoa sẽ có màu lần lượt như thế nào. Giải thích








