Bộ 3 đề thi giữa kì 1 Hóa 11 Kết nối tri thức cấu trúc mới có đáp án - Đề 3
28 câu hỏi
PHẦN I. Câu trắc nghiệm nhiều phương án lựa chọn. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
Biểu thức tính hằng số cân bằng (KC) của phản ứng tổng quát: aA + bB cC + dD là
\[{K_C} = \frac{{[A].[B]}}{{[C].[D]}}\]
\[{K_C} = \frac{{{{[A]}^a}.{{[B]}^b}}}{{{{[C]}^c}.{{[D]}^d}}}\]
\[{K_C} = \frac{{{{[C]}^c}.{{[D]}^d}}}{{{{[A]}^a}.{{[B]}^b}}}\]
\[{K_C} = \frac{{[C].[D]}}{{[A].[B]}}\]
Yếu tố nào sau đây luôn luôn khônglàm dịch chuyển cân bằng của hệ phản ứng?
Nhiệt độ.
Áp suất.
Nồng độ.
Chất xúc tác.
Cân bằng hoá học nào sau đây không bị chuyển dịch khi thay đổi áp suất?
Chất nào sau đây thuộc loại chất điện li mạnh?
NaHCO3.
C2H5OH.
H2O.
NH3.
Theo thuyết Bronsted – Lowry chất nào sau đây lưỡng tính?
Mg2+.
NH3.
HCO3−.
Cho dãy các chất: K2SO4.Al2(SO4)3.24H2O, C2H5OH, C12H22O11 (saccharose), CH3COOH, Ca(OH)2, CH3COONH4. Số chất điện li là
3.
4.
5.
2.
Một dung dịch có pH = 11,7. Nồng độ ion hydrogen (H+) của dung dịch là
2,3M.
11,7M.
5,0.10-3M.
2,0.10-12M.
Trong phản ứng: N2(g) + O2(g) 2NO(g). N2 thể hiện
tính khử.
tính oxi hóa.
tính base.
tính acid.
Khí nitrogen ít tan trong nước là do
nitrogen có bán kính nguyên tử nhỏ.
nitrogen có độ âm điện lớn.
phân tử nitrogen có liên kết ba bền vững.
phân tử nitrogen không phân cực.
Ở dạng hợp chất, nitrogen tồn tại nhiều trong các mỏ khoáng dưới dạng
NaNO3.
KNO3.
HNO3.
Ba(NO3)2.
Tính chất hóa học của NH3 là
tính base, tính khử.
tính base, tính oxi hóa.
tính acid, tính base.
tính acid, tính khử.
Có thể nhận biết muối ammonium bằng cách cho muối tác dụng với dung dịch kiềm thấy thoát ra một chất khí. Chất khí đó là
NH3.
H2.
NO2
NO.
Phương trình hóa học nào sau đây sai?
Dãy các muối ammonium nào khi bị nhiệt phân tạo thành khí NH3?
NH4Cl, NH4HCO3, (NH4)2CO3.
NH4Cl, NH4NO3, NH4HCO3.
NH4Cl, NH4NO3, (NH4)2CO3.
NH4NO3, NH4HCO3, (NH4)2CO3.
Nitrogen dioxide là tên gọi của oxide nào sau đây?
NO.
NO2.
N2O.
N2O4.
Mưa acid là hiện tượng tượng nước mưa có pH như thế nào?
> 5,6.
< 7.
> 7.
< 5,6.
Kim loại iron không phản ứng được với dung dịch nào sau đây?
HNO3 đặc, nguội.
H2SO4 đặc, nóng.
HNO3 loãng.
H2SO4 loãng.
Tổnghệsố(cácsốnguyên,tốigiản)củatấtcảcácchấttrongphươngtrìnhphảnứng giữaCuvớidungdịchHNO3đặc,nónglà
10.
11.
8.
9.
PHẦN II. Câu trắc nghiệm đúng sai. Thí sinh trả lời từ câu 1 đến câu 4. Trong mỗi ý a), b), c), d) ở mỗi câu, thí sinh chọn đúng hoặc sai. (Đ – S)
Muối ammonium được sử dụng rộng rãi trong đời sống và sản xuất, đặc biệt được dùng làm phân bón trong nông nghiệp.
a. Trong cation ammonium, có 3 liên kết cộng hoá trị và một liên kết ion.
b. Số oxi hoá của nguyên tử nitrogen trong cation ammonium là -4.
c. Cation ammonium là một acid theo Brønsted – Lowry.
d. Các liên kết trong NH4Cl là liên kết cộng hoá trị.
Cho các chất: Ba(OH)2, HF, C2H5OH, Na2SO4.
a. Có 3 chất điện li mạnh là Ba(OH)2, C2H5OH, Na2SO4.
b. Phương trình điện li của Na2SO4 là \[N{a_2}S{O_4} \to {\rm{ }}N{a^{2 + }} + {\rm{ }}SO_4^{2 - }.\]
c. Dung dịch HF trong nước chứa các phần tử: H+, F̶, H2O (bỏ qua sự phân li của H2O).
d. Dung dịch C2H5OH trong nước chứa các phần tử: C2H5+, OH−, C2H5OH, H2O (bỏ qua sự phân li của H2O).
Cho cân bằng hoá học sau:
N2(g) + 3H2(g) 2NH3(g) \[{\Delta _r}H_{298}^o = - 92\,kJ.\]
a. Khi tăng nhiệt độ của hệ, cân bằng chuyển dịch theo chiều thuận.
b. Phản ứng thuận là phản ứng toả nhiệt.
c. Khi tăng áp suất của hệ, cân bằng chuyển dịch theo chiều nghịch.
d. Khi tăng nồng độ của NH3, cân bằng chuyển dịch theo chiều nghịch
HNO3 tinh khiết là chất lỏng không màu, nhưng dung dịch HNO3 để lâu thường chuyển sang màu vàng.
a. HNO3 tan nhiều trong nước.
b. HNO3 là một base mạnh.
c. Dung dịch HNO3 có tính oxi hóa mạnh.
d. Dung dịch HNO3 đặc để lâu có hoà tan một lượng nhỏ NO2.
PHẦN III. Câu hỏi trắc nghiệm yêu cầu trả lời ngắn. Thí sinh trả lời từ câu 1 đến câu 6.
Có 4 ống nghiệm, mỗi ống đựng một chất khí khác nhau trong số các khí NH3, HCl, O2, SO2. Các ống nghiệm được úp ngược trong các chậu nước X, Y, Z, T. Kết quả thí nghiệm được mô tả bằng hình vẽ sau:
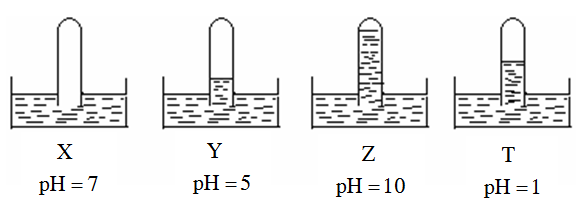
Các khí X, Y, Z, T lần lượt là?
Trong công nghiệp, hydrogen được sản xuất từ phản ứng:
CH4(g) + H2O(g) ⇌ 3H2(g) + CO(g)
Hằng số cân bằng KC của phản ứng trên ở 760 oC là?
Biết ở nhiệt độ này, tất cả các chất đều ở thể khí và nồng độ mol của CH4, H2O, H2 và CO ở trạng thái cân bằng lần lượt là 0,126 M; 0,242 M; 1,150 M và 0,126 M.
Khi bảo quản các dung dịch muối M3+ (Fe3+, Al3+ …) trong phòng thí nghiệm, người ta thường nhỏ vài giọt dung dịch nào vào trong lọ đựng dung dịch muối?
Thí nghiệm với dung dịch HNO3 thường sinh ra khí độc NO2. Để hạn chế khí NO2 thoát ra từ ống nghiệm, người ta nút ống nghiệm bằng?
Cho iron (III) oxide tác dụng với nitric acid thì sản phẩm thu được là?
Oxide được hình thành trực tiếp từ phản ứng của nitrogen với oxygen?








