Bộ 5 đề thi cuối kì 1 Hóa 10 Chân trời sáng tạo (2022-2023) có đáp án - Đề 5
32 câu hỏi
Trong nguyên tử, hạt mang điện tích âm là
chỉ có electron.
gồm neutron và electron.
gồm proton và neutron.
chỉ có proton.
Phát biểu nào sau đây là không đúng?
Khối lượng của proton lớn hơn rất nhiều so với khối lượng của neutron.
Proton và electron là các hạt mang điện, neutron là hạt không mang điện.
Electron tạo nên lớp vỏ nguyên tử.
Số lượng proton và electron trong nguyên tử là bằng nhau
Nguyên tố hoá học là tập hợp những
nguyên tử có cùng số proton.
nguyên tử có cùng số nơtron và proton.
nguyên tử có cùng số khối.
nguyên tử có cùng số neutron.
Phát biểu nào sau đây là đúng về đồng vị?
Các nguyên tử của cùng một nguyên tố hoá học có cùng số e và cùng số n là đồng vị của nhau.
Các nguyên tử của cùng một nguyên tố hoá học có cùng số p và cùng số n là đồng vị của nhau.
Các nguyên tử của cùng một nguyên tố hoá học có số neutron khác nhau là đồng vị của nhau.
Các nguyên tố hóa học khác nhau có số neutron bằng nhau là đồng vị của nhau.
Lớp electron gần hạt nhân nguyên tử nhất kí hiệu là
lớp K.
lớp L.
lớp M.
lớp N.
Theo mô hình Rutherford – Bohr, quỹ đạo chuyển động của các electron xung quanh hạt nhân có dạng hình gì?
Hình zich–zắc.
Hình tròn.
Hình vuông.
Hình cầu.
Các nguyên tố xếp ở chu kỳ 5 có bao nhiêu lớp electron trong nguyên tử?
6.
5.
3.
4.
Hình dạng của orbital (AO)s và AO(p) tương ứng là
Hình elip và hình số tám nổi.
Hình số tám nổi và hình cầu
Hình cầu và hình lục phương.
Hình cầu và hình số tám nổi.
Bảng tuần hoàn hiện nay không áp dụng nguyên tắc sắp xếp nào sau đây ?
Các nguyên tố có cùng số lớp electron trên nguyên tử được xếp thành một hàng.
Các nguyên tố được sắp xếp theo chiều tăng dần khối lượng nguyên tử.
Các nguyên tố có cùng số electron hóa trị trong nguyên tử được xếp thành một cột.
Mỗi nguyên tố hóa học được xếp vào một ô trong bảng tuần hoàn.
Nguyên tố Si (Z = 28) thuộc nhóm nào ?
VIIA.
IIA.
VIIIA.
IVA.
Trong một chu kì, theo chiều tăng dần của điện tích hạt nhân thì
bán kính nguyên tử giảm dần, tính kim loại tăng dần.
bán kính nguyên tử giảm dần, tính phi kim tăng dần.
bán kính nguyên tử tăng dần, tính phi kim tăng dần.
bán kính nguyên tử tăng dần, tính kim loại giảm dần.
Trong bảng tuần hoàn hóa học, nguyên tố nhóm A nào trong mỗi chu kỳ có độ âm điện lớn nhất:
Nhóm IIA.
Nhóm VIIIA.
Nhóm IA.
Nhóm VIIA.
Tính chất base của hydroxide trong một chu kỳ theo chiều tăng của số thứ tự là
tăng dần.
giảm dần.
không thay đổi.
vừa giảm vừa tăng.
Phát biểu nào sau đây về liên kết hóa học là đúng?
Liên kết hóa học là sự kết hợp giữa các nguyên tử tạo thành phân tử hoặc tinh thể bền vững hơn.
Liên kết hóa học là sự kết hợp giữa các phân tử tạo thành tinh thể bền vững hơn.
Liên kết hóa học là sự kết hợp giữa các nguyên tố tạo thành phân tử hoặc hợp chất kém bền hơn.
Liên kết hóa học là sự kết hợp giữa các nguyên tử tạo thành phân tử hoặc tinh thể kém bền hơn.
Liên kết ion được hình thành bởi lực hút tĩnh điện giữa
các nguyên tử trung hòa.
giữa nguyên tử và ion có điện tích dương.
giữa nguyên tử và ion mang điện tích âm.
giữa các ion mang điện tích trái dấu.
Liên kết nào sau đây thường được tạo thành giữa 1 nguyên tử kim loại điển hình và 1 phi kim điển hình:
Liên kết cộng hóa trị phân cực.
Liên kết ion.
Liên kết cộng hóa trị không phân cực.
Liên kết cho – nhận.
Chọn đáp án sai:
Khối lượng của hạt nhân xấp xỉ khối lượng nguyên tử.
Trong nguyên tử, số proton bằng số electron.
Hạt nhân tạo bởi hạt proton và hạt neutron.
Trong nguyên tử có số proton khác số electron.
Cho phổ khối lượng của chlorine như sau:
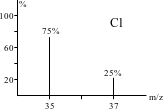
Nguyên tử khối trung bình của chlorine là
35 amu
35,5 amu
36 amu
36,5 amu
Nguyên tử 26Fe có cấu hình electron là 1s22s22p63s23p63d64s2. Nguyên tử Fe có bao nhiêu electron độc thân:
1.
3.
5.
4.
Cấu hình electron nào sau đây là của nguyên tử kim loại?
1s22s22p63s23p4
1s22s22p63s23p5
1s22s22p63s1
1s22s22p6
Ở lớp thứ ba (n = 3) có tối đa bao nhiêu electron?
2.
10.
18.
32.
Hai nguyên tố X, Y thuộc hai nhóm liên tiếp nhau trong một chu kì. Tổng số proton của chúng bằng 39. Phát biểu nào sau đây là không đúng ?
X và Y đều phản ứng mãnh liệt với nước ở điều kiện thường.
X thuộc nhóm IA và Y thuộc nhóm IIA.
X là nguyên tố p.
Tính kim loại của X lớn hơn Y.
Dãy nguyên tố nào sau đây được xếp theo chiều giảm dần tính phi kim?
Cl,F,Br,I.
F,Br,Cl,I.
F,Cl,I,Br.
F,Cl,Br,I.
Cho nguyên tử của nguyên tố X có cấu tạo như sau:
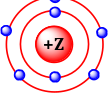
Vị trí của nguyên tố X trong bảng tuần hoàn là
ô số 7, chu kì 2, nhóm VIIA.
ô số 7, chu kì 2, nhóm VA.
ô số 5, chu kì 2, nhóm VA.
ô số 5, chu kì 7, nhóm VIIA.
Sắp xếp các base: Al(OH)3, Mg(OH)2, CsOH, Ba(OH)2 theo độ mạnh tăng dần:
Ba(OH)2 < Mg(OH)2 < Al(OH)3 < CsOH.
Mg(OH)2 < Ba(OH)2 < Al(OH)3 < CsOH.
Al(OH)3 < Mg(OH)2 < Ba(OH)2 < CsOH.
Al(OH)3 < Ba(OH)2 < Mg(OH)2 < CsOH.
Để đánh giá loại liên kết trong phân tử hợp chất, người ta có thể dựa vào hiệu độ âm điện. Khi hiệu độ âm điện của hai nguyên tử tham gia liên kết ≥ 1,7 thì đó là liên kết:
kim loại.
cộng hoá trị không cực.
cộng hoá trị có cực.
Ion.
Trong dãy sau: Na2O, MgO, Al2O3, SiO2, P2O5, SO3, Cl2O7. Những oxide có liên kết cộng hóa trị là: (Cho độ âm điện của các nguyên tố Na = 0,93; Mg = 1,31; Cl = 3,16; O = 3,44; S = 2,58; P = 1,19; Al = 1,61; Si = 1,90)
Na2O , SiO2 , P2O5.
MgO, Al2O3 , P2O5 .
Na2O, MgO, Al2O3.
SO3,Cl2O7 ,P2O5.
Chất nào trong các chất sau có khả năng tạo liên kết Hydrogen:
HI.
H2S.
PH3.
H2O.
(1 điểm) Nguyên tử tố M có 20 hạt proton trong hạt nhân. Nguyên tố Y có số proton trong hạt nhân ít hơn hạt nhân của nguyên tố M là 8 hạt. Nguyên tố Z có 19 electron trong nguyên tử.
(a) Xác định tên các nguyên tố M, Y và Z.
(b) Sắp xếp M, Y và Z theo chiều tăng dần bán kính nguyên tử.
(1 điểm) Cho độ âm điện của các nguyên tố sau:
| Nguyên tố | H | C | Br | K | Na | Cl |
| Độ âm điện | 2,20 | 2,55 | 2,96 | 0,82 | 0,93 | 3,16 |
Cho biết loại liên kết trong các phân tử sau: CH4, NaCl, KBr, HBr. Giải thích.
(0,5 điểm) (a) Giải thích tại sao NH3 tan tốt trong nước.
(b) Hãy giải thích (kèm hình vẽ) tại sao nhiệt độ sôi của HF (19,5 oC) cao hơn đáng kể so với nhiệt độ sôi của HCl (-85,1 oC).
(0,5 điểm) Flourine (F) có (Z = 9).
Hãy viết công thức Lewis của phân tử F2. Xác định số electron riêng và dùng chung của nguyên tử F trong phân tử và dự đoán khả năng nhường hay nhận electron của nguyên tố flourine khi tham gia các phản ứng hóa học








