Bộ 5 đề thi cuối kì 1 Hóa 10 Chân trời sáng tạo (2022-2023) có đáp án - Đề 2
32 câu hỏi
Hạt mang điện trong hạt nhân nguyên tử là
electron.
proton.
neutron.
neutron và electron.
Nitrogen là một chất khí chiếm số lượng lớn không chỉ ở trái đất mà còn được tìm thấy nhiều đứng hàng thứ bảy toàn bộ Dải Ngân hà và cả hệ Mặt Trời. Nói riêng về Trái đất, nó chiếm khoảng 78% toàn bộ bầu khí quyển. Trong cơ thể con người, nitrogen chiếm khoảng 3% trọng lượng cơ thể của con người chúng ta và nitrogen cũng được xem là nguyên tố có thành phần phong phú nhất chỉ sau oxygen, carbon và hydrogen. Biết rằng hạt nhân nguyên tử nitrogen có 7 proton và 7 neutron. Ký hiệu nguyên tử nitrogen là:

\(77N.\)
\(147N.\)
\(714N.\)
\(721N.\)
Công thức cấu tạo nào sau đây là công thức Lewis?

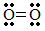
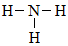
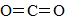
Bảng tuần hoàn hiện nay không áp dụng nguyên tắc sắp xếp nào sau đây ?
Mỗi nguyên tố hóa học được xếp vào một ô trong bảng tuần hoàn.
Các nguyên tố được sắp xếp theo chiều tăng dần khối lượng nguyên tử.
Các nguyên tố có cùng số lớp electron trong nguyên tử được xếp thành một hàng.
Các nguyên tố có cùng số electron hóa trị trong nguyên tử được xếp thành một cột.
Định luật tuần hoàn phát biểu rằng tính chất của các đơn chất cũng như thành phần và tính chất của hợp chất tạo nên từ các nguyên tố biến đổi tuần hoàn theo chiều tăng của yếu tố nào sau đây?
Điện tích hạt nhân nguyên tử.
Khối lượng nguyên tử.
Bán kính nguyên tử.
Số lớp electron.
Theo quy tắc octet, khi hình thành liên kết hóa học, các nguyên tử có xu hướng nhường, nhận hoặc góp chung electron để đạt tới cấu hình electron bền vững giống như
Kim loại kiềm gần nhất.
Kim loại kiểm thổ gần nhất.
Nguyên tử halogen gần nhất.
Nguyên tử khí hiếm gần nhất.
Điều nào dưới đây đúng khi nói về ion O2- ?
Hạt nhân có chứa 10 proton.
Lớp vỏ có chứa 10 electron.
Trung hoà về điện.
Được tạo thành khi nguyên tử Oxygen (O) nhường 2 electron.
Chọn phát biểu đúng nhất
Liên kết ion là liên kết được hình thành giữa hai nguyên tử kim loại.
Liên kết ion là liên kết được hình thành bởi lực hút tĩnh điện giữa các ion mang điện tích cùng dấu.
Liên kết ion là liên kết được hình thành bởi lực hút tĩnh điện giữa các ion mang điện tích trái dấu.
Liên kết ion thường được hình thành giữa hai nguyên tử phi kim điển hình.
Chọn phát biểu đúng nhất: Liên kết cộng hoá trị là liên kết
Giữa các nguyên tử phi kim với nhau.
Được hình thành do sự dùng chung electron giữa hai nguyên tử khác nhau.
Được hình thành giữa hai nguyên tử bằng một hay nhiều cặp electron chung.
Trong đó cặp electron dùng chung bị lệch về phía một nguyên tử.
Orbital nguyên tử là
đám mây chứa electron có dạng hình cầu.
đám mây chứa electron có dạng hình số 8 nổi.
khu vực không gian xung quanh hạt nhân mà tại đó xác suất có mặt electron lớn nhất.
quỹ đạo chuyển động của electron quay quanh hạt nhân có kích thước và năng lượng xác định.
Các liên kết bằng dấu chấm (...) có vai trò quan trọng trong việc làm bền chuỗi xoắn DNA. Đó là loại liên kết gì
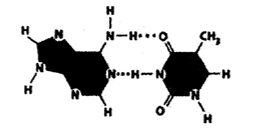
liên kết cộng hóa trị có cực.
liên kết ion.
liên kết cộng hóa trị không cực.
liên kết hydrogen.
Năng lượng liên kết (Eb) đặc trưng cho điều gì?
Độ bền liên kết.
Độ dài liên kết.
Tính chất liên kết.
Loại liên kết.
Những liên kết có lực liên kết yếu như
liên kết hydrogen và tương tác Van der Waals.
liên kết ion và liên kết cộng hóa trị.
liên kết ion và liên kết hydrogen.
liên kết hydrogen và liên kết cộng hóa trị.
Trong dãy halogen, tương tác van der Waals (1) …… theo sự (2) ….. của số electron (và proton) trong phân tử, làm (3) ….. nhiệt độ nóng chảy, nhiệt độ sôi của các chất
(1) Tăng, (2) Tăng, (3) Tăng.
(1) Tăng, (2) Giảm, (3) Tăng.
(1) Giảm, (2) Tăng, (3) Giảm.
(1) Giảm, (2) Tăng, (3) Tăng.
Liên kết cộng hóa trị không cực là gì?
Liên kết cộng hóa trị mà trong đó cặp điện tử dùng chung lệch về nguyên tử có độ âm điện lớn hơn.
Liên kết cộng hóa trị mà trong đó cặp điện tử dùng chung lệch về nguyên tử có độ âm điện bé hơn.
Liên kết cộng hóa trị mà trong đó cặp electron dùng chung không lệch về nguyên tử nào.
Liên kết hình thành giữa 2 nguyên tử có độ âm điện khác nhau.
Dựa vào giá trị hiệu độ âm điện ta có thể dự đoán được điều gì?
Tính chất của liên kết.
Loại liên kết.
Liên kết lệch về nguyên tử nào.
Độ dài liên kết.
Thông tin nào sau đây không đúng?
Proton mang điện tích dương, nằm trong hạt nhân, khối lượng gần bằng 1 amu.
Electron mang điện tích âm, nằm trong hạt nhân, khối lượng gần bằng 0 amu.
Neutron không mang điện, nằm trong hạt nhân, khối lượng gần bằng 1 amu.
Nguyên tử trung hòa về điện, có kích thước lớn hơn nhiều so với hạt nhân, nhưng có khối lượng gần bằng khối lượng hạt nhân.
Aluminium có rất nhiều ứng dụng trong cuộc sống. Kim loại này được các thương hiệu tại Việt Nam dùng để tạo thành vỏ máy bay do độ bền chắc và mỏng nhẹ của nó. Aluminium cũng được dùg để sản xuất các thiết bị và dụng cụ sinh hoạt như nồi, chảo, các đường dây tải điện, các loại cửa,… Cấu hình electron của nguyên tử Aluminium (Z = 13) theo ô orbital là:


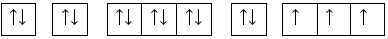
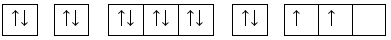

Cho các nhận xét dưới đây:
(a) Hợp chất khí với hidrogen của nguyên tố X là XH3 thì công thức oxide cao nhất của X có thể là X2O5.
(b) Công thức phân tử của hợp chất khí tạo bởi nguyên tố R và hidrogen là RH2 thì cấu hình e của R có thể là 1s22s22p4.
(c) Cho cấu hình electron của A là: 1s22s22p63s23p64s2. Vậy A thuộc chu kì 3, nhóm IIA.
(d) Nguyên tử của nguyên tố X có phân lớp electron ở mức năng lượng cao nhất là 3p4 nên X thuộc nhóm IVA trong bảng tuần hoàn.
Số phát biểu đúng là
1.
3.
2.
4.
Trong các hợp chất, để đạt được cấu hình bền của khí hiếm gần nhất, nguyên tử magnesium đã
nhường đi 2 e.
nhận vào 1 e.
nhường đi 3 e.
nhận vào 2 e.
Dãy các phân tử đều có liên kết ion là
Cl2, Br2, I2. HCl.
HCl, H2S, NaCl, N2O.
BaCl2, Al2O3, KCl, Na2O.
HCl, H3PO4, H2SO4. MgO.
Phát biểu nào sau đây không đúng?
Liên kết δ liên kết bền vững hơn liên kết \(π\).
Chỉ có các AO có hình dạng giống nhau mới xen phủ với nhau để tạo liên kết.
Khi hình thành liên kết cộng hoá trị giữa hai nguyên tử, luôn có một liên kết \(δ\).
Có hai kiểu xen phủ hình thành liên kết là xen phủ trục và xen phủ bên.
Ta có độ âm điện của Carbon là 2,55; của Hydrogen 2,20. Dựa vào hiệu độ âm điện em hãy cho biết phân tử CH4 có liên kết thuộc loại nào?
Liên kết ion.
Liên kết cộng hóa trị có cực.
Liên kết cộng hóa trị không cực.
Liên kết hydro.
Cho các chất sau: C2H6; H2O; NH3; PF3; C2H5OH. Số chất tạo được liên kết hydrogen là
2.
3.
4.
5.
Cho các phản ứng sau:
(a) 2NH3 + 3Br2 → N2 + 6HBr
(b) Ca(OH)2 + CO2 → CaCO3 + H2O
(c) 4FeS2 + 11O2 →t° 2Fe2O3 + 8SO2
(d) 2KMnO4 + 16HCl → 2KCl +2 MnCl2 + 5Cl2 + 8H2O
Trong các phản ứng trên, số phản ứng oxi hóa – khử là
1.
2.
3.
4.
Chọn số phát biểu đúng:
(a) Theo quy tắc Octet, công thức cấu tạo của phân từ H2SO4 có 2 liên kết cho nhận
(b) Theo quy tắc Octet, công thức cấu tạo của phân từ H2SO4 có 2 liên kết đôi.
(c) Theo quy tắc Octet, công thức cấu tạo của phân từ HNO3 có 2 liên kết cho nhận.
(d) Theo quy tắc Octet, công thức cấu tạo của phân từ HNO3 không có liên kết cho nhận.
1.
4.
0.
2.
Tại áp suất 1 bar, nước có nhiệt độ nóng chảy và nhiệt độ sôi tương ứng là 0oC và (xấp xỉ) 100oC, cao hơn so với nhiều chất có khối lượng phân tử lớn hơn nước. Tính chất này là do
các phân tử nước liên kết khá chặt chẽ với nhau bởi các liên kết ion.
các phân tử nước liên kết khá chặt chẽ với nhau bởi các liên kết cộng hóa trị.
các phân tử nước liên kết khá chặt chẽ với nhau bởi các liên kết hydrogen.
các phân tử nước liên kết khá chặt chẽ với nhau bởi các liên kết cho – nhận.
Trong phản ứng quang hợp:
6CO2 +6H2O \(→ánh sáng\)C6H10O6 + 6O2
Trong quá trình quang hợp thì CO2 đóng vai trò là chất gì?
Chất oxi hóa.
Chất khử.
Vừa là chất oxi hóa vừa là chất khử.
Vừa là chất oxi hóa vừa là môi trường.
(1 điểm) X và Y là hai nguyên tố thuộc nhóm A và thuộc cùng một chu kì nhỏ của bảng tuần hoàn. Tổng số electron hóa trị của X và Y là 8. Trong oxide cao nhất Y chiếm 38,798% về khối lượng. Biết cả X và Y đều thuộc nhóm lẻ.
(a) X và Y là nguyên tố gì? So sánh bán kính nguyên tử của X và Y?
(b) Hãy trình bày sự hình thành liên kết trong phân tử khi X tác dụng với Y?
(1 điểm) Một nhóm học sinh trường THPT Cái Bè thực hiện thí nghiệm như hình vẽ sau:
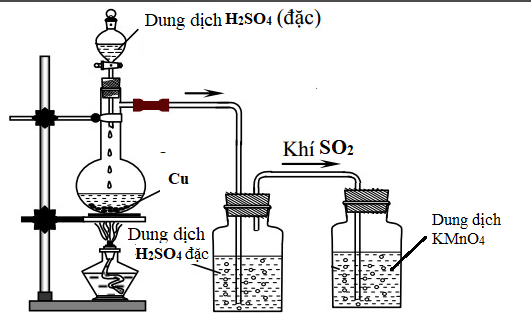
Quan sát thí nghiệm, nhóm học sinh nhận thấy kim loại copper có xảy ra phản ứng với dung dịch H2SO4 đặc, copper tan và dung dịch từ từ chuyển sang màu xanh. Bình đựng dung dịch KMnO4 do có phản ứng với khí SO2 nên màu của dung dịch nhạt dần đi. Kết thúc thí nghiệm xảy ra các phản ứng sau:
Cu + H2SO4 CuSO4 + SO2 + H2O
SO2 + KMnO4 + H2O MnSO4 + K2SO4 + H2SO4
Bằng phương pháp thăng bằng electron hãy cân bằng các phản ứng trên
(0,5 điểm) Cho phản ứng sau:
NH3 + H+ NH4+
(a) Viết công thức Lewis của NH3.
(b) Viết công thức cấu tạo của ion NH4+.
(0,5 điểm)
Để kiểm tra lượng ethanol có trong huyết thanh, người ta sẽ lấy một lượng huyết thanh đem tác dụng với dung dịch K2Cr2O7 theo phương trình phản ứng chuẩn độ sau:
CH3CH2OH + K2Cr2O7 + H2SO4 CH3CHO + Cr2(SO4)3 + K2SO4 + H2O
Trong trường hợp một người tài xế được lấy 20 ml huyết thanh tác dụng với 35 ml dung dịch K2Cr2O7 0,06M. Căn cứ theo điểm c khoản 6; điểm c khoản 7 và điểm e khoản 8 điều 6 Nghị định 100/2019/NĐ-CP quy định:
| Quy định nồng độ cồn | ≤ 50 miligam/100 ml máu | >50 miligam đến 80 miligam /100 ml máu | > 80 miligam /100 ml máu |
| Mức phạt hành chính | Phạt từ 2.000.000 đồng đến 3.000.000 | Phạt từ 4.000.000 đồng đến 5.000.000 | Phạt từ 6.000.000 đồng đến 8.000.000 |
Nếu các thao tác tính toán là chính xác, người tài xế trên sẽ bị phạt hành chính mức bao nhiêu?








