Bộ 5 đề thi cuối kì 1 Hóa 10 Chân trời sáng tạo (2022-2023) có đáp án - Đề 3
32 câu hỏi
Hiệu độ âm điện giữa 2 nguyên tử trong liên kết cộng hóa trị phân cực có giá trị
≥ 1,7.
từ 0,4 đến < 1,7.
từ 0 đến < 0,4.
≤ 1,7.
Hợp chất nào sau đây khó nóng chảy và khó bay hơi?
P.
NH3.
MgO.
Br2.
Số neutron trong nguyên tử 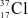 là
là
37.
20.
18.
17.
Biết độ âm điện của nitrogen và hydrogen có giá trị lần lượt là 3,04 và 2,2. Liên kết N – H trong phân tử ammonia (NH3) thuộc loại liên kết nào?
Cộng hóa trị phân cực.
Không xác định được bản chất liên kết.
Cộng hóa trị không phân cực.
Liên kết Ion.
Theo quy tắc octet, khi hình thành phân tử chlorine (Cl2), mỗi nguyên tử chlorine góp chung bao nhiêu electron?
4.
1.
2.
3.
Ion nào dưới đây là ion đơn nguyên tử?
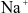 .
.
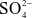 .
.
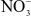 .
.
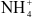 .
.
Theo quy tắc octet, khi hình thành liên kết hóa học, các nguyên tử kim loại nhóm IIA có xu hướng nhường bao nhiêu electron?
4.
2.
3.
1.
Hợp chất nào sau đây tạo được liên kết hidrogen với H2O?
NaI
HF
KCl
Cl2
Trong một nhóm A, theo chiều tăng của điện tích hạt nhân, bán kính nguyên tử các nguyên tố biến đổi như thế nào?
Giảm dần.
Không đổi.
Tăng dần.
Ban đầu tăng, sau đó giảm.
Nguyên tử X có 24 proton. Điện tích hạt nhân của X là
+29.
+11.
+19.
+24.
Liên kết σ trong phân tử nào sau đây được hình thành nhờ sự xen phủ s – s?
O2.
HF.
H2
N2.
Trong phân tử nào sau đây, S không thỏa mãn quy tắc octet
SF6.
H2S.
K2S
SCl2
Tính chất nào sau đây không là tính chất của hợp chất ion?
Khó bay hơi.
Nhiệt độ sôi thấp.
Thường dễ tan trong nước.
Nhiệt độ nóng chảy cao.
Trong một chu kì, theo chiều tăng của điện tích hạt nhân nguyên tử thì
tính kim loại giảm dần, tính phi kim tăng dần.
tính kim loại và tính phi kim đều tăng dần.
tính kim loại tăng dần, tính phi kim giảm dần.
tính kim loại và tính phi kim đều giảm dần.
Hợp chất nào dưới đây là hợp chất ion?
N2.
HBr.
HClO2.
Na2O.
Nguyên tố X thuộc nhóm IVA của bảng tuần hoàn. Cấu hình electron lớp ngoài cùng của nguyên tử nguyên tố X là
ns2np3.
ns2np4.
ns2np5.
ns2np2.
Ở điều kiện thường, nước ở thể lỏng là do vai trò của loại liên kết nào sau đây?
Liên kết Ion.
Tương tác Van der waals.
Liên kết cộng hóa trị.
Liên kết hydrogen.
Cấu hình electron nguyên tử của nguyên tố X là 1s22s22p63s23p5. Số electron lớp ngoài cùng của X là
7.
5.
2.
3.
Khí hiếm nào sau đây có nhiệt độ sôi thấp nhất?
He (Z = 2).
Ar (Z = 18).
Ne (Z = 10).
Kr (Z = 36).
Cation Na+ được hình thành khi nguyên tử Na
nhận 1 proton.
nhận 1 electron.
nhường 1 electron.
nhường 1 proton.
Liên kết cộng hóa trị là liên kết được tạo thành bằng
lực hút tĩnh điện giữa các ion mang điện trái dấu.
lực tương tác yếu giữa các nguyên tử.
lực hút tĩnh điện giữa các electron tự do với ion dương kim loại.
cặp electron chung giữa hai nguyên tử.
Trong liên kết hydrogen buộc phải có sự tham gia liên kết của nguyên tử nào?
N.
I.
S.
H.
Công thức của phân tử NH3 như hình vẽ bên là công thức:
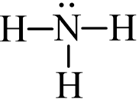
Lewis.
electron.
cấu tạo.
phân tử.
Số electron tối đa trong phân lớp p và s lần lượt là
2 và 10.
2 và 6.
6 và 2.
10 và 2.
Khi hình thành liên kết hóa học, nguyên tử có số hiệu nào sau đây có xu hướng nhận 1 electron để đạt cấu hình electron bền vững theo quy tắc octet?
Z = 9.
Z = 11.
Z = 8.
Z = 12.
Hình bên là mô phỏng của AO
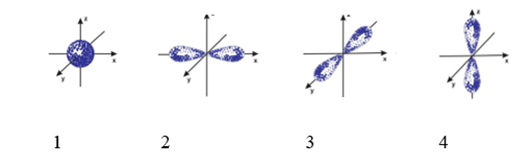
Đâu là hình mô phỏng của AOs
2.
1.
3.
4.
Nguyên tử nguyên tố X có lớp electron ngoài cùng là 3s23p3. Công thức oxide cao nhất của X là
X2O3.
XO2.
XO.
X2O5.
Cho các nguyên tố thuộc chu kỳ 3: 14Si, 15P, 16S và 17Cl. Trong các chất sau đây, chất có tính acid mạnh nhất là
H2SiO3.
HClO4.
H3PO4.
H2SO4.
Biết oxigen có 3 đồng vị bền trong tự nhiên và phần trăm số nguyên tử của chúng lần lượt là 16O (99,757%); 17O (0,039%); 18O (0,204%). Tính nguyên tử khối trung bình của oxygen.
Sodium fluoride (NaF) được sử dụng để chế dung dịch chống sâu răng, phụ gia cho kem đánh răng. Hãy viết hai giai đoạn của sự hình thành phân tử sodium fluoride từ các nguyên tử tương ứng (kèm theo cấu hình electron nguyên tử).
X và Y là hai nguyên tố kế tiếp nhau trong bảng tuần hoàn các nguyên tố hóa học (ZX < ZY), tổng số hạt mang điện của X và Y là 78. Trong X số proton ít hơn neutron là 1, trong Y số proton bằng số neutron. Viết kí hiệu nguyên tử của X và Y.
Cho biết năng lượng liên kết của Cl2 và N2 như bảng dưới:
| Liên kết | Cl - Cl | N ≡ N |
| E (kJ/mol) | 243 | 945 |
Giải thích vì sao độ âm điện của nitrogen là 3,04 xấp xỉ với độ âm điện của chlorine là 3,16 nhưng ở điều kiện thường, nitrogen kém hoạt động hơn nhiều so với chlorine. Từ đó hãy so sánh khả năng phản ứng của Cl2 và N2 khi cho lần lượt các khí này tác dụng với H2?








