Bộ 3 đề thi giữa kì 1 Hóa 10 Cánh diều có đáp án - Đề 1
32 câu hỏi
Vỏ của nguyên tử đều tạo bởi hạt nào sau đây?
Neutron.
Electron.
Neutron và proton.
Proton.
Trong nguyên tử, hạt mang điện tích dương là
electron.
proton và electron.
neutron.
proton.
Trong nguyên tử, loại hạt có khối lượng không đáng kể so với các hạt còn lại là
proton.
neutron.
electron.
neutron và electron.
Nguyên tử trung hoà về điện vì
được cấu tạo nên bởi các hạt không mang điện.
có tổng số hạt electron bằng tổng số hạt neutron.
có tổng số hạt electron bằng tổng số hạt proton.
có tổng số hạt proton bằng tổng số hạt neutron.
Số hiệu nguyên tử cho biết thông tin nào sau đây?
Số khối.
Số electron.
Số neutron.
Nguyên tử khối.
Nguyên tố hóa học là tập hợp những nguyên tử có cùng
số khối.
số hạt neutron.
số hạt proton.
số hạt neutron và số hạt proton.
Các đồng vị của cùng một nguyên tố hóa học là những nguyên tử có
cùng số proton nhưng khác nhau về số neutron.
cùng số neutron nhưng khác nhau về số proton.
cùng tổng số proton và neutron nhưng khác nhau về số electron.
cùng số electron nhưng khác nhau về tổng số proton và neutron.
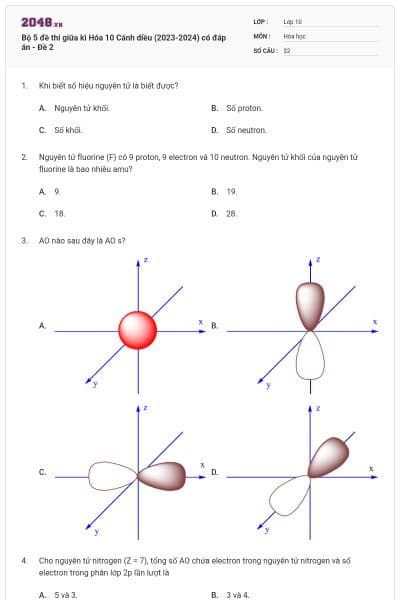
Orbital nguyên tử là
đám mây chứa electron có dạng hình cầu.
đám mây chứa electron có dạng hình số tám nổi.
khu vực không gian xung quanh hạt nhân nguyên tử mà tại đó xác suất tìm thấy electron trong khu vực đó là lớn nhất.
quỹ đạo chuyển động của electron quay quanh hạt nhân có kích thước năng lượng xác định.
Lớp M có số phân lớp electron là
1.
2.
3
4.
Phân lớp 4f có số electron tối đa là
6.
18.
14.
10.
Nguyên tử fluorine (Z = 9) có cấu hình electron là
1s22s22p3.
1s22s32p4.
1s22s22p5.
1s22s12p6.
Electron thuộc lớp nào sau đây liên kết chặt chẽ với hạt nhân nhất?
Lớp N.
Lớp M.
Lớp K.
Lớp L.
Nguyên tử của nguyên tố M có cấu hình electron là 1s22s22p3. Số electron độc thân của M là
1.
2.
0.
3.
Số thứ tự của ô nguyên tố bằng
số hiệu nguyên tử của nguyên tố đó.
số lớp electron của nguyên tử nguyên tố đó.
số electron lớp ngoài cùng của nguyên tử nguyên tố đó.
tổng số electron lớp ngoài cùng và phân lớp sát lớp ngoài cùng của nguyên tử nguyên tố đó.
Chu kì 3 của bảng hệ thống tuần hoàn có số nguyên tố là
2 nguyên tố.
8 nguyên tố.
10 nguyên tố.
18 nguyên tố.
Mendeleev sắp xếp các nguyên tố hoá học trong bảng tuần hoàn dựa theo quy luật về
số hiệu nguyên tử.
khối lượng nguyên tử.
cấu hình electron.
số khối.
Khối lượng của nguyên tử calcium là 66,5495.10–27kg. Khối lượng của nguyên tử calcium theo amu là
40,000.
66,133.10–51.
40,078.
40,078.10–3.
Nguyên tử nitrogen có 7 proton, 8 neutron. Khối lượng của các electron chiếm bao nhiêu % khối lượng nguyên tử nitrogen? (Biết mp ≈ mn ≈ 1u; me ≈ 0,00055u).
0,0257%.
0,257%.
0,0275%.
2,566%.
Nguyên tử fluorine có 9 electron, 10 neutron, kí hiệu nguyên tử của nguyên tố fluorine là
Cho các phát biểu sau:
(1) Trong một nguyên tử luôn có số proton bằng số electron và bằng số hiệu nguyên tử.
(2) Tổng số proton và số neutron trong một hạt nhân nguyên tử được gọi là số khối.
(3) Tất cả các nguyên tử nguyên tố khí hiếm đều có số electron ở lớp ngoài cùng bằng 8.
(4) Đồng vị là các nguyên tử có cùng số proton nhưng khác nhau về số neutron.
Số phát biểu không đúng là
1.
2.
3.
4.
Phát biểu nào sau đây đúng?
Số phân lớp electron có trong lớp N là 3.
Số phân lớp electron có trong lớp M là 4.
Số orbital có trong lớp N là 15.
Số orbital có trong lớp M là 9.
Tổng số hạt cơ bản của nguyên tử X là 10. Cấu hình electron của nguyên tử của X là
1s22s1.
1s12s2.
1s22s22p6.
1s22s2.
Neon có ba đồng vị với tỉ lệ % số nguyên tử tương ứng là 20Ne (90,9%), 21Ne (0,3%), 22Ne (8,8%). Nguyên tử khối trung bình của neon là
20,200.
21,000.
20,179.
20,100.
Nguyên tử của nguyên tố R có tổng số electron trên các phân lớp s là 7. Số trường hợp nguyên tử R thỏa mãn điều kiện đó là
1.
2.
3.
4.
Cấu hình electron của nguyên tử nguyên tố X có dạng 1s22s22p63s23p5. Phát biểu nào sau đây là sai?
X có 17 electron trong nguyên tử.
X là một phi kim.
Trong bảng tuần hoàn, X thuộc nhóm VA.
X thuộc chu kì 3 trong bảng tuần hoàn.
Các electron của nguyên tử nguyên tố X được phân bố trên ba lớp, lớp thứ ba có 5 electron. Trong bảng tuần hoàn, X thuộc ô
6.
8.
15.
16.
Nguyên tố X có Z = 16. Số electron ở lớp ngoài cùng của nguyên tử nguyên tố X là
4.
6.
7.
3.
Cho cấu hình electron nguyên tử của các nguyên tố sau:
(X) 1s22s22p63s2;
(Y) 1s22s22p63s23p64s1;
(Z) 1s22s22p63s23p3;
(T) 1s22s22p63s23p63d84s2.
Dãy cấu hình electron của các nguyên tử nguyên tố kim loại là
X, Z, T.
X, Y, T.
Y, Z, T.
X, Y, Z.
(1 điểm): Nguyên tử của nguyên tố R có tổng số hạt proton, neutron và electron là 116, trong đó tổng số hạt mang điện nhiều hơn số hạt không mang điện là 24.
Xác định thành phần các hạt cấu tạo nên nguyên tử R.
(1 điểm): Cho các nguyên tử nguyên tố sau: Ne (Z = 10); K (Z = 19).
Xác định vị trí của F và K trong bảng tuần hoàn (có giải thích ngắn gọn).
(0,5 điểm): X là một phi kim có khối lượng nguyên tử là 58,94755.10-24 gam. Trong tự nhiên, X có hai đồng vị hơn kém nhau 2 neutron. Tỉ lệ phần trăm số nguyên tử của đồng vị nhẹ hơn trong tự nhiên là 75%.
Tính phần trăm về khối lượng của đồng vị nặng trong hydroxide cao nhất của X là HXO4. (cho nguyên tử khối của O = 16, H = 1)
(0,5 điểm): Biết X ở chu kì 3 và Y ở chu kì 2 trong bảng tuần hoàn các nguyên tố hóa học. Tổng số electron lớp ngoài cùng của X và Y là 10. Ở trạng thái cơ bản số electron p của X nhiều hơn số electron p của Y là 8.
Xác định X, Y thuộc nhóm nào trong bảng tuần hoàn?