Bộ 3 đề thi giữa kì 1 Hóa 10 Cánh diều cấu trúc mới có đáp án - Đề 2
28 câu hỏi
PHẦN I. Câu trắc nghiệm nhiều phương án lựa chọn. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
Trong hạt nhân nguyên tử có chứa những loại hạt nào?
proton, neutron.
electron, neutron.
electron, proton.
proton, neutron, electron.
Trong thành phần cấu tạo nên nguyên tử, hạt nào sau đây mang điện tích âm?
Proton.
Hạt nhân.
Electron.
Neutron.
Khối lượng của một proton bằng
0,00055 amu.
0,1 amu.
1 amu.
0,0055 amu.
Khẳng định nào sau đây đúng?
Kích thước nguyên tử xấp xỉ bằng kích thước hạt nhân.
Kích thước nguyên tử bằng khoảng 3 đến 5 lần kích thước hạt nhân.
Kích thước nguyên tử bằng khoảng 10 lần kích thước hạt nhân.
Kích thước nguyên tử bằng khoảng 10 000 đến 100 000 lần kích thước hạt nhân.
Nguyên tố hóa học là những nguyên tử có cùng
số neutron.
nguyên tử khối.
số khối.
số proton.
Số hiệu nguyên tử (Z) của nguyên tố hóa học không bằng giá trị nào sau đây?
Số hạt proton.
Số hạt electron.
Số đơn vị điện tích dương.
Số hạt neutron.
Cho kí hiệu nguyên tử \[{}_7^{15}{\rm{X}}\]. Số khối của X bằng
7.
8.
15.
22.
Cặp nguyên tử nào sau đây là đồng vị của nhau?
\({}_6^{12}{\rm{X}},{}_5^{10}{\rm{Y}}\).
\({}_1^1{\rm{M}},{}_2^4{\rm{G}}\).
\({}_8^{16}{\rm{D}},{}_8^{17}{\rm{E}}\).
\({}_9^{17}{\rm{L}},{}_1^3{\rm{T}}\).
Từ hai đồng vị hydrogen (\[_1^1H\] và \[_1^2H\]) và hai đồng vị chlorine (\[_{17}^{35}Cl\] và \[_{17}^{37}Cl\]), số loại phân tử HCl có thể được tạo thành là
2.
3.
4.
5.
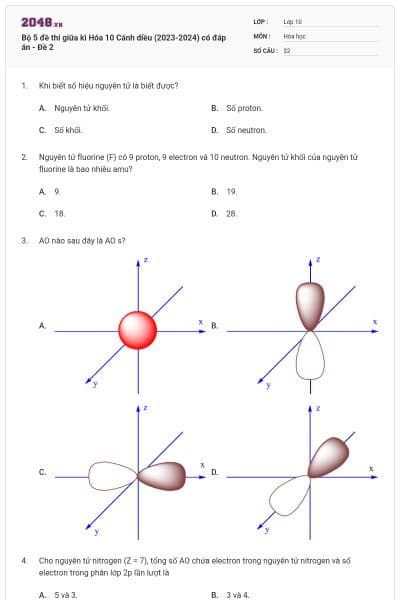
AO nào có dạng hình cầu?
AO px.
AO pz.
AO s.
AO py.
Lớp K có mấy phân lớp?
1.
3.
5.
7.
Cấu hình electron lớp ngoài cùng nào sau đây là của nguyên tử kim loại?
1s2.
2s22p6.
3s23p5.
3s2.
Nguyên tử X có 21 electron ở lớp vỏ. Trong bảng tuần hoàn, nguyên tố X thuộc chu kì nào?
4.
2.
5.
3.
Số nguyên tố trong chu kì 3 và chu kì 5 của bảng tuần hoàn lần lượt là
8 và 18.
8 và 8.
18 và 18.
18 và 32.
Chu kì là tập hợp các nguyên tố, mà nguyên tử của các nguyên tố này có cùng
số electron.
số lớp electron.
số electron hóa trị
số electron ở lớp ngoài cùng.
Nguyên tố A có số hiệu nguyên tử là 18, vị trí của A trong bảng tuần hoàn là
chu kì 3, nhóm VIB.
chu kì 3, nhóm VIIIA.
chu kì 3, nhóm VIA.
chu kì 3, nhóm VIIIB.
Nguyên tố X ở chu kì 3, nhóm IA của bảng tuần hoàn. Cấu hình electron của nguyên tử nguyên tố X là
1s²2s²2p6.
1s²2s²2p3s²3p¹.
1s²2s²2p3s³.
1s²2s²2p63s1.
Nguyên tử của nguyên tố X có electron cuối cùng điền vào phân lớp 3p1. Nguyên tử của nguyên tố Y có electron cuối cùng điền vào phân lớp 3p3. Số thứ tự ô của X và Y trong bảng tuần hoàn lần lượt là
13 và 15.
12 và 14.
13 và 14.
12 và 15.
PHẦN II. Câu trắc nghiệm đúng sai. Thí sinh trả lời từ câu 1 đến câu 4. Trong mỗi ý a), b), c), d) ở mỗi câu, thí sinh chọn đúng hoặc sai. (Đ – S)
Nguyên tố hydrogen là một trong những nguyên tố phổ biến trong vũ trụ.
a. Hydrogen là nguyên tố duy nhất có đồng vị mà hạt nhân chỉ tạo nên bởi các hạt p.
b. Hydrogen là nguyên tố có đồng vị nhẹ nhất.
c. Hydrogen được xem là nguồn năng lượng xanh của tương lai.
d. Nước chỉ tạo nên bởi các đồng vị 1H.
Một nguyên tử của một nguyên tố X có 2 electron ở lớp thứ nhất, 8 electron ở lớp thứ 2 và 8 electron ở lớp thứ 3.
a. Số hiệu nguyên tử của nguyên tố X là 18.
b. Tổng số electron trong các orbital s của X là 2.
c. Tổng số electron trong các orbital p của X là 6.
d. Chưa thể xác định được số lượng neutron trong hạt nhân nguyên tử X.
Cho các nguyên tử sau: \[{}_{17}^{35}A;\,{}_7^{14}B;\,{}_6^{12}C;\,{}_{19}^{39}D;\,{}_{17}^{37}E;\,{}_6^{14}F.\]
a. Nguyên tử của nguyên tố B và F có cùng số khối.
b. A, E thuộc cùng một nguyên tố hoá học.
c. Có 3 cặp chất là đồng vị của nhau.
d. D và E có cùng số neutron trong nguyên tử.
X là một nguyên tố chu kì 2, phân lớp ngoài cùng của nguyên tử nguyên tố X có 3 electron độc thân.
a. X là nguyên tố nhóm IIIA hoặc IIIB.
b. Số electron lớp ngoài cùng của X là 3.
c. Số electron lớp ngoài cùng của X là 5.
d. X là một kim loại.
Phần III. Câu hỏi trắc nghiệm yêu cầu trả lời ngắn. Thí sinh trả lời từ câu 1 đến câu 6.
Cho biết, khối lượng của một proton bằng 1 amu, của một electron bằng 0,00055 amu. Tỉ lệ về khối lượng giữa hạt proton và hạt electron có giá trị bằng khoảng?
Nguyên tử nguyên tố X có tổng các electron trên phân lớp p là 7. Vậy X thuộc loại nguyên tố nào?
Trong tự nhiên potassium (kí hiệu là: K) có hai đồng vị \[{}_{19}^{39}K\]và \[{}_{19}^{41}K.\]Thành phần phần trăm về khối lượng của \[{}_{19}^{39}K\]có trong KClO4 là (cho biết nguyên tử khối trung bình của K là 39,13; O là 16 và Cl là 35,5)?
Hợp chất ion XY được sử dụng để bảo quản mẫu tế bào trong viện nghiên cứu dược phẩm và hóa sinh vì ion Y- ngăn cản sự thủy phân của glycogen. Trong phân tử XY, số electron của anion bằng số electron của cation và tổng số electron của XY là 20. Biết trong mọi hợp chất, Y chỉ có một hoá trị duy nhất. Hãy xác định vị trí của X, Y trong bảng tuần hoàn?
Cho cấu hình electron nguyên tử của một số nguyên tố như sau: \([{\rm{Ne}}]3\;{{\rm{s}}^2},[{\rm{Ar}}]3\;{{\rm{d}}^{10}}4\;{{\rm{s}}^1},\)\[[{\rm{Ar}}]3\;{{\rm{d}}^{10}}4\;{{\rm{s}}^2}4{{\rm{p}}^5},[{\rm{He}}]2\;{{\rm{s}}^2}2{{\rm{p}}^6},[{\rm{Ar}}]3\;{{\rm{d}}^7}4\;{{\rm{s}}^2}.\] Số nguyên tố thuộc nhóm A trong bảng tuần hoàn là?
Carbon và các nguyên tố phi kim khác nằm ở vị trí nào trong bảng tuần hoàn?