Bộ 3 đề thi cuối kì 1 Hóa 11 Kết nối tri thức cấu trúc mới có đáp án - Đề 3
28 câu hỏi
Trong các phát biểu sau, phát biểu nào không đúng?
NH3 là chất khí không màu, tan nhiều trong nước.
Khí NH3 nặng hơn không khí.
Khí NH3 dễ hoá lỏng, tan nhiều trong nước.
Phân tử NH3 chứa các liên kết cộng hoá trị phân cực.
Ứng dụng nào sau đây không là ứng dụng của sulfur?
Lưu hoá cao su.
Sản xuất diêm, thuốc nổ.
Sản xuất nitric acid.
Sản xuất thuốc trừ sâu, thuốc diệt nấm.
Ở nhiệt độ thường, nitrogen khá trơ về mặt hoạt động hóa học là do
nitrogen có bán kính nguyên tử nhỏ.
nitrogen có độ âm điện lớn.
phân tử nitrogen có liên kết ba bền vững.
phân tử nitrogen không phân cực.
Chất nào sau đây là dẫn xuất của hydrocarbon?
CO2.
CH4.
CH3Cl.
HCN.
Thành phần chính của quặng pyrite là
PbS.
FeS2.
CaSO4.
BaSO4.
Cho phản ứng sau: 2C(s) + O2(g) ⇌2CO(g). Biểu thức hằng số cân bằng KC của phản ứng là
KC = \(\frac{{{{\left[ {CO} \right]}^2}}}{{{{\left[ C \right]}^2}.\left[ {{O_2}} \right]}}\)
KC = \(\frac{{{{\left[ {CO} \right]}^2}}}{{\left[ {{O_2}} \right]}}\)
KC = \(\frac{{{{\left[ C \right]}^2}.\left[ {{O_2}} \right]}}{{{{\left[ {CO} \right]}^2}}}\)
KC = \(\frac{{\left[ {{O_2}} \right]}}{{{{\left[ {CO} \right]}^2}}}\)
Lưu ý bắt buộc để đảm bảo an toàn khi sử dụng dung dịch sulfuric acid đặc là
bảo quản sulfuric acid trong lọ bằng chất dẻo.
đè chai đựng acid lên miệng cốc khi rót acid.
lượng acid dư thừa sau khi sử dụng phải đổ xuống cống thoát nước.
không đổ nước vào dung dịch acid đặc.
Nitric acid thể hiện tính acid khi tác dụng với chất nào sau đây?
S.
Mg.
Fe2O3.
FeO
Chất khí (X) tan trong nước tạo ra dung dịch làm quỳ tím hoá đỏ và khí (X) có thể được dùng làm chất tẩy màu. Khí (X) là
NH3.
CO2.
SO2.
O3.
Hợp chất nào sau đây không là hợp chất hữu cơ?
CH4.
HCN.
CH3CHO.
CH3Cl.
Phổ hồng ngoại là phương pháp vật lí rất quan trọng và phổ biến để nghiên cứu về
thành phần nguyên tố chất hữu cơ.
thành phần phân tử hợp chất hữu cơ.
cấu tạo hợp chất hữu cơ.
cấu trúc không gian hợp chất hữu cơ.
Phương pháp kết tinh được ứng dụng trong trường hợp nào dưới đây?
Tinh chế đường đỏ thành đường trắng.
Tách β – carotene từ nước ép cà rốt.
Nấu rượu để uống.
Ngâm rượu thuốc.
Các chất hữu cơ có tính chất hoá học tương tự nhau và thành phần phân tử hơn kém nhau một hay nhiều nhóm CH2 được gọi là các chất
đồng phân của nhau.
đồng đẳng của nhau.
đồng vị của nhau.
đồng khối của nhau.
Cho phản ứng thuận nghịch sau: NH3 + H2O ⇌
Trong phản ứng nghịch, theo thuyết Bronsted – Lowry chất nào là base?
NH3.
H2O.
OH−.
NH4+.
Phân biệt được dung dịch NH4NO3 và KNO3 bằng thuốc thử là dung dịch
NaCl.
NaNO3.
NaOH.
K2SO4.
Trong phản ứng với chất nào sau đây, nitrogen thể hiện tính khử?
H2.
O2.
NH3.
Mg.
Công thức hoá học nào sau đây phù hợp với thuyết cấu tạo hoá học?
CH3 – CH2 = OH.
CH3–O=CH–CH3.
CH3 – CH2 – CH2 – N.
CH3CH2Cl.
Để phân biệt hai dung dịch NaCl và K2SO4 có thể dùng thuốc thử là
BaSO4.
BaCl2.
BaCO3.
HNO3.
Cho các nhận định sau:
a. CH2Cl2, CH2Br-CH2Br, CHCl3, CH3COOCH3, C6H5CH3 đều là dẫn xuất của hydrocabon.
b. CH2Cl2, CH2=CH-CHO, CH3COOH, CH2=CH2 đều là hợp chất hữu cơ.
c. CHBr3, CH2=CH-COOCH3, C6H5OH, C2H5OH, (CH3)3N đều là hợp chất vô cơ.
d. Trong dãy CH3OH, CH2=CH-Cl, C6H5ONa, CH≡C-CH3 có một chất là hydrocarbon.
Sulfur dioxide có thể tham gia những phản ứng sau:
(1) SO2 + Br2 + 2H2O H2SO4 + 2HBr
(2) SO2 + 2H2S 3S + 2H2O
a. Phản ứng (1): SO2 là chất khử, Br2 là chất oxi hóa.
b. Phản ứng (2): SO2 là chất oxi hóa, H2S là chất khử.
c. Phản ứng (2): SO2 là vừa là chất khử, vừa là chất oxi hóa.
d. Phản ứng (1): Br2 là chất oxi hóa; phản ứng (2): H2S là chất khử.
Sự cố tràn dầu trên biển gây thiệt hại rất lớn về kinh tế và môi trường. Để thu hồi dầu tràn, người ta dùng hệ thống phao để gom dầu tràn vào một khu vực, sau đó hút vào các bồn lớn trên tàu. Để thu được dầu, người ta li tâm để tách hỗn hợp lỏng thành hai lớp: lớp nước và lớp dầu. Mở van xả để loại bỏ nước phía dưới, thu được lớp dầu.
a. Dầu nhẹ hơn nước và không tan trong nước.
b. Li tâm để tách hỗn hợp thành 2 lớp chất lỏng dựa vào sự không tan vào nhau và khối lượng riêng khác nhau của dầu và nước.
c. Trong quá trình trên đã sử dụng kĩ thuật chiết lỏng – lỏng.
d. Có thể chưng cất hỗn hợp dầu và nước để thu lấy dầu.
Cho các công thức cấu tạo sau
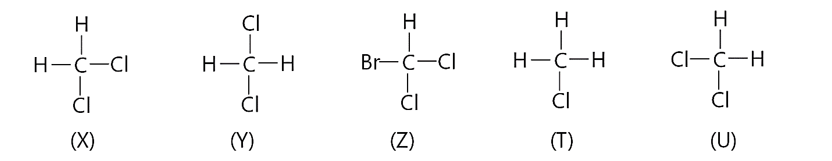
a. X, Y, Z cùng biểu diễn một chất.
b. X, T, U là đồng đẳng của nhau.
c. X, Y, U có cùng công thức phân tử CH2Cl2.
d. Y, T, U là đồng phân của nhau.
Khí SO2 do các nhà máy thải ra là nguyên nhân chính trong việc gây ô nhiễm môi trường. Theo quy chuẩn kĩ thuật quốc gia về chất lượng không khí xung quanh (QCVN 05:2013/BTNMT) thì nếu lượng SO2 vượt quá 350 μg/m3 không khí đo trong 1 giờ ở một thành phố thì coi như không khí bị ô nhiễm. Nếu người ta lấy 50 lít không khí trong 1 giờ ở một thành phố và phân tích thấy có 0,012 mg SO2 thì nồng độ SO2 (μg/m3) ở khu vực đó là?
Một hợp chất có công thức cấu tạo:
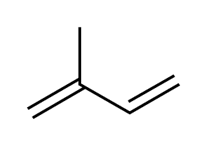
Hợp chất này có tổng số bao nhiêu nguyên tử carbon và hydrogen?
Để xác định nồng độ của một dung dịch HCl, người ta đã tiến hành chuẩn độ bằng dung dịch NaOH 0,1 M. Để chuẩn độ 10 mL dung dịch HCl này cần 15 mL dung dịch NaOH. Xác định nồng độ của dung dịch HCl trên
Cho các chất: Ag, CuO, KCl, Mg, KOH, S, Na2CO3, tổng số chất vừa tác dụng với dung dịch H2SO4 loãng, vừa tác dụng với dung dịch H2SO4 đặc, nóng là?
Acetone là một hợp chất hữu cơ dùng để làm sạch dụng cụ trong phòng thí nghiệm, tẩy rửa sơn móng tay…. Kết quả phân tích nguyên tố của acetone như sau: 62,07% C; 27,59% O về khối lượng, còn lại là hydrogen. Biết phân tử khối của acetone được xác định thông qua phổ khối lượng dưới đây, số lượng các nguyên tử có trong 1 phân tử acetone là?
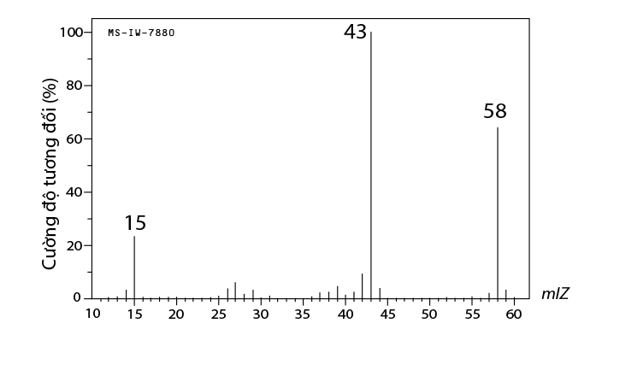
Cho 4 lít N2 và 14 lít H2 vào bình kín rồi nung nóng với xúc tác thích hợp để phản ứng xảy ra, sau phản ứng thu được 16,4 lít hỗn hợp khí (các khí đo ở cùng điều kiện nhiệt độ và áp suất). Thể tích khí amoniac thu được là?








