30 bài tập Liên kết hóa học có đáp án
30 câu hỏi
PHẦN I. Câu trắc nghiệm nhiều phương án lựa chọn. Mỗi câu hỏi học sinh chỉ chọn một phương án.
Phân tử nào sau đây có liên kết cộng hóa trị không phân cực?
HCl.
SO2.
HBr.
N2.
Trong phân tử carbon dioxide (O=C=O) số liên kết ![]() và liên kết
và liên kết ![]() lần lượt là
lần lượt là
0 và 4.
2 và 2.
3 và 1.
4 và 0.
Cho bảng số liệu sau:
Chất | Nước ( | Hydrogen sulfide ( |
Nhiệt độ sôi | 100,0 | - 60,7 |
Phát biểu nào sau đây sai?
Liên kết O – H trong phân tử ![]() kém phân cực hơn liên kết S – H trong phân tử
kém phân cực hơn liên kết S – H trong phân tử ![]()
Số liên kết trong phân tử ![]() bằng số liên kết trong phân tử
bằng số liên kết trong phân tử ![]()
Trong phân tử ![]() và phân tử
và phân tử ![]() chỉ có các liên kết cộng hóa trị.
chỉ có các liên kết cộng hóa trị.
Do có liên kết hydrogen giữa các phân tử nên ![]() có nhiệt độ sôi cao hơn H2S.
có nhiệt độ sôi cao hơn H2S.
Chất nào sau đây không tạo được liên kết hydrogen giữa các phân tử?
H2O.
NH3.
HF.
CH4.
Cho các hình biểu diễn sự xen phủ orbital nguyên tử để tạo liên kết hóa học sau:
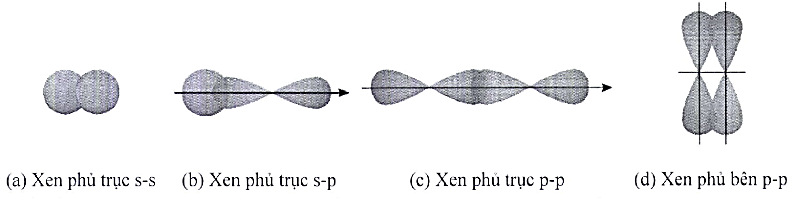
Biết số hiệu các nguyên tử của H, F và S lần lượt là 1, 9 và 16. Sự tạo liên kết trong các phân tử H2S và F2 theo kiểu xen phủ tương ứng là
(a) và (c).
(b) và (c).
(b) và (d).
(c) và (d).
Vì sao các nguyên tử Ne (Z = 10) và Ar (Z = 18) hiếm khi tạo thành hợp chất?
Vì chúng có lớp electron ngoài cùng đã bão hoà.
Vì chúng có phân lớp electron bên trong đã được được điền đầy đủ.
Vì bán kính nguyên tử của chúng rất nhỏ.
Vì mỗi nguyên tử đã có đủ 8 electron.
Phosphorus là nguyên tố thuộc chu kì 3 và nhóm VA trong bảng tuần hoàn. Phosphorus có xu hướng nhường hay nhận bao nhiêu electron để đạt được cấu hình electron bền vững?
Nhường 5 electron.
Nhận 3 electron.
Nhường 3 electron.
Nhận 5 electron.
Phân tử nào sau đây chứa nguyên tử không tuân theo quy tắc octet?
Biết: H (Z = 1), B (Z = 5), C (Z = 6), N (Z = 7), O (Z = 8).
![]()
![]()
![]()
![]()
Magnesium oxide thường được sử dụng để lót bên trong các lò công nghiệp vì có nhiệt độ nóng chảy cao. Loại liên kết hay tương tác hoá học trong magnesium oxide là
liên kết ion.
liên kết cộng hoá trị.
liên kết hydrogen.
tương tác van der Waals
Trong các phân tử ![]() số lượng phân tử chỉ chứa các liên kết cộng hoá trị không phân cực là
số lượng phân tử chỉ chứa các liên kết cộng hoá trị không phân cực là
2.
3.
4.
5.
Số lượng electron tham gia hình thành liên kết đơn, đôi và ba lần lượt là
1, 2, 3.
2, 4, 6.
1, 3, 5.
2, 3, 4.
Trong số các cặp nguyên tố sau, cặp nguyên tố nào có nhiều khả năng tạo thành liên kết cộng hoá trị nhất?
K và Cl.
C và O.
Al và Mg.
K và Na.
Giữa các nguyên tử khí hiếm Ar, có thể hình thành loại liên kết hay tương tác hoá học nào?
Liên kết ion.
Liên kết cộng hoá trị.
Liên kết hydrogen.
Tương tác van der Waals.
Trong các cặp nguyên tố sau, cặp nguyên tố nào có nhiều khả năng tạo thành liên kết ion nhất?
Nitrogen và oxygen.
Carbon và hydrogen.
Sulfur và oxygen.
Sodium và oxygen.
Các nguyên tố F, Cl, Br và I đều thuộc nhóm VIIA và ở các chu kì tương ứng là 2, 3, 4 và 5. Liên kết cộng hoá trị trong phân tử HX (X là F, Cl, Br, I) nào phân cực mạnh nhất?
HF.
HCl.
HBr.
HI.
Cho bảng số lượng electron, neutron và proton của các phần tử (nguyên tử hoặc ion) sau:
Phần tử | Số electron | Số neutron | Số proton |
(a) | 8 | 8 | 8 |
(b) | 10 | 12 | 11 |
(c) | 19 | 20 | 19 |
(d) | 18 | 18 | 17 |
Những phần tử thuộc loại ion là
(a) và (d).
(a) và (b).
(c) và (d).
(b) và (d).
PHẦN II. Câu trắc nghiệm đúng sai. Trong mỗi ý a), b), c), d) ở mỗi câu, học sinh chọn đúng hoặc sai.
Các nguyên tố phổ biến thuộc nhóm halogen (VIIA) trong bảng tuần hoàn các nguyên tố hóa học gồm: F (Z = 9), Cl (Z = 17), Br (Z = 35) và I (Z = 53). Đơn chất halogen tồn tại dạng phân tử X2, giữa các phân tử X2 thường có tương tác với nhau.
Cho giá trị năng lượng liên kết X – X ở bảng sau:
Liên kết | F – F | Cl – Cl | Br – Br | I – I |
Năng lượng liên kết ( | 159 | 243 | 193 | 151 |
Năng lượng liên kết X – X càng lớn thì liên kết càng bền.
a. Liên kết giữa các nguyên tử trong ![]() là liên kết cộng hóa trị không phân cực.
là liên kết cộng hóa trị không phân cực.
b. Tương tác giữa các phân tử ![]() là tương tác van der Waals.
là tương tác van der Waals.
c. Cấu hình electron lớp ngoài cùng của nguyên tử X có dạng ![]()
d. Năng lượng liên kết Cl – Cl lớn nhất trong dãy trên vì Cl có bán kính nguyên tử nhỏ nhất.
Chỉ ra các nhận định Đúng/Sai trong các nhận định sau?
a. Các orbital p vừa có khả năng xen phủ tạo liên kết s vừa có khả năng xen phủ tạo liên kết p tuỳ thuộc vào kiểu xen phủ.
b. Liên kết cộng hoá trị không phân cực chỉ có thể tạo thành từ các nguyên tử của cùng một nguyên tố hoá học.
c. Tất cả các nguyên tử khi tham gia tạo thành liên kết cộng hoá trị đều thoả mãn quy tắc octet.
d. Hiệu độ âm điện giữa hai nguyên tử càng cao thì liên kết càng phân cực.
Cho các hợp chất sau: ![]()
a. Có 3 hợp chất ion.
b. ![]() là các hợp chất cộng hóa trị.
là các hợp chất cộng hóa trị.
c. Chỉ có NaCl là hợp chất ion.
d. Có 2 hợp chất ion là: CaO và NaCl.
Khi đun nóng dung dịch sodium chloride bão hòa, thu được tinh thể sodium chloride khan. Sau đó, nung nóng đến khoảng 800 °C thì tinh thể sodium chloride chảy lỏng.
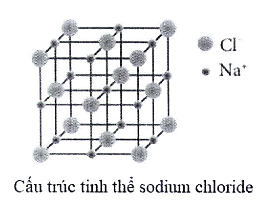
a. Quá trình hình thành tinh thể sodium chloride ở trên được gọi là sự kết tinh.
b. Quá trình hình thành tinh thể sodium chloride ở trên là quá trình sắp xếp lại các ion ![]() từ chuyển động tự do thành cấu trúc có trật tự trong tinh thể.
từ chuyển động tự do thành cấu trúc có trật tự trong tinh thể.
c. Trong tinh thể sodium chloride, xung quanh 1 ion ![]() có 6 ion
có 6 ion ![]() gần nhất.
gần nhất.
d. Tinh thể sodium chloride nóng chảy ở khoảng 800 °C, chứng tỏ lực liên kết giữa các ion trong tinh thể là yếu.
Độ âm điện của N và H tương ứng là 3,04 và 2,2.
a. Liên kết H−N là liên kết cộng hoá trị không phân cực.
b. Hợp chất ![]() có nhiệt độ nóng chảy, nhiệt độ sôi cao.
có nhiệt độ nóng chảy, nhiệt độ sôi cao.
c. Cặp electron dùng chung trong liên kết H−N lệch về phía nguyên tử N.
d. ![]() là hợp chất ion.
là hợp chất ion.
Liên kết được tạo nên từ sự xen phủ trục của hai AO gọi là liên kết sigma. Liên kết được tạo nên từ sự xen phủ bên của hai AO gọi là liên kết pi.
a. Các AO s chỉ có khả năng xen phủ tạo liên kết s.
b. Các AO p không có khả năng xen phủ tạo liên kết s.
c. Liên kết s bền vững hơn liên kết p.
d. Liên kết s có thể tạo thành từ sự xen phủ trục của hai AO khác loại.
PHẦN III. Câu trắc nghiệm yêu cầu trả lời ngắn
Có bao nhiêu hợp chất ion trong dãy các chất sau: NH3, CaO, KCl, CH4, NaOH?
Trong công thức ![]() tổng số cặp electron lớp ngoài cùng của C và S chưa tham gia liên kết là?
tổng số cặp electron lớp ngoài cùng của C và S chưa tham gia liên kết là?
Cho các hợp chất: ![]() Chất nào không thỏa mãn quy tắc octet?
Chất nào không thỏa mãn quy tắc octet?
Không cần sử dụng hiệu độ âm điện, có bao nhiêu phân tử trong số các phân tử sau có liên kết cộng hóa trị: ![]() và HI?
và HI?
Tổng số các phân tử không có cực trong số các phân tử sau: ![]() và
và ![]() là bao nhiêu?
là bao nhiêu?
Cho các phân tử sau: ![]() và
và ![]() Có bao nhiêu nguyên tử trong các phân tử trên đạt cấu hình electron bền của khí hiếm neon?
Có bao nhiêu nguyên tử trong các phân tử trên đạt cấu hình electron bền của khí hiếm neon?
X, Y, Z là các hợp chất ion thuộc trong số các chất sau: NaF, MgO và ![]() Nhiệt độ nóng chảy của các hợp chất X, Y, Z được thể hiện qua biểu đồ:
Nhiệt độ nóng chảy của các hợp chất X, Y, Z được thể hiện qua biểu đồ:
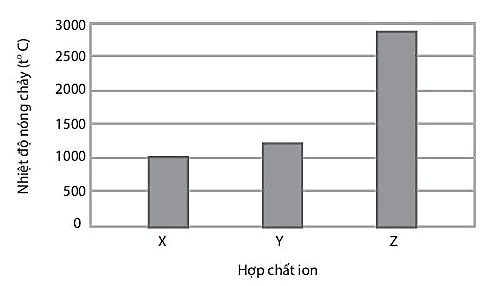
Hợp chất X là?
Cho số hiệu của nguyên tố N và O lần lượt là 7 và 8. Biết rằng hóa trị của nguyên tố N trong phân từ HNO3 bằng tổng số liên kết ![]() và liên kết
và liên kết ![]() mà nguyên tử N tạo thành khi liên kết với các nguyên tử xung quanh. Trong phân từ HNO3, nguyên tử N không liên kết với nguyên tử H mà liên kết với 3 nguyên tử O. Từ đó viết được công thức Lewis phù hợp của phân tử HNO3 với hóa trị của N là n. Giá trị của n là bao nhiêu?
mà nguyên tử N tạo thành khi liên kết với các nguyên tử xung quanh. Trong phân từ HNO3, nguyên tử N không liên kết với nguyên tử H mà liên kết với 3 nguyên tử O. Từ đó viết được công thức Lewis phù hợp của phân tử HNO3 với hóa trị của N là n. Giá trị của n là bao nhiêu?








