(Đúng Sai) 25 bài tập Hóa 10 Kết nối tri thức Bài 22: Nhóm Halogen Halide. Muối Halide có lời giải - Phần 02
48 câu hỏi
Cho các phát biểu khi nói về ứng dụng hiện nay của một số hydrogen halide và hydrohalic acid.
a. Lượng lớn hydrochloric acid sử dụng trong sản xuất nhựa, phân bón, thuốc nhuộm,…
b. Trong công nghiệp, hydrofluoric acid dùng tẩy rửa các oxide của sắt trên bề mặt của thép.
c. Hydrofluoric acid hoặc hydrogen fluoride phản ứng với chlorine dùng để sản xuất fluorine.
d. Hydrochloric acid được dùng làm nguyên liệu để sản xuất hợp chất chống dính teflon.
Thuỷ tinh vốn cứng, trơn và khá trơ về mặt hoá học nên việc chạm khắc là điều không đơn giản. Muốn khắc các hoa văn, cần phủ lên bề mặt thuỷ tinh một lớp paraffin, thực hiện chạm khắc các hoa văn lên lớp paraffin, để phần thuỷ tinh cần khắc lộ ra. Nhỏ dung dịch hydrofluoric acid hoặc hỗn hợp CaF2 và H2SO4 đặc lên lớp paraffin đó, phần thuỷ tinh cần chạm khắc sẽ bị ăn mòn, tạo nên những hoa văn trên vật dụng cần trang trí.
a. HF là acid mạnh và có tính chất đặc biệt là ăn mòn thuỷ tinh.
b. Phương trình hoá học của phản ứng ăn mòn thủy tinh là: 4HF + SiO2 ![]() SiF4 + 2H2O.
SiF4 + 2H2O.
c. Để bảo quản hydrofluoric acid, người ta chứa trong bình bằng nhựa.
d. Tất cả các hydrohalic acid đều có khả năng ăn mòn thủy tinh.
Trong các hydrogen halide thì hydrogen fluoride có nhiều ứng dụng phổ biến.
a. Trong công nghiệp, HF được dùng để khắc chữ lên bề mặt thủy tinh.
b. Từ hydrogen fluoride người ta sản xuất hydrochlorofluorocarbon (HCFC) sử dụng cho các hệ thống làm lạnh.
c. Hydrogen halide được dùng để điều chế cryolite (Na3AlF6), đây là “chất chảy” trong quá trình sản xuất nhôm (aluminium).
d. Trong dạ dày của người có HF với nồng độ 10–4 đến 10–2 mol.L–1, làm môi trường tiêu hóa thức ăn.
Mỗi phát biểu sau đây là đúng hay sai?
a. Trong công nghiệp, một lượng nhỏ hydrogen chloride được sản xuất từ các đơn chất:
H2 + Cl2 ![]() 2HCl
2HCl
b. Trong công nghiệp, hydrogen fluoride (HF) được sản xuất khi cho sulfuric acid đặc (H2SO4) tác dụng với quặng fluorite (CaF2):
CaF2 + H2SO4 (đặc) ![]() CaSO4 + 2HF
CaSO4 + 2HF
c. Trong phòng thí nghiệm, cho muối sodium chloride rắn (NaCl) tác dụng với sulfuric acid đặc (H2SO4), thu được khí hydrogen chloride (HCl):
NaCl + H2SO4 (đặc) ![]() NaHSO4 + HCl
NaHSO4 + HCl
d. Trong phòng thí nghiệm, hydrogen halide (HBr và HI) có thể được điều chế bằng phương pháp sulfate: NaX + H2SO4 (đặc) ![]() NaHSO4 + HX.
NaHSO4 + HX.
Trong ion halide, các halogen có số oxi hoá thấp nhất là –1, do đó ion halide chỉ thể hiện tính khử trong phản ứng oxi hoá – khử.
a. Ion F– và Cl– không bị oxi hóa bởi dung dịch H2SO4 đặc.
b. Ion halide được sắp xếp theo chiều giảm dần tính khử là I–, Br–, Cl–, F–
c. Khi phản ứng với H2SO4 đặc, Br– có tính khử mạnh hơn ion I–.
d. Ion Br– và I– có thể khử H2SO4 loãng thành SO2, S, H2S tùy vào điều kiện phản ứng.
Mỗi phát biểu sau đây là đúng hay sai?
a. Muối NaCl thể hiện tính khử khi phản ứng với dung dịch H2SO4 đặc.
b. Muối NaBr khử được H2SO4 đặc thành sulfur dioxide (SO2).
d. Muối NaF khử được H2SO4 đặc thành sulfur (S).
c. Muối NaI khử được H2SO4 đặc thành hydrogen sulfide (H2S).
Hầu hết các muối halide đều tan trong nước, trừ một số muối không tan.
a. Các muối halide NaF, AgF, KBr, PbCl2 đều tan tốt trong nước ở điều kiện thường.
b. Cho dung dịch muối NaI vào dung dịch AgNO3 thấy xuất hiện kết tủa trắng.
c. Tính khử của các ion halide tăng theo chiều I– < Br– < Cl–.
d. Có thể nhận biết các ion halide bằng dung dịch silver nitrate (AgNO3).
Thực hiện thí nghiệm cho từ từ vài giọt dung dịch silver nitrate vào từng ống nghiệm như hình vẽ:
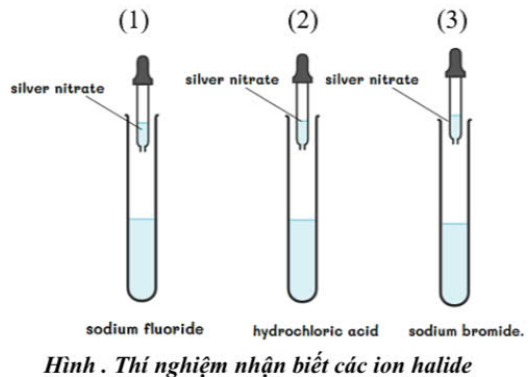
a. Thí nghiệm trên dùng để nhận biết các ion halide trong dung dịch.
b. Hiện tượng quan sát được là cả ba ống nghiệm đều xuất hiện kết tủa với các màu sắc khác nhau.
c. Ở ống nghiệm (2), nếu thay dung dịch hydrochloric acid bằng dung dịch sodium chloride thì kết quả thí nghiệm không thay đổi.
d. Thay dung dịch silver nitrate bằng dung dịch copper(II) sulfate, ta vẫn có thể nhận biết được các ion halide.
Trong phòng thí nghiệm, học sinh A dự định dùng dung dịch silver nitrate để phân biệt hai dung dịch sodium iodide và sodium bromide. Tuy nhiên, sau khi kiểm tra A thấy dung dịch silver nitrate đã hết. Em A đã đề xuất một quy trình tiến hành thí nghiệm thay thế để phân biệt được hai dung dịch trên như sau:
- Bước 1: Lấy 0,5 mL mỗi dung dịch cho vào các ống nghiệm riêng biệt.
- Bước 2: Nhỏ vào mỗi ống khoảng 3 giọt dung dịch nước chlorine, quan sát thấy dung dịch trong hai ống đều sẫm màu hơn.
- Bước 3: Thêm tiếp vào mỗi ống nghiệm 2 – 3 giọt hồ tinh bột, ống nghiệm nào chuyển màu xanh tím thì chứa NaI.
a. Quy trình thí nghiệm của em A chưa chính xác do ở bước (2) sự quan sát màu sắc là không rõ ràng.
b. Nếu đun sôi dung dịch ở 2 ống nghiệm sau bước (3) rồi để nguội ta sẽ thu được các dung dịch có màu sắc giống nhau.
c. Áp dụng quy trình thí nghiệm như trên có thể nhận biết được sodium iodide và sodium chloride, do hiện tượng quan sát được của ion iodide là không đổi.
d. Áp dụng quy trình thí nghiệm như trên có thể nhận biết được hydroiodic acid và hydrochloric acid.
Mỗi phát biểu nào sau đây là đúng hay sai?
a. Muối iodized dùng để phòng bệnh bướu cổ do thiếu iodine.
b. Chloramin-B được dùng phun khử khuẩn phòng dịch covid – 19.
d. Muối ăn là nguyên liệu sản xuất xút, chlorine, nước javel.
c. Nước Javel được dùng để tẩy màu và sát trùng.
Trong phòng thí nghiệm, một lượng nhỏ hydrogen chloride có thể được điều chế bằng phản ứng trực tiếp giữa dung dịch sodium chloride và dung dịch sulfuric acid đặc như hình dưới:
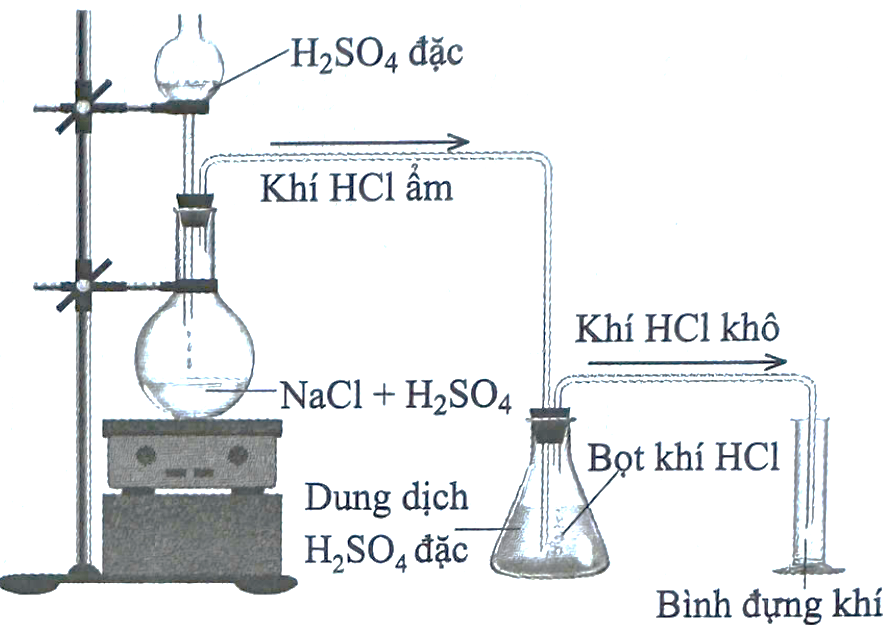
Tuy nhiên, phương pháp này không thể dùng để điều chế hydrogen bromide, do không thu được HBr từ phản ứng giữa NaBr và H2SO4 đặc:
2NaBr + 3H2SO4 ![]() 2NaHSO4 + Br2 + SO2 + 2H2O
2NaHSO4 + Br2 + SO2 + 2H2O
Mỗi phát biểu sau đây là đúng hay sai?
a. Anion Cl– không thể hiện tính khử khi tác dụng với sulfuric acid đặc nóng.
b. Tương tự HBr, HI cũng không thể điều chế bằng phương pháp này.
c. Trong thực tế, người ta điều chế HF cũng bằng thí nghiệm theo thiết kế ở hình trên.
d. Tính khử của anion Br– yếu hơn anion Cl–.
Hydrogen fluoride là chất có độc tính cao. Với kích thước phân tử nhỏ, HF dễ dàng thấm qua da, đến các mô sâu bên trong cơ thể và phá huỷ chúng. HF phá huỷ các mô xương thông qua việc tạo thành các kết tủa với Ca2+ và Mg2+ có trong cấu tạo xương; anion F từ HF sẽ làm vô hiệu hoá vai trò của một số enzyme trong cơ thể; khi lượng ion F lớn, nồng độ calcium trong máu nhanh chóng sụt giảm có thể gây ngưng tim đột ngột.
Calcium gluconate là một chất đặc hiệu trong sơ cấp cứu khi cơ thể bị phơi nhiễm với HF. Chất này có thể được sử dụng bằng cách bôi lên vùng da đã tiếp xúc với HF, kết hợp tiêm dưới da, tiêm vào mạch tuỳ vào mức độ ngộ độc.
Mỗi phát biểu dưới đây là đúng hay sai?
a. CaF2, MgF2 là những muối không tan trong nước
b. HCl cũng gây ngộ độc cho cơ thể theo cách tương tự như HF.
c. Dung dịch có nồng độ NaF cao cũng có thể gây hại cho tim nếu uống phải.
d. Calcium gluconate có thể làm giảm nồng độ fluoride trong cơ thể người ngộ độc.








