(Đúng Sai) 25 bài tập Hóa 10 Kết nối tri thức Bài 21: Nhóm Halogen (đơn chất) có lời giải - Phần 02
48 câu hỏi
Cho hai phản ứng hóa học sau đây:
(1) H2(g) + Cl2(g) ![]() 2HCl(g);
2HCl(g); ![]()
(2) 2Na(s) + Cl2(g) ![]() 2NaCl(s);
2NaCl(s); ![]()
a. Sản phẩm ở phản ứng (1) có chứa liên kết cộng hóa trị phân cực.
b. Sản phẩm ở phản ứng (2) có chứa liên kết ion
c. Phản ứng (2) khó xảy ra hơn phản ứng (1)
d. Cả hai phản ứng đều là phản ứng thu nhiệt
Xét các phản ứng hoá học: H2(g) + X2(g) ![]() 2HX(g) (X là các halogen). Cho bảng số liệu năng lượng liên kết H – X:
2HX(g) (X là các halogen). Cho bảng số liệu năng lượng liên kết H – X:
Năng lượng liên kết | H – F | H – Cl | H – Br | H – I |
(kJ.mol–1) | 565 | 427 | 363 | 295 |
a. Mức độ phản ứng với hydrogen giảm từ fluorine đến iodine nên tính oxi hóa của fluorine đến iodine cũng giảm dần.
b. H – I có năng lượng liên kết thấp nhất nên là phản ứng giữa H2 và I2 dễ xảy ra nhất.
c. Giá trị năng lượng HX giảm dần nên độ bền nhiệt cũng giảm dần từ HF đến HI.
d. Phản ứng giữa đơn chất hydrogen và đơn chất halogen đều là phản ứng một chiều.
Biến thiên enthalpy tạo thành chuẩn của các halogen halide được cho trong bảng sau:
Chất | HF(g) | HCl(g) | HBr(g) | HI(g) |
| –272,3 | –92,3 | –36,3 | 26,5 |
Mỗi phát biểu sau là đúng hay sai?
a. Phản ứng H2(g) + Cl2(g) ![]() 2HCl(g) có
2HCl(g) có ![]() .
.
b. Năng lượng liên kết HX giảm dần từ H – F đến H – I.
c. Phản ứng phân huỷ HI: 2HI(g) ![]() H2(g) + I2(g) là phản ứng toả nhiệt.
H2(g) + I2(g) là phản ứng toả nhiệt.
d. Trong phản ứng giữa halogen và hydrogen, nhiệt lượng toả ra tăng dần từ F2 đến I2.
Mỗi phát biểu sau khi nói về phản ứng của đơn chất nhóm VIIA với nước là đúng hay sai?
a. Các đơn chất nhóm VIIA vừa thể hiện tính oxi hóa, vừa thể hiện tính khử; mức độ phản ứng giảm dần từ fluorine đến iodine.
b. Fluorine phản ứng rất mạnh với nước tạo dung dịch có tính oxi hóa mạnh, có thể dùng để sát khuẩn.
c. Phản ứng của bromine hoặc chlorine với nước đều là phản ứng thuận nghịch.
d. Iodine tan rất ít và hầu như không phản ứng với nước
Chlorine dễ dàng tác dụng với dung dịch sodium hydroxide theo phản ứng như sau:
Cl2 + 2NaOH ![]() NaCl + NaClO + H2O
NaCl + NaClO + H2O
a. Phản ứng trên thuộc loại phản ứng trao đổ
b. Đun nóng phản ứng trên thì phản ứng xảy ra nhanh hơn và sản phẩm của phản ứng không thay đổi.
c. Trong phản ứng trên, chlorine vừa thể hiện tính oxi hóa, vừa thể hiện tính khử.
d. Nước Javel (chứa NaClO, NaCl và NaOH dư) được dùng làm chất tẩy rửa, khử trùng.
Mỗi phát biểu sau đây về tính chất hóa học của đơn chất halogen là đúng hay sai?
a. Khi cho khí fluorine vào dung dịch sodium chloride thì fluorine phản ứng với nước mà không phản ứng với sodium chloride.
b. Phản ứng giữa chlorine với nước tạo thành hydrochloric acid (HCl) và hypochlorous acid (HClO).
c. Phản ứng của iodine với hydrogen khó xảy ra hơn, cần phải có chất xúc tác và thực hiện ở nhiệt độ cao.
d. Các halogen mạnh hơn (trừ fluorine) có thể đẩy các halogen yếu hơn ra khỏi muối.
Mỗi phát biểu sau khi nói về phản ứng của đơn chất halogen với hydrogen là đúng hay sai?
a. Các phản ứng đều phát nhiệt mạnh và kèm hiện tượng nổ.
b. Phản ứng giữa fluorine với hydrogen diễn ra mãnh liệt nhất.
c. Điều kiện và mức độ phản ứng phù hợp với xu hướng giảm dần tính oxi hóa từ fluorine đến iodine.
d. Do hợp chất hydrogen iodide sinh ra kém bền (giá trị năng lượng liên kết nhỏ) nên phản ứng giữa iodine với hydrogen là phản ứng hai chiều.
Mỗi phát biểu sau là đúng hay sai?
a. Đơn chất chlorine có tính oxi hóa mạnh hơn đơn chất bromine và iodine.
b. Tương tác van der Walls của các đơn chất halogen tăng từ fluorine đến iodine đã góp phần làm tăng nhiệt độ sôi của chúng.
c. Thành phần của nước bromine gồm các chất: Br2, H2O, HBr và HBrO.
d. Hóa trị phổ biến của nguyên tố halogen là I
Người ta thường tách bromine trong rong biển bằng quá trình sục khí chlorine vào dung dịch chiết chứa ion bromide. Phương trình hoá học của phản ứng có thể được mô tả dạng thu gọn như sau: 2Br–(aq) + Cl2(aq) ![]() 2Cl– (aq) + Br2(aq)
2Cl– (aq) + Br2(aq)
Cho các số liệu enthalpy tạo thành chuẩn ![]() trong bảng dưới đây:
trong bảng dưới đây:
Br–(aq) | Cl–(aq) | Br2(aq) | Cl2(aq) |
–121,55 | –167,16 | –2,16 | –17,30 |
a. Phản ứng trên chứng minh chlorine có tính oxi hóa mạnh hơn bromine.
b. Nếu thay thế ion Br– bằng dung dịch I– thì phản ứng không xảy ra.
c. Giá trị tuyệt đối của biến thiên enthalpy phản ứng trên là 76,08 kJ.
d. Phản ứng trên không thuận lợi về năng lượng
Một học sinh thực hiện thí nghiệm và cho kết quả như sau:
- Bước 1: Lấy 2 mL dung dịch NaBr vào ống nghiệm, dung dịch không màu.
- Bước 2: Lấy tiếp 1 mL hexane vào ống nghiệm, lắc mạnh để quan sát khả năng hoà tan của hai chất lỏng. Nhận thấy hai chất lỏng không tan vào nhau và phân tách lớp.
- Bước 3: Thêm 1 mL nước Cl2 vào ống nghiệm, lắc đều rồi để yên. Quan sát thấy lớp chất lỏng phía trên có màu da cam.
a. Sau bước 2, hỗn hợp tách thành hai lớp trong đó NaBr nằm ở phần lớp trên
b. Sau bước 3, lớp chất lỏng phía trên có màu da cam là do Br2, Cl2 tan trong hexane.
c. Có thể thay dung dịch NaBr bằng dung dịch KBr nhưng vẫn không làm thay đổi hiện tượng của thínghiệm.
d. Thí nghiệm trên chứng minh tính oxi hóa của Cl2 yếu hơn Br2.
Trong phòng thí nghiệm, khí chlorine được điều chế, làm khô và thu vào bình theo sơ đồ dưới đây:
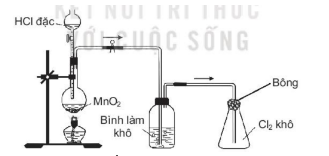
a. Có thể thay MnO2 bằng KMnO4 và không cần đun nóng.
b. Dung dịch chứa trong bình làm khô là NaOH đặc
d. Có thể nhận biết khí Cl2 khô thu được ở bình tam giác bằng màu sắc.
c. Bông tẩm dung dịch H2SO4 đặc có thể hạn chế khí Cl2 thoát ra môi trường.
Trong thí nghiệm ở hình dưới đây, người ta dẫn khí chlorine ẩm vào bình A có đặt một miếng giấy quì tím khô.
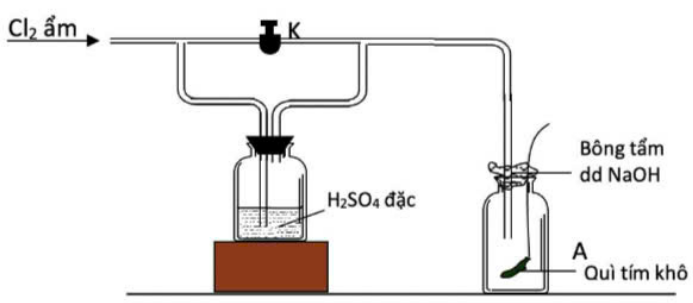
a. Khi đóng khóa K thì giấy quỳ tím bị nhạt màu
b. Khi mở khóa K thì giấy quỳ tím không bị nhạt màu
c. Vai trò của dung dịch NaOH ở bông tẩm trên miệng bình là hấp thụ khí Cl2, ngăn khí Cl2 khi đầy thoát ra ngoài.
d. Thí nghiệm trên chứng minh tính tẩy màu của khí Cl2 ẩm.








