Bộ 5 đề thi giữa kì Hóa 10 Kết nối tri thức (2023-2024) có đáp án - Đề 2
31 câu hỏi
Sự phân bố electron vào các lớp và phân lớp căn cứ vào
nguyên tử khối tăng dần.
số khối tăng dần.
mức năng lượng electron.
điện tích hạt nhân tăng dần.
Kí hiệu nguyên tử nào sau đây được viết sai?
.
.
.
.
Các nguyên tử nào dưới đây thuộc cùng một nguyên tố hóa học?
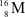 ;
; 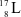 .
.
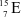 ;
; 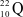 .
.
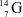 ;
; 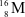 .
.
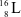 ;
; 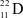 .
.
Hạt mang điện trong nhân nguyên tử là
neutron.
proton.
electron.
proton và neutron.
Photpho có Z=15 tổng số electron của lớp ngoài cùng là
3.
4.
5.
6.
Vỏ nguyên tử gồm các electron chuyển động như thế nào xung quanh hạt nhân?
Chuyển động rất chậm và không theo những quỹ đạo xác định.
Chuyển động rất chậm và không theo những quỹ đạo xác định.
Chuyển động rất nhanh theo những quỹ đạo xác định.
Chuyển động rất nhanh không theo những quỹ đạo xác định.
Nguyên tố chlorine (clo) có hai đồng vị bền với tỉ lệ phần trăm số nguyên tử tương ứng là: chiếm 75,77% và chiếm 24,23%. Trong phân tử CaCl2, phần trăm khối lượng của là (Ca=40) là
23,9%.
47,8%.
16,2%.
75,8%.
Phân lớp 3d có số electron tối đa là
6.
10.
14.
18.
Electron thuộc lớp nào sau đây liên kết chặt chẽ nhất với hạt nhân?
Lớp N.
Lớp L.
Lớp M.
Lớp K.
Orbital s có dạng
hình bầu dục.
hình số 8 nổi.
hình tròn.
hình cầu.
Nguyên tử chứa những hạt mang điện là
electron.
proton và electron.
proton và neutron.
electron và neutron.
Các phân lớp trong mỗi lớp electron được kí hiệu bằng các chữ cái viết thường theo thứ tự là
s, d, p, f.
s, p, d, f.
s, p, f,
d, p, s.
Nguyên tử không mang điện (trung hòa về điện) vì
có tổng số hạt proton bằng tổng số hạt electron.
tổng số hạt neutron bằng tổng số hạt proton.
được tạo nên bởi các hạt không mang điện.
có tổng số hạt electron bằng tổng số hạt neutron.
Nguyên tố hóa học là tập hợp các nguyên tử có cùng
số khối.
số electron.
neutron.
số proton.
Lớp electron thứ 3 (lớp M) có bao nhiêu phân lớp?
1.
2.
3.
4.
Orbital p có dạng
hình tròn.
hình số 8 nổi.
hình cầu.
hình bầu dục.
Những loại hạt cấu tạo nên hầu hết các hạt nhân nguyên tử là
Neutron và proton.
Electron và neutron.
Electron, neutron và proton.
Electron và proton.
Nguyên tử của nguyên tố X có cấu hình electron đã xây dựng đến phân lớp 3d2. Tổng số electron của nguyên tử nguyên tố X là
18.
20
24.
22.
Trong bảng hệ thống tuần hoàn, số thứ tự của chu kỳ bằng
số lớp electron.
số electron hoá trị.
số electron lớp ngoài cùng.
số hiệu nguyên tử.
Mỗi orbital nguyên tử chứa tối đa
1 electron.
2 electron.
4 electron.
3 electron.
Cấu hình electron nào sau đây thuộc về nguyên tố phi kim?
1s22s22p63s2.
1s22s22p63s23p1.
1s22s22p63s23p6.
1s22s22p63s23p4.
Trong nguyên tử, loại hạt nào có khối lượng không đáng kể so với các hạt còn lại?
Electron.
Proton.
Neutron.
Neutron và electron.
Số hiệu nguyên tử cho biết thông tin nào sau đây?
Nguyên tử khối.
Số proton.
Số neutron.
Số khối.
Số thứ tự ô nguyên tố trong bảng hệ thống tuần hoàn bằng
số nơtron.
số khối.
số hiệu nguyên tử.
số electron hóa trị.
Copper (đồng) có 2 đồng vị chiếm 73% và chiếm 27%. Khối lượng nguyên tử trung bình của Cu là
63,45.
63,63.
63,54.
64,63.
Nguyên tử nguyên tố X có hai lớp electron. Trong bảng tuần hoàn, X thuộc chu kì nào?
3.
4.
2.
5.
Trong tự nhiên, chlorine (clo) có 2 đồng vị . Số phân tử Cl2 được tạo thành từ 2 đồng vị là
3.
2.
4.
1.
Một nguyên tử được đặc trưng cơ bản bằng
Số proton và số đơn vị điện tích hạt nhân.
Số proton và số electron.
Số khối A và số neutron.
Số khối A và số đơn vị điện tích hạt nhân.
(1 điểm) Cấu hình electron của:
- Nguyên tử X: 1s22s22p63s23p64s2
- Nguyên tử Y: 1s22s22p63s23p5
(a) Mỗi nguyên tử X và Y chứa bao nhiêu electron?
(b) Lớp electron nào trong nguyên tử X và Y có mức năng lượng cao nhất?
(c) X và Y là nguyên tố kim loại, phi kim hay khí hiếm?
(1 điểm)
Nguyên tử nguyên tố X có tổng số các loại hạt cơ bản là 82, trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 22.
(a) Hãy Xác định số hiệu nguyên tử của nguyên tố X.
(b) Xác định số lượng các hạt cơ bản trong ion X2+ và viết cấu hình electron của ion đó.
(1 điểm)
(a) Xác định số hạt proton, số hạt electron, số hạt neutron trong mỗi nguyên tử sau , .
(b) Đồng (Copper) là là kim loại dễ dát mỏng, dẫn điện và dẫn nhiệt tốt. Vì thế đồng được sử dụng rất nhiều trong sản xuất các nguyên liệu. Các đồ dùng từ đồng như: dây điện, đồ dùng nội thất trong nhà, các tượng đúc, động cơ máy móc,... Đồng có hai đồng vị bền làvà . Nguyên tử khối trung bình của đồng là 63,54. Tính số nguyên tử trong 20,181 gam CuCl2 (Cl = 35,5, số Avogađro N=6,02.1023).








