(Đúng sai) 28 bài tập Hóa 10 Kết nối tri thức Bài 19: Tốc độ phản ứng hóa học có lời giải (Phần 1)
84 câu hỏi
Mỗi phát biểu sau về tốc độ phản ứng hóa học là đúng hay sai?
a. Là đại lượng đặc trưng cho sự thay đổi nồng độ của chất phản ứng hoặc sản phẩm trong một đơn vị thời gian.
b. Kí hiệu là v, có đơn vị là mol/L.
c. Dùng để đánh giá mức độ nhanh hay chậm của một phản ứng hóa học.
d. Phụ thuộc vào nồng độ và thời gian phản ứng.
a. Tốc độ của phản ứng hóa học chỉ có thể được xác định theo sự thay đổi nồng độ chất phản ứng theo thời gian.
b. Tốc độ của phản ứng hóa học không thể xác định được từ sự thay đổi nồng độ chất sản phẩm tạo thành theo thời gian.
c. Dấu “–” trong biểu thức tính tốc độ trung bình theo biến thiên nồng độ chất phản ứng là để đảm bảo cho giá trị của tốc độ phản ứng không âm.
d. Tốc độ trung bình của một phản ứng trong một khoảng thời gian nhất định được biểu thị bằng biến thiên nồng độ một chất phản ứng hoặc sản phẩm tạo thành chia cho khoảng thời gian đó.
Mỗi phát biểu sau là đúng hay sai?
a. Tốc độ phản ứng giảm theo thời gian vì nồng độ chất phản ứng giảm.
b. Tốc độ phản ứng là như nhau tại bất kì thời điểm nào trong suốt quá trình phản ứng.
c. Tốc độ phản ứng phụ thuộc vào nhiệt độ và thường tăng khi nhiệt độ tăng.
d. Tốc độ phản ứng giảm khi tăng nồng độ chất phản ứng.
Mỗi phát biểu nào sau đây về chất xúc tác là đúng hay sai?
a. Xúc tác giúp làm giảm năng lượng hoạt hoá của phản ứng.
b. Khối lượng xúc tác giảm dần theo thời gian trong quá trình phản ứng.
c. Xúc tác làm tăng tốc độ phản ứng.
d. Xúc tác kết hợp với sản phẩm phản ứng tạo thành hợp chất bền.
Tốc độ của một phản ứng hóa học
a. không phụ thuộc vào nồng độ các chất tham gia phản ứng.
b. tăng khi nhiệt độ phản ứng tăng.
c. càng nhanh khi giá trị năng lượng hoạt hóa càng lớn.
d. phụ thuộc vào diện tích bề mặt.
Tốc độ của một phản ứng giảm đi khi
a. giảm áp suất đối với phản ứng có chất tham gia phản ứng ở thể lỏng hoặc rắn.
b. thêm chất ức chế vào hỗn hợp chất tham gia phản ứng.
c. tăng nồng độ chất tham gia phản ứng
d. nghiền chất tham gia dạng khối thành dạng bột
Vì sao nếu xẻ một khúc củi to thành những mảnh củi nhỏ sẽ cháy nhanh hơn? Mỗi phát biểu sau là đúng hay sai?
a. Nhiều mảnh củi nhỏ sẽ có tổng diện tích tiếp xúc với oxygen nhiều hơn là một khúc củi to.
b. Khúc củi to có bề mặt lớn nên cần nhiều thời gian hơn mới cháy.
c. Tất cả những mảnh củi nhỏ đều bắt lửa cùng một lúc.
d. Khúc củi to nặng hơn nên cháy khó hơn
Xét phản ứng: H2 + I2 ![]() 2HI (*). Nghiên cứu sự thay đổi nồng độ các chất tham gia và chất tạo thành trong phản ứng theo thời gian, thu được đồ thị sau:
2HI (*). Nghiên cứu sự thay đổi nồng độ các chất tham gia và chất tạo thành trong phản ứng theo thời gian, thu được đồ thị sau:
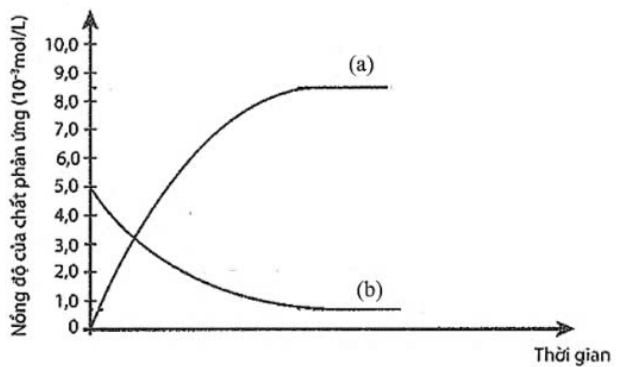
a. Đường (a) mô tả sự thay đổi nồng độ của H2 và I2 theo thời gian.
b. Đường (b) mô tả sự thay đổi nồng độ của HI theo thời gian.
c. Biểu thức tính tốc độ trung bình của phản ứng (*) là ![]() (với
(với ![]() ,
, ![]() ,
, ![]() lần lượt là biến thiên nồng độ các chất).
lần lượt là biến thiên nồng độ các chất).
d. Đơn vị tốc độ phản ứng trong phản ứng (*) là mmol/(L.s).
Cho phản ứng đơn giản: aA + bB ![]() CD + dD. Tốc độ tức thời của phản ứng được tính theo biểu thức:
CD + dD. Tốc độ tức thời của phản ứng được tính theo biểu thức: ![]() (trong đó CA, CB là nồng độ của A và B tại thời điểm đang xét; v là tốc độ phản ứng tại thời điểm đang xét).
(trong đó CA, CB là nồng độ của A và B tại thời điểm đang xét; v là tốc độ phản ứng tại thời điểm đang xét).
a. Hằng số tốc độ phản ứng k là tốc độ của phản ứng khi nồng độ của tất cả các chất A, B đều bằng nhau và bằng 1 M.
b. Hằng số tốc độ phản ứng k phụ thuộc vào nồng độ phản ứng.
c. Giá trị v luôn không đổi trong thời gian phản ứng xảy ra.
d. Ở nhiệt độ không đổi, tốc độ phản ứng tỉ lệ thuận với tích số nồng độ các chất phản ứng hoặc sản phẩm với số mũ thích hợp.
Cho phản ứng hóa học tổng quát: aA + bB ![]() cC + dD (*) có tốc độ phản ứng là v.
cC + dD (*) có tốc độ phản ứng là v.
a. Giá trị của v phụ thuộc vào nồng độ của chất C hoặc D
b. Giá trị của v phụ thuộc vào nồng độ của chất A hoặc B
c. Sau một đơn vị thời gian, nồng độ của chất A và B giảm xuống còn nồng độ của chất C và D tăng lên.
d. Tốc độ tiêu hao của chất A luôn bằng tốc độ tạo thành của chất C.
Nghiên cứu ảnh hưởng của nồng độ đến tốc độ phản ứng:
Na2S2O3 + H2SO4 ![]() Na2SO4 + S + SO2 + H2O
Na2SO4 + S + SO2 + H2O
Chuẩn bị: Các dung dịch: Na2S2O3 0,05 M, Na2S2O3 0,10 M, Na2S2O3 0,30 M, H2SO4 0,5 M; 3 bình tam giác, đồng hồ bấm giờ, tờ giấy trắng có kẻ chữ X.
Tiến hành:
- Cho vào mỗi bình tam giác 30 mL dung dịch Na2S2O3 với các nồng độ tương ứng là 0,05 M; 0,10 M và 0,30 M. Đặt các bình lên tờ giấy trắng có kẻ sẵn chữ X.
- Rót nhanh vào mỗi bình 30 mL dung dịch H2SO4 0,5 M và bắt đầu bấm giờ.
Lưu ý: Phản ứng có sinh ra khí độc. Cần tiến hành cẩn thận và tránh ngửi trực tiếp trên miệng bình tam giác.
a. Phản ứng ở bình chứa dung dịch Na2S2O3 có nồng độ 0,3 M xảy ra nhanh nhất.
b. Phản ứng ở bình chứa dung dịch Na2S2O3 có nồng độ 0,05 M xảy ra chậm nhất.
c. Khi nồng độ các chất tham gia giảm, tốc độ phản ứng sẽ tăng.
d. Khi nồng độ các chất tham gia tăng, tốc độ phản ứng sẽ tăng.
Nghiên cứu ảnh hưởng của diện tích bề mặt đến tốc độ phản ứng:
CaCO3(s) + 2HCl(aq) ![]() CaCl2(aq) + CO2(g) + H2O(l)
CaCl2(aq) + CO2(g) + H2O(l)
Chuẩn bị: 2 bình tam giác, dung dịch HCl 0,5 M, đá vôi dạng viên, đá vôi đập nhỏ.
Tiến hành:
- Cho cùng một lượng (khoảng 2 g) đá vôi dạng viên vào bình tam giác (1) và đá vôi đập nhỏ vào bình tam giác (2).
- Rót 20 mL dung dịch HCl 0,5 M vào mỗi bình.
a. Phản ứng trong bình tam giác (1) có tốc độ thoát khí nhanh hơn.
b. Đá vôi dạng viên có tổng diện tích bề mặt nhỏ hơn đá vôi dạng đập nhỏ.
c. Nếu lấy cùng một lượng đá vôi thì đá vôi dạng đập nhỏ tan nhanh hơn đá vôi dạng viên.
d. Khi tăng diện tích bề mặt tiếp xúc, số va chạm giữa các chất đầu tăng lên, số va chạm hiệu quả cũng tăng theo, dẫn đến tốc độ phản ứng tăng.
Nghiên cứu ảnh hưởng của chất xúc tác đến tốc độ phản ứng:
2H2O2(aq) ![]() 2H2O(l) + O2(g)
2H2O(l) + O2(g)
Hóa chất: dung dịch hydrogen peroxide (H2O2) 30%, bột MnO2.
Dụng cụ: Ống nghiệm, tàn đóm đỏ.
Tiến hành:
- Bước 1: Rót khoảng 2 mL dung dịch H2O2 vào 2 ống nghiệm (1), (2).
- Bước 2: Thêm một ít bột MnO2 vào ống nghiệm (2) và đưa nhanh tàn đóm đỏ vào miệng 2 ống nghiệm.
a. Tàn đóm ở ống nghiệm (1) chỉ cháy nhẹ.
b. Tàn đóm ở ống nghiệm (2) bùng cháy mãnh liệt hơn.
c. Sau khi phản ứng kết thúc, chất xúc tác MnO2 cũng bị tiêu hao hết.
d. Khi có xúc tác, phản ứng sẽ xảy ra qua nhiều giai đoạn, mỗi giai đoạn đều có năng lượng hoạt hoá thấp hơn so với phản ứng không xúc tác, do đó số hạt có đủ năng lượng hoạt hoá sẽ nhiều hơn, dẫn đến tốc độ phản ứng tăng.
Cùng một lượng kim loại Zn phản ứng với cùng một thể tích dung dịch H2SO4 1 M, nhưng ở hai nhiệt độ khác nhau theo phản ứng: Zn + H2SO4 ![]() ZnSO4 + H2.
ZnSO4 + H2.
Thể tích khí H2 sinh ra ở mỗi thí nghiệm theo thời gian được biểu diễn ở đồ thị sau:
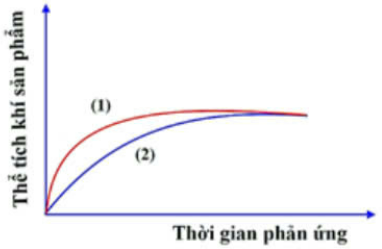
a. Đồ thị (1) mô tả phản ứng xảy ra ở nhiệt độ cao hơn đồ thị (2).
b. Thể tích khí sinh ra ở đồ thị (1) nhiều hơn thể tích khí sinh ra ở đồ thị (2).
c. Lượng muối thu được ở cả hai thí nghiệm là như nhau.
d. Sau một thời gian, hai đồ thị lại chụm lại với nhau do phản ứng đã dừng lại.
Có hai miếng sắt có kích thước giống hệt nhau, một miếng là khối sắt đặc (A), một miếng có nhiều lỗ nhỏ li ti bên trong và trên bề mặt (B). Thả hai miếng sắt vào hai cốc đựng dung dịch HCl cùng thể tích và nồng độ, theo dõi thể tích khí hydrogen thoát ra theo thời gian. Vẽ đồ thị thể tích khí theo thời gian, thu được hai đồ thị sau:
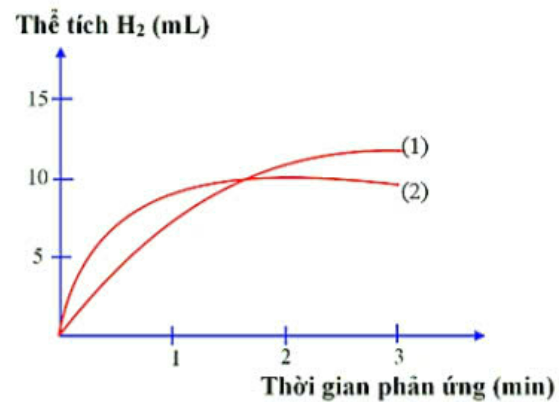
a. Đồ thị (1) mô tả tốc độ thoát khí từ miếng sắt (A).
b. Đồ thị (2) mô tả tốc độ thoát khí từ miếng sắt (B).
c. Miếng sắt (B) có nhiều lỗ có diện tích bề mặt nhỏ hơn miếng sắt (A) nên lúc đầu tốc độ phản ứng với HCl cao hơn.
d. Lượng khí hydrogen sinh ra từ đồ thị (1) nhiều hơn lượng khí sinh ra từ đồ thị (2).
Cho 6 gam Zn hạt vào một cốc đựng dung dịch H2SO4 4 M (dư) ở nhiệt độ 20 °C. Mỗi phát biểu nào dưới đây là đúng hay sai?
a. Thay 6 gam Zn hạt bằng 6 gam Zn bột làm tốc độ phản ứng tăng lên.
b. Thay dung dịch H2SO4 4 M bằng dung dịch H2SO4 2 M làm tốc độ phản ứng giảm xuống.
c. Thực hiện phản ứng ở nhiệt độ cao hơn (khoảng 50 °C) làm tốc độ phản ứng giảm xuống.
d. Dùng thể tích dung dịch H2SO4 4 M lên gấp đôi ban đầu làm tăng tốc độ phản ứng.
Trong quy trình sản xuất sulfuric acid, xảy ra phản ứng hoá học:
2SO2(g) + O2(g) ![]() 2SO3(g)
2SO3(g)
a. Xúc tác V2O5 sẽ dần chuyển hoá thành chất khác nhưng khối lượng của V2O5 không thay đổi
b. Khi giảm nhiệt độ của phản ứng thì tốc độ phản ứng giảm xuống.
c. Trong quá trình phản ứng thì nồng độ SO2 tăng còn nồng độ SO3 giảm dần.
d. Khi tăng áp suất khí SO2 hoặc O2 thì tốc độ phản ứng đều tăng.
Mối quan hệ của hệ số Van't Hoff với tốc độ và nhiệt độ được biểu diễn bằng công thức:
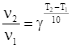
Trong đó: γ là hệ số nhiệt độ Van't Hoff.
v1, v2 là tốc độ phản ứng ở hai nhiệt độ T1 và T2.
a. Quy tắc Van't Hoff chỉ gần đúng trong khoảng nhiệt độ không cao.
b. Với đa số các phản ứng, khi nhiệt độ tăng 1 °C thì tốc độ phản ứng tăng từ 2 đến 4 lần.
c. Với phản ứng có γ = 2, nếu nhiệt độ tăng lên từ 20 °C lên 60 °C thì tốc độ phản ứng tăng 8 lần.
d. Với phản ứng có γ = 3, tốc độ phản ứng giảm 9 lần khi giảm nhiệt độ từ 70 °C xuống 40 °C.
Một bạn học sinh thực hiện hai thí nghiệm:
Thí nghiệm 1: Cho 100 mL dung dịch acid HCl vào cốc (1), sau đó thêm một mẫu zinc (Zn) và đo tốc độ khí H2 thoát ra theo thời gian.
Thí nghiệm 2 (lặp lại tương tự thí nghiệm 1): 100 mL dung dịch acid HCl khác được cho vào cốc (2) rồi cũng thêm một mẫu zinc vào và lại đo tốc độ khí hydrogen thoát ra theo thời gian.
Bạn học sinh đó nhận thấy tốc độ thoát khí hydrogen ở cốc (2) nhanh hơn cốc (1).
a. Phản ứng ở cốc (2) nhanh hơn nhờ có chất xúc tác.
b. Lượng Zn ở cốc (1) nhiều hơn ở cốc (2).
c. Acid HCl ở cốc (1) có nồng độ thấp hơn acid ở cốc (2).
d. Zn ở cốc (1) được nghiền nhỏ còn Zn ở cốc (2) ở dạng viên.
Thực hiện phản ứng sau: CaCO3 + 2HCl ![]() CaCl2 + CO2 + H2O
CaCl2 + CO2 + H2O
Theo dõi thể tích CO2 thoát ra theo thời gian, thu đồ thị như sau (thể tích khí được đo ở áp suất khí quyển và nhiệt độ phòng):
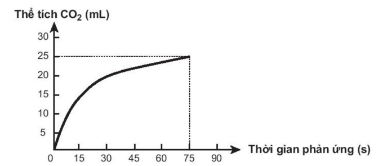
Trong các phát biểu sau, phát biểu nào không đúng?
a. Ở thời điểm 90 giây, tốc độ phản ứng bằng 0.
b. Tốc độ trung bình của phản ứng trong khoảng thời gian từ thời điểm đầu đến 75 giây là 033 mL/s.
c. Tốc độ phản ứng giảm dần theo thời gian
d. Tốc độ trung bình của phản ứng trong các khoảng thời gian 15 giây là như nhau.
Trong quy trình sản xuất sulfuric acid, xảy ra phản ứng hóa học sau:
2SO2 + O2 ![]() 2SO3
2SO3
a. Khi tăng áp suất khí SO2 hay O2 thì tốc độ phản ứng đều tăng lên.
b. Tăng diện tích bề mặt của xúc tác V2O5 sẽ làm tăng tốc độ phản ứng.
c. Xúc tác sẽ dần chuyển hóa thành chất khác nhưng khối lượng không đổi.
d. Cần làm nóng bình phản ứng để đẩy nhanh tốc độ phản ứng.








