Đề ôn thi Hóa học ĐGNL ĐHSP Hà Nội có đáp án - Đề số 3
27 câu hỏi
Để nghiên cứu về sự ăn mòn của kim loại, một học sinh đã thiết kế thí nghiệm như các hình dưới, trong đó bốn thanh sắt được đặt tiếp xúc với những kim loại khác nhau và đều được nhúng trong dung dịch HCl 1M.
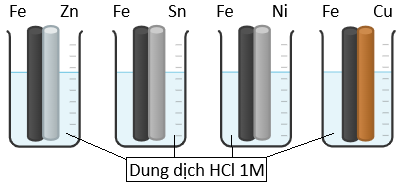
Có các phát biểu sau:
(1) Thanh sắt bị hòa tan nhanh nhất sẽ là thanh được đặt tiếp xúc với Cu.
(2) Cả 4 thí nghiệm đều xảy ra sự ăn mòn điện hóa.
(3) Có 2 thí nghiệm trong đó Fe đóng vai trò là cathode.
(4) Có 3 thí nghiệm trong đó Fe bị ăn mòn trước.
Số phát biểu đúng là
1.
2.
3.
4.
Cho các phát biểu sau:
(1) Cao su thiên nhiên chứa các mắt xích isoprene, liên kết đôi trong mạch đều ở dạng cis.
(2) Vật liệu composite thường gồm hai thành phần chính là vật liệu cốt và vật liệu nền.
(3) Phương pháp xử lí rác thải nhựa không gây ô nhiễm môi trường là đốt cháy.
(4) Tơ tằm có thành phần chính là protein, chúng rất bền nhiệt và bền trong môi trường kiềm.
(5) Keo dán epoxy có thành phần chính là chất hữu cơ có nhóm –COOH và –NH2 ở hai đầu.
Có bao nhiêu phát biểu đúng?
2.
3.
4.
5.
Điện phân dung dịch copper(II) sulfate, nhóm học sinh đã tiến hành như sau: Nhúng hai điện cực vào cốc đựng khoảng 60 mL dung dịch CuSO4 0,5M rồi nối hai điện cực với nguồn điện để tiến hành điện phân (chú ý không để hai điện cực đã nối nguồn điện chạm vào nhau). Thời gian điện phân là 5 phút với cường độ dòng điện 10A. Quan sát hiện tượng thí nghiệm xảy ra, một học sinh đưa ra các phát biểu dưới đây, hãy cho biết phát biểu nào sai?
Màu xanh lam của dung dịch CuSO4 nhạt dần.
Kim loại màu đỏ được sinh ra bám vào cathode.
Có khí không màu (O2) thoát ra ở anode.
Thấy có khí thoát ra ở 2 điện cực.
Phương trình hoá học thuỷ phân 2-bromo-2-methylpropane trong NaOH là:
(CH3)3CBr + NaOH → (CH3)3COH + NaBr
Phản ứng trên diễn ra theo 2 giai đoạn được mô tả như sau:
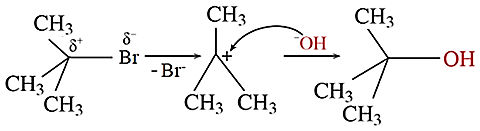
Nhận định nào sau đây đúng?
Phản ứng thuỷ phân 2-bromo-2-methylpropane là phản ứng tách hydrogen halide.
Trong giai đoạn (1) do độ âm điện C lớn hơn Br nên liên kết phân cực về phía Br.
Trong giai đoạn (2) có sự hình thành liên kết σ.
Sản phẩm thu được sau phản ứng thủy phân là alcohol bậc IV.
Cho các phát biểu sau:
(1) Để làm mềm nước cứng tạm thời có thể dùng dung dịch Ca(OH)2 hoặc NaOH.
(2) Nhúng thanh Cu trong dung dịch Fe2(SO4)3 có nhỏ vài giọt dung dịch H2SO4 có xuất hiện ăn mòn điện hóa.
(3) Các kim loại nhóm IIA có nhiệt độ sôi, nhiệt độ nóng chảy biến đổi không theo quy luật nhất định.
(4) Các kim loại đều có bán kính nhỏ hơn các phi kim thuộc cùng một chu kì.
(5) Khử zinc oxide ở nhiệt độ cao bằng than cốc thu được zinc ở trạng thái khí.
(6) Dùng dung dịch Fe2(SO4)3 dư có thể tách Ag ra khỏi hỗn hợp Ag và Cu.
Có bao nhiêu phát biểu đúng?
3.
4.
5.
6.
Alanine, ký hiệu là Ala là một amino acid được sử dụng trong quá trình sinh tổng hợp protein. Trong dung dịch ở pH khác nhau, alanine sẽ tồn tại ở các dạng như dưới đây:
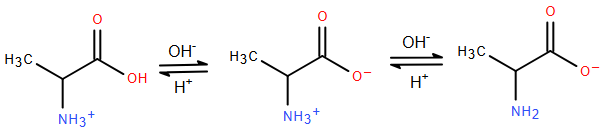
Ở pH = 6 alanine tồn tại chủ yếu ở dạng ion lưỡng cực có tổng điện tích bằng không. Khi đặt trong điện trường, alanine hầu như không di chuyển. Nhận định nào sau đây về alanine là không đúng?
Alanine là một α-amino acid.
Trong môi trường kiềm, dạng tồn tại của alanine là dạng anion.
Alanine có tính lưỡng tính.
Ở pH < 6, alanine nhận proton trở thành anion, khi đặt trong điện trường di chuyển về cực dương.
Phát biểu nào dưới đây là sai về quá trình sản xuất aluminium (Al) trong công nghiệp?
Điện phân nóng chảy Al2O3 với cryolite (Na3AlF6) làm xúc tác thu được Al ở cathode dưới dạng nóng chảy.
Trong quá trình điện phân phải hạ thấp dần các điện cực anode vào thùng điện phân, do khí O2 thoát ra đốt cháy dần điện cực.
Al có thể được tái chế nhiều lần do các tính chất vốn có của nó bị biến đổi, nên chủ yếu sử dụng trong xây dựng.
Vai trò cryolite để tiết kiệm năng lượng, tạo chất lỏng có tính dẫn điện tốt và nổi lên trên Al lỏng để ngăn cách Al lỏng với không khí.
Cho các phát biểu sau
(1) Thảo dược được ngâm chiết trong rượu thuộc phương pháp chiết lỏng – lỏng.
(2) Làm đường từ mía thuộc phương pháp chưng cất.
(3) Nấu rượu uống thuộc phương pháp kết tinh.
(4) Phân tích thổ nhưỡng thuộc phương pháp chiết lỏng – rắn.
(5) Để phân tích dư lượng thuốc bảo vệ thực vật trong nông sản dùng phương pháp chưng cất.
Số phát biểu đúng là
4.
2.
1.
3.
Khi đốt nóng tinh thể LiCl trong ngọn lửa đèn khí không màu thì tạo ra ngọn lửa có màu
da cam.
tím nhạt.
vàng.
đỏ tía.
Kết quả thí nghiệm của các chất X, Y, Z với các thuốc thử được ghi ở bảng sau:
| Chất | Thuốc thử | Hiện tượng |
| X | Quỳ tím | Quỳ tím chuyển màu hồng |
| Y | Dung dịch AgNO3 trong NH3 | Tạo kết tủa Ag |
| Z | Nước bromine | Tạo kết tủa trắng |
Các chất X, Y, Z lần lượt là
ethyl formate, glutamic acid, aniline.
aniline, ethyl formate, glutamic acid.
glutamic acid, ethyl formate, aniline.
glutamic acid, aniline, ethyl formate.
Trong tự nhiên, calcium sulfate tồn tại dưới dạng muối ngậm nước (CaSO4.2H2O) được gọi là
vôi sống.
vôi tôi.
thạch cao sống.
đá vôi.
Amine X có phân tử khối nhỏ hơn 80. Trong phân tử X, nitrogen chiếm 19,18% về khối lượng. Cho X tác dụng với nitrous acid (HNO2) ở nhiệt độ thường thu được alcohol và giải phóng khí. Số công thức cấu tạo thỏa mãn X là
4.
8.
3.
2.
Cũng giống như nam châm, mỗi nguyên tử/ ion cũng có thể có từ tính (bị nam châm hút). Nếu nguyên tử/ ion có electron độc thân thì nó có từ tính và được gọi là chất thuận từ. Ngược lại, nguyên tử/ ion nếu không có electron độc thân thì được gọi là chất nghịch từ. Nguyên tử/ ion nào sau đây nghịch từ?
Cu.
Cu+.
Na.
Al.
Cho phản ứng cracking sau:

Công thức cấu tạo thu gọn của X là
CH3CH2CH3.
CH3CH=CH2.
CH3CH=CHCH3.
CH3CH2CH2CH3.
Khi nhiệt độ tăng lên 10 oC, tốc độ của một phản ứng hóa học tăng lên 3 lần. Hỏi tốc độ của phản ứng đó tăng lên bao nhiêu lần khi nâng nhiệt độ lên từ 30 oC đến 50 oC?
3 lần.
6 lần.
9 lần.
27 lần.
Cho bảng số liệu sau:
| Chất | Nước (H2O) | Hydrogen sulfide (H2S) |
| Nhiệt độ sôi ( o C ) ở 1 atm | 100,0 | -60,7 |
Phát biểu nào sau đây sai?
Liên kết O – H trong phân tử H2O kém phân cực hơn liên kết S – H trong phân tử H2S.
Số liên kết trong phân tử H2O bằng số liên kết trong phân tử H2S.
Trong phân tử H2O và phân tử H2S chỉ có các liên kết cộng hóa trị.
Do có liên kết hydrogen giữa các phân tử nên nước có nhiệt độ sôi cao hơn hydrogen sulfide.
Trong phân tử phức chất K 3 [ F e ( C N ) 6 ] , Fe3+ được gọi là
phối tử.
base.
chất khử.
nguyên tử trung tâm.
Tiến hành điều chế ethyl acetate theo các bước như hình sau:
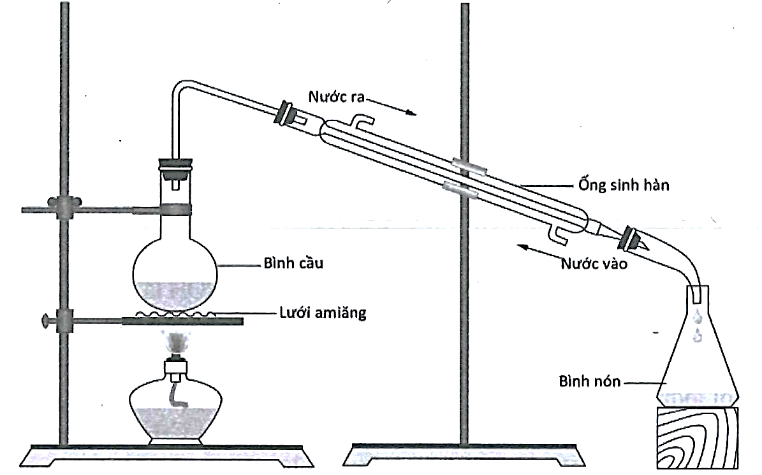
Bước 1: Cho 10 mL C2H5OH (D = 0,78 g/cm3) cùng với 10 mL CH3COOH (D = 1,05 g/cm3), vài giọt dung dịch H2SO4 đặc và lắc đều bình cầu.
Bước 2: Đun nóng bình cầu đến 70oC trong khoảng từ 5 đến 6 phút.
Bước 3: Các chất thu được ở bình nón được thêm tiếp vào 2 mL dung dịch NaCl bão hòa.
Phát biểu nào dưới đây là đúng?
Sau bước 1, trong bình cầu có phản ứng ester hóa sau: CH3COOH + HOCH2CH3 ⇌ H 2 S O 4 d , t o CH3COOCH2CH3 + H2O
Ở bước 3, dung dịch NaCl bão hòa có vai trò làm tăng hiệu suất phản ứng ester hóa.
Sau bước 2, các chất C2H5OH và CH3COOH vẫn còn trong bình cầu.
Đun nóng 6 gam acetic acid với 6 gam ethyl alcohol có H2SO4 đặc làm xúc tác. Khối lượng ester tạo thành khi hiệu suất phản ứng 80% là 8,8 gam.
Xét hai phân tử NH3 và CH4. Phát biểu nào sau đây sai?
Trong cả hai phân tử, nguyên tử trung tâm lai hóa sp3
Góc liên kết trong phân tử NH3 lớn hơn trong CH4.
Trong các phân tử này chỉ có liên kết đơn.
Phân tử NH3 phân cực, phân tử CH4 không phân cực.
Cho phản ứng:
H2 (g) + I2(g) ⇌ 2HI (g)
Ở nhiệt độ 430°C, hằng số cân bằng KCcủa phản ứng trên bằng 53,96. Đun nóng một bình kín dung tích không đổi 10 lít chứa 4,0 gam H2và 406,4 gam I2. Khi hệ phản ứng đạt trạng thái cân bằng ở 430°C, nồng độ của HI gần nhất với
0,275M.
0,320M.
0,151M.
0,225M.
Trong phòng thí nghiệm, một nhóm học sinh tìm hiểu ảnh hưởng của thời gian lưu giữ tới nồng độ FeSO₄ trong dung dịch. Giả thuyết của nhóm học sinh là: “Khi để lâu, nồng độ FeSO4 trong dung dịch giảm.” Nhóm học sinh chuẩn bị 250,0 mL dung dịch FeSO4 (nồng độ khoảng 0,1 M) đựng trong bình kín (dán nhãn bình là Y) và tiến hành các thí nghiệm ở hai thời điểm khác nhau như sau:
- Ngày thứ nhất:
Bước 1: Lấy 10,00 mL dung dịch trong bình Y cho vào bình tam giác rồi thêm tiếp 5 mL dung dịch H2SO4 2 M.
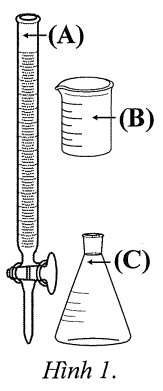 Bước 2: Chuẩn độ dung dịch trong bình tam giác bằng dung dịch KMnO4 2,20×10⁻2 M đến khi xuất hiện màu hồng nhạt (bền trong khoảng 20 giây) thì dừng. Ghi lại thể tích dung dịch KMnO4 đã dùng.
Bước 2: Chuẩn độ dung dịch trong bình tam giác bằng dung dịch KMnO4 2,20×10⁻2 M đến khi xuất hiện màu hồng nhạt (bền trong khoảng 20 giây) thì dừng. Ghi lại thể tích dung dịch KMnO4 đã dùng.
Lặp lại thí nghiệm chuẩn độ thêm 2 lần. Thể tích trung bình của dung dịch KMnO4 sau 3 lần chuẩn độ là 10,70 mL. Nồng độ của Fe(II) xác định được là C1 M.
- Ngày thứ tám:
Xác định lại hàm lượng Fe(II) của dung dịch chứa trong bình Y theo các bước tương tự như ngày thứ nhất. Thể tích trung bình của dung dịch KMnO4 sau 3 lần chuẩn độ là 9,92 mL. Nồng độ của Fe(II) xác định được là C2 M.
Nồng độ dung dịch KMnO4 như nhau trong các thí nghiệm chuẩn độ. Sự thay đổi nồng độ của Fe(II) (q%) được tính theo công thức:
q % = C 1 − C 2 C 1 × 1 0 0 %
Khi chuẩn độ, dung dịch KMnO₄ được nhỏ trực tiếp vào bình tam giác từ dụng cụ kí hiệu là (B) được minh họa ở Hình 1.
Giá trị của q là 7,9. (Kết quả các phép tính trung gian không được làm tròn, chỉ kết quả cuối cùng được làm tròn đến hàng phần mười.)
Giá trị của C2 là 0,109. (Kết quả các phép tính trung gian không được làm tròn, chỉ kết quả cuối cùng được làm tròn đến hàng phần nghìn.)
Kết quả thu được từ các thí nghiệm phù hợp với giả thuyết ban đầu của nhóm học sinh.
Muối Epsom ( M g S O 4 . n H 2 O ) có nhiều ứng dụng: vừa có thể dùng pha chế thuốc nhuận tràng, vừa như một loại phân bón cho cây, hay dung dịch khử khuẩn. Khi làm lạnh 440,0 gam dung dịch M g S O 4 2 7 , 2 7 % thì có 49,2 gam muối Epsom tách ra, phần dung dịch thu được có nồng độ 24,56%. Biết độ tan của M g S O 4 tại 8 0 o C và 2 0 o C lần lượt là 54,80 gam và 35,10 gam. Khối lượng Epsom được tách ra khi làm lạnh 9288 gam dung dịch bão hòa M g S O 4 từ 8 0 o C xuống 2 0 o C là b gam.
Để lâu Epsom trong không khí sẽ bị chảy rữa.
Giá trị của b là 3837 gam (kết quả làm tròn đến hàng đơn vị).
Epsom là một loại muối có ứng dụng trong y học.
Công thức của muối Epsom là M g S O 4 . 6 H 2 O .
Cho phản ứng:
C 4 H 1 0 ( g ) + 6 , 5 O 2 ( g ) → 4 C O 2 ( g ) + 5 H 2 O ( l ) ( 1 )
Dựa vào bảng số liệu sau:
Liên kết | C−H | C−C | O=O | C=O | H-O |
EbkJ.mol−1 | 418 | 346 | 494 | 732 | 459 |
Một bình gas chứa 12 kg khí trong đó butane (C4H10) chiếm 96,67% về khối lượng còn lại là tạp chất không cháy. Một hộ gia đình cần đốt gas để cung cấp 10 000 kJ nhiệt trong mỗi ngày. Biết hiệu suất hấp thụ nhiệt là 80%. Sau bao nhiêu ngày thì hộ gia đình trên dùng hết bình gas 12 kg? ((làm tròn đến hàng đơn vị).
32,3
Limonen là một chất có mùi thơm dịu được tách từ tinh dầu chanh. Kết quả phân tích nguyên tố cho thấy limonen được cấu tạo từ hai nguyên tố C và H, trong đó C chiếm 88,235% về khối lượng. Tỉ khối hơi của limonen so với không khí gần bằng 4,69. Công thức phân tử của limonen là?
C10H16
Các polyalcohol có các nhóm – OH liền kề như ethylene glycol, glycerol có thể tác dụng với copper(II) hydroxide tạo thành dung dịch màu xanh lam đậm. Viết phương trình hóa học của phản ứng xảy ra khi cho ethylene glycol tác dụng với copper(II) hydroxide.
Gọi tên chất sau theo danh pháp thay thế:
C H 3 − C H 2 − C H 2 − N | − C H 3 C H 3
N,N – dimethylpropan – 1 – amine
Trong dung dịch, amino acid tồn tại ở dạng ion lưỡng cực, cation hay anion tùy thuộc vào pH của dung dịch. Giá trị pH mà tại đó nồng độ dạng ion lưỡng cực đạt giá trị lớn nhất gọi là điểm đẳng điện (ký hiệu là pI). Điểm đẳng điện của các amino acid được tính theo biểu thức: p I = ( p K a 1 + p K a 2 ) 2 .
(với Ka1, Ka2 là hằng số phân li acid của các nhóm chức; pKa = -logKa)
Đối với các diamino monocarboxylic hoặc monoamino dicarboxylic, pI là giá trị trung bình của hai giá trị pKa gần nhau. Cho pKa của các amino acid như sau:
| Amino acid | pKa1 | pKa2 | pKa3 |
| Alanine | 2,35 | 9,87 | |
| Lysine | 2,18 | 8,95 | 10,53 |
| Aspartic acid | 2,10 | 3,86 | 9,82 |
(a). Tính điểm đẳng điện của alanine, lysine, aspartic acid.
(b). Viết công thức dạng ion lưỡng cực của các amino acid alanine, lysine, aspartic acid tại điểm đẳng điện.
(c). Viết công thức các dạng ion chủ yếu của từng amino acid trong dung dịch ở pH = 1 và ở pH = 13.
(d). Các amino acid có các điểm đẳng điện khác nhau nên ở một pH xác định, chúng sẽ di chuyển về cathode hoặc anode với những vận tốc khác nhau. Dựa trên cơ sở này người ta xây dựng phương pháp điện di để phân tích và tinh chế các amino acid từ hỗn hợp của chúng. Tính các dạng tồn tại chủ yếu của alanine và aspartic acid ở pH = 5,97. Từ đó cho biết có thể tách được 2 amino acid này bằng phương pháp điện di ở không?




