Đề ôn thi Hóa học ĐGNL ĐHSP Hà Nội có đáp án - Đề số 2
27 câu hỏi
A. TÔ TRÊN PHIẾU TRẢ LỜI TRẮC NGHIỆM
Phần I (5 điểm). Thí sinh trả lời từ câu 1 đến câu 20. Đối với mỗi câu, thí sinh chỉ chọn một phương án.
Thực hiện điện phân dung dịch copper(II) sulfate (CuSO4) nồng độ 0,5M với các điện cực trơ ở hiệu điện thế phù hợp. Quá trình xảy ra ở anode là
H2O bị khử và giải phóng H2.
Cu2+ bị khử thành Cu.
S O 4 2 − bị khử thành SO2.
H2O bị oxi hóa và giải phóng O2.
Kevlar là một polyamide có độ bền kéo rất cao. Loại vật liệu này được dùng để sản xuất áo chống đạn và mũ bảo hiểm cho quân đội. Kevlar được điều chế bằng phản ứng của hai chất sau:

Nhận xét nào sau đây sai?
Benzene-1,4-diamine thuộc loại arylamine.
Các monomer tạo nên vật liệu Kevlar đều là hợp chất hữu cơ đa chức.
Công thức cấu tạo của Kevlar là:

Kevlar được điều chế bằng phản ứng trùng hợp.
Thứ tự một số cặp oxi hoá - khử trong dãy điện hoá như sau: Mg2+/Mg; Fe2+/Fe; Cu2+/Cu; Fe3+/Fe2+; Ag+/Ag. Dãy chỉ gồm các chất, ion tác dụng được với ion Fe3+ trong dung dịch là
Fe, Cu, Ag+.
Mg, Fe2+, Ag.
Mg, Cu, Cu2+.
Mg, Fe, Cu.
Cho sơ đồ phản ứng sau:
(1) X + H 2 O → x t Y
(2) Y + [ A g ( N H 3 ) 2 ] O H → t o ammonium gluconate + Ag + N H 3 + H 2 O
(3) Y → x t E + Z
(4) Z + H2O →chất diệp lụcánh sáng X + G
Các chất X, Y, Z lần lượt là
cellulose, fructose, carbon dioxide.
cellulose, saccharose, carbon dioxide.
tinh bột, glucose, carbon dioxide.
tinh bột, glucose, ethanol.
Cho khí CO (dư) đi qua ống sứ nung nóng đựng hỗn hợp X gồm Al2O3, MgO, Fe3O4 và CuO, thu được chất rắn Y. Cho Y vào dung dịch NaOH dư, khuấy kĩ, thấy còn lại phần không tan Z. Giả sử các phản ứng xảy ra hoàn toàn. Phần không tan Z gồm:
MgO, Fe, Cu.
Mg, Fe, Cu.
MgO, Fe3O4, Cu.
Mg, Al, Fe, Cu
Malic acid là một loại acid tự nhiên, thường được tìm thấy trong các loại trái cây, đặc biệt là quả táo và các loại rau. Công thức cấu tạo của malic acid được cho như sau:
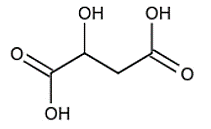
Phát biểu nào sau đây về malic acid là đúng?
Công thức phân tử của malic acid là C4H7O5.
1,0 mol malic acid phản ứng được tối đa với 2,0 mol K.
1,0 mol malic acid phản ứng được tối đa với 2,0 mol NaOH.
Dung dịch malic acid không tác dụng với NaHCO3.
Vàng ( A u ) tồn tại trong tự nhiên ở dạng đơn chất. Tuy nhiên, hàm lượng Au trong quặng hoặc trong đất thường rất thấp vì vậy rất khó tách Au bằng phương pháp cơ học. Trong công nghiệp, người ta tách vàng từ quặng theo sơ đồ sau:
Quặng chứa vàng ( A u ) → + O 2 + K C N + H 2 O K [ A u ( C N ) 2 ] ( a q ) → + Z n d u A u ( s )
Phương pháp điều chế kim loại nào đã được sử dụng trong quá trình sản xuất vàng theo sơ đồ trên?
Thuỷ luyện.
Nhiệt luyện.
Điện phân.
Chiết.
Khí nitrogen và khí oxygen là hai thành phần chính của không khí. Trong kĩ thuật người ta có thể hạ thấp nhiệt độ để hóa lỏng không khí. Biết nitrogen lỏng sôi ở -196 oC oxygen lỏng sôi ở -183 oC. Phương pháp tách riêng khí nitrogen và oxygen là
lọc.
chưng cất.
cô cạn.
chiết.
Hợp chất A tan nhiều trong nước; khi được đốt cháy trên ngọn lửa đèn khí thì tạo ra ngọn lửa màu vàng; khi tan trong dung dịch hydrochloric acid tạo ra khí, khí này làm đục nước vôi trong. Hợp chất A có thể là
K2CO3.
Na2CO3.
C a C O 3 hoặc C a ( H C O 3 ) 2 .
N a 2 C O 3 hoặc N a H C O 3 .
Nhỏ từ từ đến dư dung dịch ethylamine vào ống nghiệm (1) đựng dung dịch FeCl3; ống nghiệm (2) đựng dung dịch CuSO4; ống nghiệm (3) đựng dung dịch HCl có pha một vài giọt phenolphthalein; ống nghiệm (4) đựng nước bromine. Phát biểu nào sau đây sai?
Trong ống nghiệm (1) có kết tủa nâu đỏ.
Trong ống nghiệm (2) xuất hiện kết tủa màu xanh sau đó bị hoà tan thành dung dịch màu xanh lam.
Trong ống nghiệm (3) xuất hiện màu hồng.
Trong ống nghiệm (4) xuất hiện kết tủa trắng.
Một mẫu nước cứng có nồng độ các ion như sau: C a 2 + x M ; M g 2 + y M ; H C O 3 − 0 , 0 0 5 M ; C l − 0 , 0 0 4 M ; S O 4 2 − 0 , 0 0 1 M . Để làm mềm 1 0 L nước này cần dùng tối thiểu bao nhiêu gam sodium carbonate? (Kết quả làm tròn đến hàng phần trăm)
5,83.
0,58.
4,62.
0,46.
Hợp chất hữu cơ X là thành phần chính trong tinh dầu cây đinh hương và cây hương nhu. Trên phổ hồng ngoại của X có số sóng hấp thụ ở 3 515 cm−1 nhưng không có số sóng hấp thụ mạnh ở vùng 1 780 – 1 650 cm−1. Chất nào sau đây có phổ hồng ngoại phù hợp với X?
Số sóng hấp thụ đặc trưng trên phổ hồng ngoại của một số nhóm chức cơ bản được cho bởi bảng sau:

 .
.
 .
.
 .
.
 .
.
Liên kết trong phân tử nào sau đây được hình thành nhờ sự xen phủ orbital p–p?
H2.
Cl2.
NH3.
HCl.
Khi đun nóng chất hữu cơ X với dung dịch NaOH thu được ethylene glycol (HO-CH2-CH2-OH) và muối sodium acetate. Công thức cấu tạo đúng của X là
CH3COOCH2-CH2OH.
(CH3COO)2CH-CH3.
CH3COOCH2-CH2OCOCH3.
Cả A và C.
Enzyme amylase là một protein có khả năng xúc tác cho phản ứng thủy phân tinh bột. Hoạt tính xúc tác của enzyme càng cao thì phản ứng thủy phân tinh bột diễn ra càng nhanh. Hoạt tính xúc tác của enzyme phụ thuộc vào các yếu tố như nhiệt độ, p H , … Một nhóm học sinh dự đoán "pH càng tăng thì hoạt tính xúc tác của enzyme amylase càng cao". Từ đó, học sinh tiến hành thí nghiệm ở nhiệt độ không đổi nhưng thay đổi pH của môi trường để kiểm tra dự đoán trên như sau:
Bước 1: Thêm 2,0 mL dung dịch một loại enzyme amylase vào một ống nghiệm chứa 5,0 mL dung dịch có vai trò duy trì ổn định pH bằng 5.
Bước 2: Thêm tiếp 2,0 mL dung dịch tinh bột vào ống nghiệm trên, lắc đều.
Bước 3: Sau khoảng mỗi 10 giây, dùng ống hút lấy 1-2 giọt hỗn hợp phản ứng trong ống nghiệm và cho vào đĩa sứ chứa sẵn dung dịch iodine, quan sát để từ đó xác định thời gian tinh bột thủy phân hết.
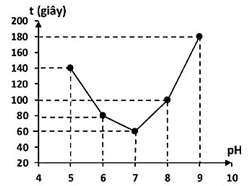
Lặp lại thí nghiệm theo ba bước trên, chỉ thay đổi pH dung dịch trong Bước 1 lần lượt là 6; 7; 8; 9.
Nhóm học sinh ghi lại kết quả thời gian t (giây) mà tinh bột thủy phân hết trong môi trường pH = 5; 6; 7; 8; 9 và vẽ đồ thị như hình bên.
Trong các phát biểu sau, phát biểu nào đúng?
Ở Bước 3, nếu dung dịch iodine chuyển sang màu xanh tím nghĩa là tinh bột thủy phân hết.
Theo số liệu thu được, phản ứng thủy phân tinh bột ở pH = 9 diễn ra nhanh hơn ở pH = 8.
Ở các giá trị pH nghiên cứu, hoạt tính xúc tác của enzyme amylase cao nhất tại pH = 7.
Từ kết quả thí nghiệm, kết luận được hoạt tính xúc tác của enzyme amylase tăng khi pH tăng.
Dãy gồm các chất trong phân tử chỉ có liên kết cộng hoá trị phân cực là
O2, H2O, NH3.
H2O, HF, HCl.
HCl, F2, O3.
HF, Cl2, H2O.
Số oxi hoá của nguyên tử trung tâm trong phức chất [Co(NH3)4(OH2)2]SO4 là
+3.
+6.
+2.
+4.
Tiến hành thí nghiệm điều chế ethyl propionate (có mùi dứa) theo thứ tự các bước sau:
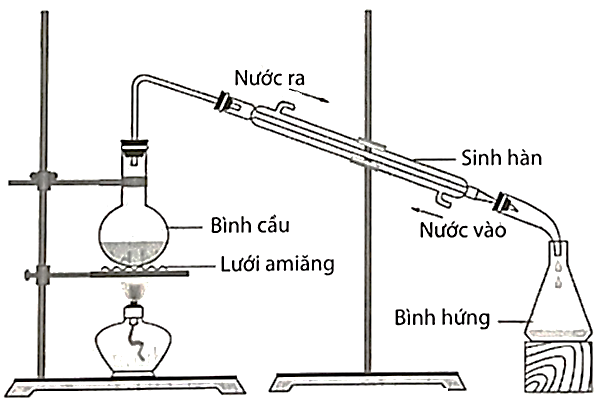
Bước 1. Cho 3 mL ethyl alcohol, 4 mL propionic acid và 5 mL H2SO4 đặc vào bình cầu, lắc đều và đun nhẹ trong khoảng 7 - 8 phút.
Bước 2. Để nguội chất lỏng ở bình hứng, thêm 10 mL dung dịch NaCl bão hoà và cho sang phễu chiết để tách sản phẩm thu được.
Trong các phát biểu sau, phát biểu nào đúng?
H2SO4 đặc chỉ có vai trò là chất xúc tác để phản ứng xảy ra nhanh hơn.
Trong phễu chiết, lớp chất lỏng phía dưới có thành phần chính là ethyl propionate.
Phản ứng điều chế ethyl propionate trong thí nghiệm trên là phản ứng xà phòng hoá.
Việc thêm dung dịch NaCl bão hoà giúp tách ethyl propionate dễ dàng hơn.
Phát biểu nào sau đây đúng khi nói về sự hình thành phân tử BF3?
Trên nguyên tử B, AO–2s tổ hợp với 2AO–2p để tạo 3AO lai hóa sp2 và còn 1AO p không lai hóa.
Ba AO lai hóa sp2 của B xen phủ với 3AO–p của 3 nguyên tử F tạo thành 3 liên kết σ hướng về 3 đỉnh của một tứ diện đều.
Phân tử BF3 có dạng hình học là tứ diện đều.
Góc liên kết trong phân tử BF3 là 180\(°\).
Hòa tan 12,675 gam một oleum A vào nước được 300 mL dung dịch Y. Chuẩn độ 10 mL dung dịch Y bằng dung dịch NaOH 0,25M thì kết quả cho ở bảng sau:
| Chuẩn độ | Lần 1 | Lần 2 | Lần 3 |
| V dung dịch NaOH 0,25M (mL) | 39,9 | 40,0 | 40,1 |
Khối lượng phân tử của oleum (amu) là
338.
418.
258.
178.
Phần II (2 điểm). Thí sinh trả lời từ câu 1, câu 2. Trong mỗi ý a), b), c, d) ở mỗi câu, thí sinh chọn đúng hoặc sai.
Hai chất X và Y là đồng phân cấu tạo của nhau và đều có mạch carbon no, không phân nhánh. Phân tích nguyên tố trong phân tử X cho kết quả: %C = 66,67%, %H = 11,11%; còn lại là oxygen. Từ phổ khối lượng, xác định được phân tử khối của X bằng 72.
X và Y đều là các alcohol đơn chức.
Công thức phân tử của X và Y là C 4 H 8 O .
Trên phổ hồng ngoại của X và Y đều có tín hiệu đặc trưng trong khoảng 1740 – 1 670 c m − 1 .
Ứng với công thức phân tử của X và Y có tổng 5 đồng phân mạch hở.
Methyl cinnamate (ester của cinnamic acid) là chất rắn có mùi thơm nồng. Nó được tìm thấy trong nhiều loại thực vật như dâu tây, húng quế, bạch đàn trắng.

Thủy phân hoàn toàn methyl cinnamate trong dung dịch NaOH đun nóng, thu được alcohol X và sodium cinnamate.
Trong phân tử methyl cinnamate, thành phần phần trăm theo khối lượng của carbon là 78,8 %. (Làm tròn kết quả đến hàng phần mười).
Methyl cinnamate là ester đơn chức.
Một mẫu cồn Z (thành phần chính là C2H5OH có lẫn alcohol X). Đốt cháy 10 gam cồn Z tỏa ra nhiệt lượng 291,9 kJ. Đốt cháy hoàn toàn 1 mol alcohol X toả ra lượng nhiệt là 716 kJ và 1 mol C2H5OH toả ra lượng nhiệt là 1370 kJ. Phần trăm khối lượng alcohol X trong mẫu cồn Z là 8 %.
Cho a mol alcohol X phản ứng tối đa với a mol Na thì sinh ra a mol H2.
B. VIẾT TRÊN TỜ GIẤY THI
Phần III (1 điểm). Thí sinh trả lời từ câu 1 đến câu 4. Đối với mỗi câu, thí sinh chỉ viết kết quả, không trình bày suy luận.
Dung dịch glucose (C6H12O6) 5%, có khối lượng riêng là 1,02 g/mL, phản ứng oxi hóa 1 mol glucose tạo thành CO2 (g) và H2O (l) tỏa ra nhiệt lượng là 2803,0 kJ. Một người bệnh được truyền một chai nước chứa 500 mL dung dịch glucose 5%. Năng lượng tối đa từ phản ứng oxi hóa hoàn toàn glucose mà bệnh nhân đó có thể nhận được là bao nhiêu kJ? Làm tròn kết quả đến hàng phần mười.
397,1
Quế có vị cay, mùi thơm nồng, được sử dụng phổ biến làm gia vị, vị thuốc trong Đông y. Hợp chất hữu cơ X tạo mùi đặc trưng của quế, có công thức phân tử là C9H8O. Trong phân tử X chứa vòng benzene có một nhóm thế. X tham gia phản ứng tráng bạc và có đồng phân hình học dạng trans. Xác định công thức cấu tạo của X.
Dưới tác dụng của enzyme từ các vi sinh vật khác nhau, glucose được lên men tạo thành các hợp chất có nhiều ứng dụng trong đời sống như ethanol, lactic acid… Viết phương trình hóa học của phản ứng tạo thành lactic acid từ glucose.
Cho hợp chất hữu cơ X sau:
H 2 N − [ C H 2 ] 4 − C | H − C O O H N H 2
Viết tên gọi của hợp chất X theo danh pháp thay thế.
2,6-diaminohexanoic acid
Phần IV (2 điểm). Thí sinh trả lời câu 5; viết quá trình và kết quả suy luận.
Sulfur dioxide (SO2) là một chất khí không màu, mùi hắc, độc và là một trong những tác nhân hàng đầu gây mưa acid.
(a) Viết phương trình hóa học chứng minh SO2 là một trong các tác nhân gây mưa acid.
(b) Cho biết tác động của mưa acid đối với calcium carbonate trong núi đá vôi và với kim loại sắt trong gang - thép. Viết các phương trình hóa học minh họa.
(c) Để tách SO2 có trong một nguồn khí thải của nhà máy nhiệt điện, người ta dẫn khí thải đi qua thiết bị lọc bụi tĩnh điện rồi qua thiết bị khử lưu huỳnh ướt (sơ đồ như hình bên dưới).

- Mô tả quá trình loại bỏ SO2 khỏi khí thải theo phương pháp khử lưu huỳnh ướt. Trong quá trình này, khí SO2 được hấp thụ theo nguyên tắc nào?
- Viết phương trình hóa học của các phản ứng xảy ra.
(d) Tính khối lượng CaCO3 (theo kilogam) tối thiểu tiêu thụ mỗi ngày đêm để loại bỏ 95% lượng SO2 có trong khí thải của nhà máy trên. Cho biết lưu lượng khí thải của nhà máy đó là 10 000 m³/giờ (đã hiệu chỉnh tới điều kiện chuẩn) và SO2 chiếm 0,15% thể tích khí thải.




