40 CÂU HỎI
Nếu M là nguyên tố nhóm IA thì oxit cao nhất của nó có công thức là
A. M2O3.
B. MO2.
C. M2O.
D. MO.
Sơ đồ phản ứng nào sau đây thể hiện cách điều chế kim loại đồng theo phương pháp nhiệt luyện?
A. CuSO4 + H2O → Cu + H2SO4 + O2.
B. CO + CuO → Cu + CO2.
C. CuCl2 → Cu + Cl2.
D. Fe + CuSO4 → Cu + FeSO4.
Nguyên tắc chung để điều chế kim loại là
A. cho ion kim loại tác dụng với axit.
B. oxi hoá ion kim loại thành kim loại.
C. cho ion kim loại tác dụng với bazơ.
D. khử ion kim loại thành nguyên tử kim loại.
Dẫn khí CO2 vào dung dịch NaOH dư, khi phản ứng kết thúc thu được dung dịch Y. Dung dịch Y có chứa
A. Na2CO3 và NaOH.
B. Na2CO3.
C. Na2CO3 và NaHCO3.
D. NaHCO3.
Quặng đôlômitcó thành phần chính là
A. MgCO3.Ca(HCO3)2
B. MgCO3.CaCl2
C. CaCO3.MgCl2
D. CaCO3.MgCO3
Nguyên liệu chính dùng để sản xuất nhôm là
A. quặng đôlômit.
B. quặng pirit.
C. quặng manhetit.
D. quặng boxit.
Nước cứng là nước
A. không chứa Ca2+, Mg2+ .
B. chứa nhiều Ca2+, Mg2+, .
C. chứa nhiều ion Ca2+, Mg2+ .
D. chứa nhiều ion kim loại nặng.
Khi thổi từ từ khí CO2 đến dư vào nước vôi trong thì
A. thu được kết tủa trắng.
B. có kết tủa trắng sau đó tan dần đến hết.
C. có kết tủa vàng sau đó tan dần đến hết.
D. dung dịch trong suốt từ đầu đến cuối.
Trong phòng thí nghiệm Na bảo quản bằng cách ngâm trong
A. nước lạnh.
B. dầu hoả.
C. cồn 90o.
D. cồn 70o.
Phèn chua có công thức hóa học nào sau đây?
A. Na2SO4. Al2(SO4)3. 24H2O
B. K2SO4. Al2(SO4)3.24H2O
C. Al2 (SO4)3
D. KAl(SO4)2.24H2O
Kim loại nào sau đây được điều chế bằng phương pháp thủy luyện?
A. Na.
B. Al.
C. Ag.
D. Mg.
Cho các chất sau: CaO, Na, Al2O3, Be, Mg(OH)2, K2O. Số chất tan được trong nước cho dung dịch bazơ là
A. 3.
B. 4.
C. 1.
D. 2.
Nồng độ phần trăm của dung dịch thu được khi cho 3,9 gam kali vào 136,2 gam H2O là
A. 5,0%
B. 6,0%
C. 4,0%
D. 7,0%.
Khử hoàn toàn 4,8 gam Fe2O3bằng CO dư ở nhiệt độ cao. Khối lượng Fe thu được sau phản ứng là
A. 1,44 gam.
B. 1,68 gam.
C. 2,52 gam.
D. 3,36 gam.
Chất có tính bazơ mạnh nhất trong các chất dưới đây là
A. KOH.
B. CsOH.
C. LiOH.
D. NaOH.
Cho các phát biểu sau về nước cứng:
(a) Khi đun sôi ta có thể loại được độ cứng tạm thời của nước.
(b) Có thể dùng Na2CO3 để loại cả độ cứng tạm thời và độ cứng vĩnh cửu của nước.
(c)Dung dịch HCl hòa tan được CaCO3, MgCO3 nên dùng HCl để làm mềm nước cứng.
(d) Có thể dùng Ca(OH)2 với lượng vừa đủ để làm mềm nước cứng toàn phần.
Số phát biểu đúng là
A. 3.
B. 1.
C. 4.
D. 2.
Sục từ từ khí CO2 đến dư vào dung dịch gồm a mol Ca(OH)2 và b mol NaOH . Sự phụ thuộc của số mol kết tủa CaCO3 vào số mol CO2 được biểu diễn theo đồ thị sau:
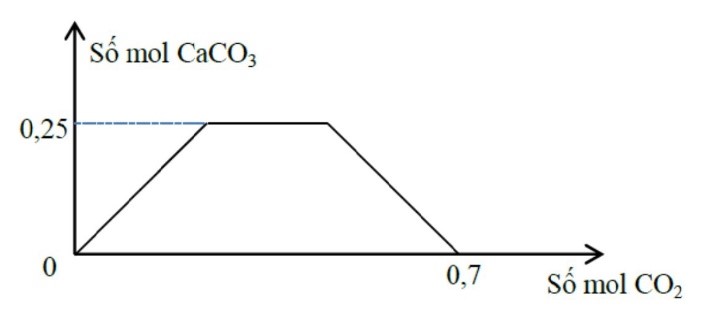
Tỉ lệ a : b tương ứng là
A. 4 : 5.
B. 4 : 3.
C. 5 : 4.
D. 2 : 3.
Cho 1,17 gam một kim loại kiềm tác dụng với nước (dư) thu được 0,336 lít khí hiđro (ở đktc). Kim loại kiềm là
A. Rb.
B. K.
C. Li.
D. Na.
Khi điện phân NaCl nóng chảy (điện cực trơ), tại anot xảy ra
A. sự khử ion Na+.
B. sự oxi hoá ion Cl-.
C. sự oxi hoá ion Na+.
D. sự khử ion Cl-.
Khi cho từ từ đến dư dung dịch NH3 vào dung dịch AlCl3. Hiện tượng thu được là
A. có kết tủa keo trắng không tan.
B. có khí thoát ra, có kết tủa keo trắng.
C. có kết tủa keo trắng, sau đó kết tủa tan.
D. có khí thoát ra.
Muối X tác dụng với dung dịch HCl có khí thoát ra, tác dụng với dung dịch NaOH có kết tủa. X là
A. Ca(HCO3)2.
B. Na2CO3.
C. (NH4)2CO3.
D. NaHCO3.
Dãy gồm các chất đều tác dụng được với dung dịch HCl và dung dịch NaOH là
A. Na2CO3, NaAlO2, AlCl3, KHSO4
B. NaHCO3, Al, NaAlO2, AlCl3
C. KHCO3, Al, Al2(SO4)3, Al2O3.
D. NaHCO3, K, Al2O3, Al(OH)3
Để phản ứng vừa đủ với 5,4 gam Al cần 100 ml dung dịch NaOH x (mol/l). Giá trị của x là
A. 2,5.
B. 1,0.
C. 1,5.
D. 2,0.
Thể tích dung dịch Ca(OH)2 0,01M tối thiểu để hấp thụ hết 0,02 mol khí CO2 là
A. 1,5 lít.
B. 1,0 lít.
C. 2,5 lít.
D. 2,0 lít.
Điện phân dung dịch CuCl2 (có dư) trong thời gian 386 giây, cường độ dòng điện là 10A. Khối lượng Cu thu được là
A. 6,4 gam.
B. 0,64 gam.
C. 1,28 gam.
D. 1,12 gam.
Có thể dùng một thuốc thử duy nhất để phân biệt 3 chất rắn Mg, Al, Al2O3 đựng trong các lọ mất nhãn. Thuốc thử đó là
A. dung dịch NH3.
B. dung dịch NaOH.
C. nước.
D. dung dịch HCl.
Điện phân dung dịch NaCl có màng ngăn, ở catốt thu được khí
A. O2.
B. H2, Cl2.
C. Cl2.
D. H2.
Nhỏ từ từ từng giọt đến hết 40 ml dung dịch HCl 1M vào 100 ml dung dịch chứa Na2CO3 0,15 M và NaHCO3 0,2M, sau phản ứng thu được số mol CO2 là
A. 0,025.
B. 0,015.
C. 0,020.
D. 0,010.
Cho 31,2 gam hỗn hợp bột Al và Al2O3 tác dụng với dung dịch NaOH dư thu được 13,44 lít H2 (ở đktc). Khối lượng Al2O3 có trong hỗn hợp ban đầu là
A. 20,4 gam.
B. 10,8g.
C. 8,1g.
D. 23,1g.
Điều nào sau đây không đúng với canxi?
A. Ion Ca2+ bị khử khi điện phân CaCl2 nóng chảy
B. Nguyên tử Ca bị oxi hoá khi Ca tác dụng với nước
C. Nguyên tử Ca bị khử khi Ca tác dụng với Cl2
D. Ion Ca2+ không bị khử khi Ca(OH)2 tác dụng với HCl
Phản ứng nào sau đây có phương trình ion thu gọn: CO2 + OH- → HCO3-
A. CO2 + Ca(OH)2; (tỉ lệ mol 2:1)
B. CO2 + NaOH; (tỉ lệ mol 1:2)
C. CO2 + Ca(OH)2; (tỉ lệ mol 1:1)
D. Na2CO3 + Ba(OH)2; (tỉ lệ mol 1:1)
Điện phân dung dịch X gồm FeCl2 và NaCl (tỉ lệ mol tương ứng là 1 : 2) với điện cực trơ màng ngăn xốp thu được dung dịch Y chứa hai chất tan, biết khối lượng dung dịch X lớn hơn khối lượng dịch Y là 4,54 gam. Dung dịch Y hòa tan tối đa 0,54 gam Al. Mặt khác dung dịch X tác dụng với lượng dư dung dịch AgNO3 thu được m gam kết tủa. Giá trị m là
A. 14,35.
B. 17,22.
C. 17,59.
D. 20,46.
Cho hỗn hợp gồm Na2O, CuO, Al2O3 có tỷ lệ mol 1:1:1 vào nước dư được chất rắn X. Dẫn H2 có dư đi qua X ở nhiệt độ cao được chất rắn Y. Y chứa
A. Cu và Al2O3.
B. Cu.
C. Cu và Al.
D. CuO.
Thực hiện các thí nghiệm sau:
(a) Cho dung dịch NaOH vào dung dịch Ca(HCO3)2.
(b) Cho dung dịch Fe(NO3)2 vào dung dịch AgNO3.
(c) Đun nóng nước cứng vĩnh cửu.
(d) Cho dung dịch HCl đến dư vào dung dịch NaAlO2.
(e) Cho dung dịch Ba(OH)2 dư vào dung dịch AlCl3.
(f) Cho dung dịch NaOH vào nước cứng tạm thời.
Số thí nghiệm thu được kết tủa sau phản ứng là
A. 6.
B. 5.
C. 3.
D. 4.
Cho từ từ x mol khí CO2 vào 500 gam dung dịch hỗn hợp KOH và Ba(OH)2. Kết quả thí nghiệm được biểu diễn trên đồ thị sau:
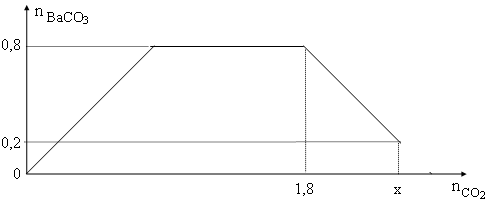
Nồng độ phần trăm của chất tan trong dung dịch sau phản ứng là
A. 45,11%.
B. 55,45%.
C. 51,08%.
D. 42,17%.
Để tách Ag từ hỗn hợp bột gồm Cu và Ag mà không làm thay đổi khối lượng của Ag ban đầu, người ta ngâm hỗn hợp trên vào một lượng dư dung dịch
A. Fe(NO3)3.
B. AgNO3.
C. Fe(NO3)2.
D. Cu(NO3)2.
Hai thanh kẽm có kích thước và khối lượng như nhau. Thanh (1) ngâm vào dung dịch CuSO4 0,5M, thanh (2) ngâm vào dung dịch MgSO4 0,5M. Sau một thời gian như nhau, lấy hai thanh ra làm khô, cân nặng thì khối lượng lúc này so với ban đầu là
A. (1) tăng, (2) giảm.
B. (1) giảm, (2) tăng.
C. (1) tăng, (2) không đổi.
D. (1) giảm (2) không đổi.
Phương trình hóa học nào sau đây là đúng?
A. Al2O3 + 3CO 2Al + 3CO2
B. CO2 + Ca(OH)2 dư Ca(HCO3)2
C. 2Na + O2 (khô) Na2O2
D. NaHCO3 NaOH + CO2
Hoà tan hết m gam hỗn hợp X gồm Na2O, K, K2O, Ba, BaO (trong đó oxi chiếm 8% khối lượng hỗn hợp) vào lượng nước dư thu được dung dịch Y và 1,792 lít H2 (đktc). Dung dịch Y hoà tan tối đa 8,64 gam Al. Giá trị của m là
A. 15,8.
B. 17,2.
C. 16,0.
D. 18,0.
Hỗn hợp X gồm 0,1 mol Na2O; 0,1 mol Ba; 0,5 mol Al. Cho X vào lượng nước dư đến khi phản ứng xảy ra hoàn toàn thì thu được V lít H2 (đktc). Giá trị của V là
A. 13,44.
B. 11,2.
C. 17,92.
D. 15,68.


