28 CÂU HỎI
Phản ứng thuận nghịch là phản ứng
A. xảy ra theo hai chiều ngược nhau trong cùng điều kiện.
B. có phương trình hoá học được biểu diễn bằng mũi tên một chiều.
C. chỉ xảy ra theo một chiều nhất định.
D. xảy ra giữa hai chất khí.
Yếu tố nào sau đây luôn luôn không làm dịch chuyển cân bằng của hệ phản ứng?
A. Nhiệt độ.
B. Nồng độ.
C. Chất xúc tác.
D. Áp suất.
Hằng số cân bằng KC của một phản ứng thuận nghịch phụ thuộc vào yếu tố nào sau đây?
A. Nồng độ.
B. Nhiệt độ.
C. Áp suất.
D. Chất xúc tác.
Khi phản ứng thuận nghịch đạt đến trạng thái cân bằng thì mối quan hệ giữa tốc độ phản ứng thuận (vt) với tốc độ phản ứng nghịch (vn) là
A. vt > vn.
B. vt = 2vn.
C. vt = vn.
D. vt < vn.
Xét phản ứng thuận nghịch tổng quát: aA + bB cC + d D.
Ở trạng thái cân bằng, hằng số cân bằng (KC) của phản ứng được xác định theo biểu thức:
A.\[{K_C} = \frac{{[A].[B]}}{{[C].[D]}}\]
B.\[{K_C} = \frac{{{{[A]}^a}.{{[B]}^b}}}{{{{[C]}^c}.{{[D]}^d}}}\]
C.\[{K_C} = \frac{{{{[C]}^c}.{{[D]}^d}}}{{{{[A]}^a}.{{[B]}^b}}}\]
D.\[{K_C} = \frac{{[C].[D]}}{{[A].[B]}}\]
Cho cân bằng hóa học sau:
CaCO3(s) CaO(s) + CO2(g) 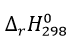 = 176 kJ
= 176 kJ
Yếu tố nào sau đây làm cho cân bằng dịch chuyển theo chiều thuận?
A. Tăng nồng độ khí CO2.
B. Tăng áp suất.
C.Giảm nhiệt độ.
D. Tăng nhiệt độ.
Cho cân bằng sau trong bình kín: 2NO2 (g) N2O4(g).
(màu nâu đỏ) (không màu)
Biết khi hạ nhiệt độ của bình thì màu nâu đỏ nhạt dần. Phản ứng thuận có
A.> 0, phản ứng tỏa nhiệt.
B. < 0, phản ứng tỏa nhiệt.
C.> 0, phản ứng thu nhiệt.
D. < 0, phản ứng thu nhiệt.
Chất nào sau đây không phải chất điện li?
A. C12H22O11.
B. NaOH.
C. NaCl.
D. HCl .
Chất nào sau đây thuộc loại chất điện li mạnh?
A. NaCl.
B. H2S.
C. CH3COOH.
D. C2H5OH.
Chất nào sau đây là chất điện li yếu?
A. CH3COOH.
B. FeCl3.
C. HNO3.
D. NaCl.
Cho phương trình:NH3 + H2O NH4+ + OH-
Trong phản ứng thuận, theo thuyết Bronsted – Lowry chất nào là base?
A. H2O.
B. NH3.
C. OH-.
D. NH4+.
Dung dịch chất nào sau đây có pH > 7?
A. NaNO3.
B. KCl.
C. H2SO4.
D. KOH.
Đối với dung dịch acid yếu CH3COOH 0,10 M, nếu bỏ qua sự điện li của nước thì đánh giá nào về nồng độ mol ion nào sau đây là đúng?
A. [H+] = 0,10 M.
B. [H+] < [CH3COO-].
C. [H+] > [CH3COO-].
D. [H+] < 0,10 M.
Nồng độ mol của ion NO3- trong dung dịch Ba(NO3)2 0,05M là
A. 0,020M.
B. 0,025M.
C. 0,100M.
D. 0,050M.
Trong dung dịch NaHCO3 (bỏ qua sự phân li của H2O) có những phần tử nào?
A. H+, HCO3-, Na+.
B. HCO3-, Na+.
C. H+, HCO3-, Na+, CO32-.
D. H+, CO32-, Na+.
Cho ba dung dịch có cùng nồng độ: hydrochloric acid (HCl), ethanol acid (acetic acid, CH3COOH) và sodium hydroxide (NaOH). Khi chuẩn độ riêng một thể tích như nhau của dung dịch HCl và dung dịch CH3COOH bằng dung dịch NaOH, phát biểu nào sau đây là đúng?
A.Trước khi chuẩn độ, pH của hai acid bằng nhau.
B.Tại các điểm tương đương, dung dịch của cả hai phép chuẩn độ đều có giá trị bằng 7.
C.Cần cùng một thể tích sodium hydroxide để đạt đến điểm tương đương.
D.Giá trị pH của hai acid tăng như nhau cho đến khi đạt điểm tương đương.
Ở trạng thái tự nhiên, nitrogen
A. tồn tại ở cả dạng đơn chất và dạng hợp chất.
B. chỉ tồn tại ở dạng đơn chất.
C. chỉ tồn tại ở dạng hợp chất.
D. tồn tại dạng tự do và chiếm khoảng 20% thể tích không khí.
Ở nhiệt độ thường, nitrogen khá trơ về mặt hoạt động hóa học là do
A. nitrogen có bán kính nguyên tử nhỏ.
B. nitrogen có độ âm điện lớn.
C. phân tử nitrogen có liên kết ba bền vững.
D. phân tử nitrogen không phân cực.
Ứng dụng nào sau đây không phải của N2?
A. Tổng hợp NH3.
B. Bảo quản máu, mẫu vật sinh học.
C. Diệt khuẩn, khử trùng.
D. Bảo quản thực phẩm.
Dạng hình học của phân tử ammonia là
A. hình tam giác đều.
B. hình tứ diện.
C. đường thẳng.
D. hình chóp tam giác.
Để tạo độ xốp cho một số loại bánh, có thể dùng chất nào sau đây?
A. (NH4)3PO4.
B. NH4HCO3.
C. CaCO3.
D. NaCl.
Có thể phân biệt ba dung dịch riêng biệt gồm: NH4Cl và (NH4)2SO4; Na2SO4 mà chỉ cần một dung dịch thuốc thử, đó là dung dịch
A. NaOH.
B. BaCl2.
C. Ba(OH)2.
D.Ba(NO3)2.
Phân tử nào sau đây có liên kết cho – nhận?
A. NH3.
B. N2.
C. HNO3.
D. H2.
KiN5m loại bị thụ động hóa trong dung dịch HNO3 đặc, nguội là
A. Mg.
B. Al.
C. Zn.
D. Cu.
Trong phân tử HNO3, nguyên tử N có số oxi hóa là
A. +5.
B. +3.
C. +4.
D. -3.
Nitric acid thường được sử dụng để phá mẫu quặng trong việc nghiên cứu, xác định hàm lượng các kim loại trong quặng do có
A. tính oxi hoá mạnh.
B. tính khử.
C. tính acid mạnh.
D. tính khử và tính axit mạnh.
Các oxide của nitrogen không được tạo thành trong trường hợp nào sau đây?
A. Núi lửa phun trào.
B. Đốt cháy các nhiên liệu hóa thạch.
C. Mưa dông, sấm sét.
D. Xả thải nước thải công nghiệp chưa qua xử lí.
Hợp chất nào của nitrogen không được tạo ra khi cho HNO3 tác dụng với kim loại?
A. NO.
B. N2O.
C. NO2.
D. N2O5.

