Bộ 5 đề thi cuối kì 1 Hóa 10 Kết nối tri thức (2022-2023) có đáp án - Đề 4
32 câu hỏi
Nguyên tử X, ion Y2+ và ion R- đều có cấu hình electron là 1s22s22p6. Kết luận nào sau đây đúng:
X: Phi kim; Y: Khí hiếm.
X: Khí hiếm; R: Kim loại.
Y: Phi kim; R: Khí hiếm.
X: Khí hiếm; R: Phi kim.
Cho cấu hình electron nguyên tử các nguyên tố sau:
(1) 1s22s1
(2) 1s22s22p63s23p1
(3) 1s22s22p5
(4) 1s22s22p63s23p4
(5) 1s22s22p63s2
Cấu hình của các nguyên tố phi kim là
(3), (4).
(2), (3).
(1), (2).
(2), (5).
Công thức nào sau đây ứng với công thức Lewis của phân tử PCl3 ?
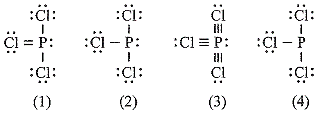
Công thức (3).
Công thức (4).
Công thức (2).
Công thức (1).
Nguyên tử X có cấu hình electron: 1s22s22p5. Vị trí của X trong bảng tuần hoàn là
ô thứ 9; chu kỳ 2; nhóm VB.
ô thứ 9; chu kỳ 2; nhóm VA.
ô thứ 9; chu kỳ 2; nhóm VIIB.
ô thứ 9; chu kỳ 2; nhóm VIIA.
Cho dãy các chất sau Cu, O2, N2, HCl, H2SO4, O2, NH4NO3, Al, He, H2O. Số lượng các đơn chất là
7
6
5
4
Các chất sau: Na2O, H2O, NH3, MgCl2, CO2, KF, NH4Cl. Số chất có liên kết ion là
4.
3.
6.
5.
Nguyên tố hóa học là những nguyên tử có cùng
số neutron.
số neutron và số proton.
số khối.
số proton.
Điều nào dưới đây đúng khi nói về ion 1 6 3 2 S 2 − ?
Có chứa 18 proton.
Tổng số hạt của ion là 50 hạt
Có chứa 16 electron.
Trung hoà về điện.
Cho độ âm điện của các nguyên tố như sau: O (3,44), Cl (3,16), Mg (1,31), C (2,55), H (2,2). Trong các phân tử: MgO, CO2, CH4, Cl2O. Số chất có chứa liên kết cộng hóa trị có cực là
2.
1.
3.
4.
Tìm câu sai trong các câu sau:
Nguyên tử có kích thước vô cùng nhỏ và trung hoà về điện.
Khối lượng nguyên tử hầu hết tập trung ở hạt nhân.
Nguyên tử có cấu trúc đặc khít, gồm vỏ nguyên tử và hạt nhân nguyên tử.
Trong nguyên tử, hạt neutron không mang điện.
Liên kết trong phân tử nào sau đây được hình thành nhờ sự xen phủ orbital s – p ?
NH3
H2
O2
Cl2
Tìm câu sai trong các câu sau:
Cả (1) và (2) đều là quá trình biến đổi vật lí.
(1) là quá trình biến đổi hóa học, (2) là quá trình biến đổi vật lí.
(1) là quá trình biến đổi vật lí, (2) là quá trình biến đổi hóa học.
Cả (1) và (2) đều là quá trình biến đổi hóa học.
Cho các nguyên tố 4Be, 3Li, 11Na, 19K. Nguyên tố có tính kim loại mạnh nhất là
Be
K
Na
Li
Nhóm A bao gồm các nguyên tố
nguyên tố d và nguyên tố f.
nguyên tố s.
nguyên tố s và nguyên tố p.
nguyên tố p.
Trong nguyên tử, loại hạt có khối lượng không đáng kể so với các hạt còn lại là
electron.
proton.
neutron và electron.
neutron.
Để đạt quy tắc octet, nguyên tử của nguyên tố potassium (Z = 19) phải
nhận thêm 1 electron.
nhường đi 2 electron.
nhường đi 1 electron.
nhận thêm 2 electron.
Sự phân bố electron theo ô orbital nào dưới đây là đúng?

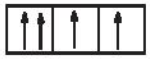
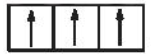
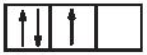
Nhóm nguyên tố là tập hợp các nguyên tố mà nguyên tử của nó có cùng
số lớp electron.
số electron lớp ngoài cùng.
số electron hóa trị.
số electron.
Các nguyên tố X, Y, Z có cấu hình electron nguyên tử lần lượt là: 1s22s22p5; 1s22s22p63s1; 1s22s22p63s23p4. Dãy gồm các nguyên tố xếp theo thứ tự tăng dần độ âm điện là
Y, Z, X
X, Z, Y
Y, Z, X
X, Y, Z
Trong mỗi chu kì, theo chiều tăng của điện tích hạt nhân, bán kính nguyên tử của các nguyên tố…….; tính kim loại của các nguyên tố……… Cặp từ thích hợp điền vào chỗ trống theo thứ tự là
giảm dần; tăng dần
tăng dần; giảm dần
tăng dần; tăng dần
giảm dần; giảm dần
Nhận định nào sau đây đúng khi nói về 3 nguyên tử: 1 3 2 6 X , 2 6 5 5 Y , 1 2 2 6 Z ?
X, Z là 2 đồng vị của cùng một nguyên tố hoá học.
X, Y thuộc cùng một nguyên tố hoá học.
X và Z có cùng số khối.
X và Y có cùng số neutron.
Nguyên tố R thuộc chu kì 3, nhóm VA của bảng tuần hoàn các nguyên tố hóa học. Công thức oxide cao nhất của R là
R2O5.
R2O3.
R2O.
RO3.
Anion X2- có cấu hình electron [Ne]3s23p6. Nguyên tố X có tính chất nào sau đây?
kim loại
phi kim
lưỡng tính
trơ của khí hiếm
Trong nguyên tử, hạt mang điện là
electron.
electron và neutron.
proton và neutron.
proton và electron.
Phân tử nào sau đây có liên kết cộng hóa trị không cực?
H2O.
HCl.
NH3.
Cl2.
Cho Na (Z =11), O (Z=8), Al (Z =13), khi tham gia liên kết thì các nguyên tử Na, O, Al có xu hướng tạo thành ion
Na2+, O2+, Al3+.
Na+, O+, Al+.
Na+, O2-, Al3+.
Na2+, O-, Al+.
Cho chất hữu cơ A có công thức cấu tạo sau:
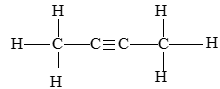
Số liên kết σ trong phân tử A là
11
9
6
8
Trong các hợp chất, nguyên tử Magnesium ( 1 2 2 4 M g ) đã đạt cấu hình bền vững của khí hiếm gần nhất bằng cách
nhận vào 2 electron.
nhận vào 1 electron.
cho đi 2 electron.
cho đi 3 electron.
Cho các nguyên tố: Fe (Z = 26); P (Z = 15).
(a). Viết cấu hình electron của Fe, P.
(b). Xác định vị trí của Fe, P trong bảng tuần hoàn.
Hai nguyên tố X và Y đứng kế tiếp nhau trong một chu kỳ, có tổng số điện tích hạt nhân bằng 25.
(a) Hãy viết cấu hình electron của nguyên tử X và Y.
(b) Xác định vị trí của X, Y trong bảng tuần hoàn và tên nguyên tố X, Y.
Nguyên tử khối trung bình của bromine là 79,91. Bromine có 2 đồng vị, trong đó đồng vị 79Br chiếm 54,5% số nguyên tử.
(a) Tính nguyên tử khối của đồng vị còn lại.
(b) Tính % khối lượng của đồng vị 79Br có trong phân tử HBrO4.
Oxide cao nhất của nguyên tố R có công thức RO3. Hợp chất khí của nó với hydrogen có 5,88 % hydrogen về khối lượng. Tìm R.








