Bộ 5 đề thi cuối kì 1 Hóa 10 Kết nối tri thức (2022-2023) có đáp án - Đề 3
32 câu hỏi
Đặc điểm của hạt neutron là
mang điện tích dương và có khối lượng.
mang điện tích âm và có khối lượng.
không mang điện và có khối lượng.
mang điện tích âm và không có khối lượng.
Lớp M có số electron tối đa là
32.
18.
8.
2.
Phân lớp nào sau đây không tồn tại?
1s.
3p.
4d.
2f.
Số nguyên tố trong chu kì 3 là
2.
8.
18.
32.
X thuộc nhóm VA. Công thức oxide cao nhất của X là
XO2.
XO.
XO3.
X2O5.
Trong một chu kì, theo chiều tăng của điện tích hạt nhân biến đổi nào sau đây đúng?
Tính acid giảm.
Bán kính nguyên tử tăng.
Tính phi kim giảm.
Độ âm điện tăng.
Nguyên tử nguyên tố nhóm IA nào sau đây có bán kính lớm nhất?
Li (Z=3).
Na (Z=11).
K (Z=19).
Cs (Z=55).
Cấu hình electron hóa trị của nguyên tử các nguyên tố nhóm IVA trong bảng tuần hoàn là
np2.
ns2.
ns2np2.
ns2np4.
Theo quy tắc octet, xu hướng chung của các nguyên tử nguyên tố nhóm IIA là nhường
2 electron.
3 electron.
1 electron.
4 electron.
Sodium chloride là một hợp chất có thể tan trong nước lạnh và có nhiệt độ nóng chảy cao. Liên kết trong phân tử sodium chloride là liên kết
cộng hóa trị không phân cực.
liên kết ion.
hydrogen.
cộng hóa trị phân cực.
Trong các hợp chất sau: CaO, Ba(NO3)2, Na2O, KF, K2SO4, NH4Cl, số hợp chất không chứa ion đa nguyên tử là
2.
3.
4.
5.
Phân tử nào sau đây có liên kết ion?
NH3.
H2S.
HCl.
NaBr.
Liên kết cộng hóa trị là liên kết được hình thành giữa hai nguyên tử
bằng nhiều electron chung.
bằng sự cho – nhận electron.
bằng một hay nhiều cặp electron chung.
bằng một hay nhiều electron độc thân.
Phân tử nào sau đây có liên kết cộng hóa trị phân cực?
O2.
H2S.
C2H2.
NH3.
Phát biểu nào sau đây về tính chất của hợp chất cộng hóa trị là sai?
Có nhiệt độ nóng chảy và nhiệt độ sôi thấp.
Tồn tại ở thể rắn, lỏng hoặc khí trong điều kiện thường.
Tất cả các hợp chất cộng hóa trị đều dẫn điện tốt.
Hợp chất cộng hóa trị phân cực tan tốt trong dung môi phân cực.
Cho sơ đồ liên kết giữa hai phân tử acid CH3COOH: 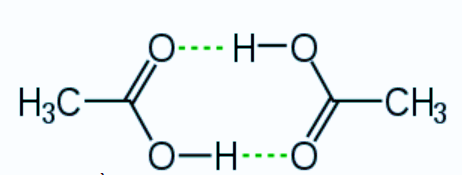
Trong sơ đồ trên, đường nét đứt đại diện cho
Liên kết ion.
Liên kết hydrogen.
Liên kết cộng hóa trị.
Liên kết cho - nhận
Nguyên tử 1 3 2 8 Al có số lượng các loại hạt proton, electron và neutron lần lượt là:
15, 13 và 13.
15, 15 và 13.
13, 13 và 15.
13, 15 và 13.
Nguyên tố có Z= 25 thuộc loại nguyên tố
f.
s.
p.
d.
Nguyên tố ở chu kì 3, nhóm VA có cấu hình electron là
[Ne]3s23p1.
[Ne]3s23p4.
[Ne]3s23p3.
[Ne]3s23p6.
Cho cấu hình electron nguyên tử các nguyên tố sau: X (1s22s22p63s23p64s1), Y (1s22s22p63s1), Z (1s22s22p63s2), T (1s22s2). Dãy các nguyên tố được sắp xếp theo chiều tăng dần tính kim loại từ trái sang phải là:
T, Z, X, Y.
X, Y, T, Z.
T, Z, Y, X.
T, Y, Z, X.
Cho các nguyên tố cùng chu kỳ: 11Na ,12Mg, 13Al và 14Si. Dãy các nguyên tố được sắp xếp theo chiều tăng dần tính phi kim từ trái sang phải là:
Na, Si, Mg, Al.
Na, Mg, Al, Si.
Si, Al, Mg, Na.
Si, Na, Al, Mg.
Phát biểu nào sau đây về Ca (Z=20) không đúng?
Có 2 electron hóa trị.
Là nguyên tố s.
Hóa trị cao nhất với oxygen là II.
Hydroxide cao nhất của calcium có tính axit.
Theo quy tắc octet nguyên tử nào sau đây nhường 1 electron để đạt cấu trúc ion bền?
X (Z = 8).
Y (Z = 9).
T (Z = 11).
Q (Z = 12).
Cho các phát biểu sau về hợp chất ion:
(a) Liên kết được tạo thành do lực hút tĩnh điện giữa các ion mang điện tích trái dấu.
(b) Được tạo thành giữa kim loại điển hình và phi kim điển hình.
(c) Có nhiệt độ nóng chảy và nhiệt độ sôi cao.
(d) Thường tồn tại ở trạng thái khí ở điều kiện thường.
Số phát biểu đúng là
2.
1.
3.
4.
Nguyên tử X có 20 electron, nguyên tử Y có 9 electron. Công thức hợp chất và loại liên kết hình thành giữa hai nguyên tử này là
XY2, liên kết ion.
X3Y2, liên kết cộng hóa trị.
X2Y, liên kết cộng hóa trị.
XY, liên kết ion.
Phân tử Cl2 được hình thành thừ sự xen phủ nào?
 .
.
 .
.
 .
.
 .
.
Dãy nào sau đây gồm các phân tử đều phân cực?
HCl, N2, NaCl, H2O.
HCl, NH3, NaCl, CO2.
HCl, NH3, NaCl, O2.
HCl, NH3, NaCl, H2O.
Chất nào sau đây không thể tạo được liên kết hydrogen?
H2O.
C2H4.
CH3OH.
NH3.
(1 điểm)
(a) Trong bản tuần hoàn các nguyên tố hóa học, các nguyên tố được sắp xếp theo những nguyên tắc nào?
(b) Nguyên tố X là là một thành phần quan trọng của khẩu phần dinh dưỡng. Sự thiếu hụt rất nhỏ của nó đã ảnh hưởng tới sự hình thành và phát triển của xương và răng. Nguyên tố X thuộc chu kì 4, nhóm IIA trong bản tuần hòa. Viết cấu hình e của nguyên tố X.
(1 điểm)
(a) Viết hai giai đoạn của sự hình thành NaCl từ các nguyên tử tương ứng (kèm theo cấu hình electron).
(b) Viết công thức electron và công thức Lewis của phân tử NH3.
(0,5 điểm) Dựa vào kiến thức đã học về liên kết hóa học hãy giải thích vì sao ethanol C2H5OH tan vô hạn trong nước, khí nitrogen tan ít trong nước.
(0,5 điểm) Hợp chất M2X có tổng số hạt cơ bản trong phân tử là 116, trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 36. Số khối của X lớn hơn M là 9. Tổng số hạt trong X2- nhiều hơn trong M+ là 17. Tính số neutron của nguyên tử M và X.








