Bộ 3 đề thi cuối kì 2 Hóa 12 Cánh diều cấu trúc mới có đáp án - Đề 3
28 câu hỏi
PHẦN I (4,5 điểm). Câu trắc nghiệm nhiều phương án lựa chọn. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
Điện phân CaCl2 nóng chảy, ở cathode xảy ra quá trình nào?
Oxi hóa ion Ca2+.
Khử ion Ca2+.
Oxi hóa ion Cl−.
Khử ion Cl−.
Khi điện phân dung dịch gồm Cu(NO3)2 0,1 M và AgNO3 0,1 M, quá trình oxi hóa xảy ra ở anode là
2H2O → 4H++ O2 + 4e.
2H2O + 2e → H2 + 2OH–.
Cu2+ + 2e → Cu.
Ag+ + 1e → Ag.
Ion halide hầu như không bị điện phân trong dung dịch là
\[{\rm{B}}{{\rm{r}}^{\rm{ - }}}\].
\[{{\rm{I}}^{\rm{ - }}}\].
\[{{\rm{F}}^{\rm{ - }}}\].
\[{\rm{C}}{{\rm{l}}^{\rm{ - }}}\].
Phát biểu nào dưới đây không đúng?
Các electron nằm ở nút mạng tinh thể và các electron chuyển động tự do xung quanh.
Kiểu mạng lập phương tâm khối có độ đặc khít là 68%.
Tất các kim loại kiềm và kim loại kiềm thổ đều có kiểu mạng lập phương tâm khối nên dễ có tính khử mạnh.
Số phối trí trong kiểu mạng lập phương tâm khối là 8.
Tính chất nào của thủy ngân giúp nó được sử dụng trong nhiệt kế?
Có độc tính mạnh.
Có khối lượng riêng nặng hơn nước.
Có nhiệt độ nóng chảy thấp hơn nhiệt độ phòng.
Có nhiệt độ sôi thấp hơn nhiệt độ phòng.
Cho dãy các kim loại sau: K, Ca, Mg, Fe, Cu. Số kim loại trong dãy có khả năng tác dụng với nước ở điều kiện thường là
5.
4.
3.
2.
Lần lượt nối thanh Zn với mỗi kim loại sau đây và cho vào dung dịch HCl. Quá trình ăn mòn thanh Zn xảy ra nhanh nhất khi nối với
Mg.
Pb.
Ag.
Cu.
Kim loại Li nên được bảo quản trong
dầu hoả khan.
phenol.
khí trơ.
bình hút ẩm.
Quá trình nào sau đây dùng để tách kim loại Na từ hợp chất?
Dung dịch NaOH tác dụng với dung dịch HCl.
Điện phân NaCl nóng chảy.
Dung dịch \({\rm{N}}{{\rm{a}}_2}{\rm{C}}{{\rm{O}}_3}\) tác dụng với dung dịch HCl.
Dung dịch NaCl tác dụng với dung dịch \({\rm{AgN}}{{\rm{O}}_3}.\)
Phân kali đỏ (chứa KCl) là một loại phân bón đa lượng phổ biến trên thị trường vì giá thành rẻ, phù hợp rất nhiều loại đất khác nhau và hàm lượng potassium cao. Phân kali đỏ thường được sản xuất từ quặng sylvinite bằng cách tách muối KCl ra khỏi quặng theo sơ đồ sau:
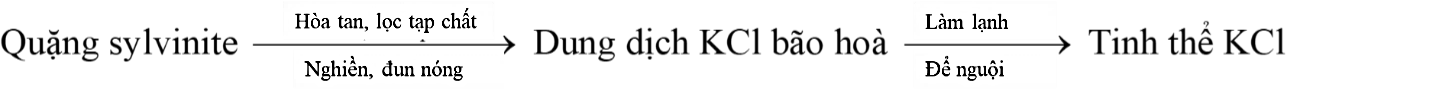
Phương pháp nào sau đây dùng để tách KCl ở trên?
Sắc kí.
Chưng cất.
Chiết.
Kết tinh.
Khi đun nóng đến 60 °C, thạch cao sống mất một phần nước trở thành thạch cao nung, được dùng để đúc khuôn trong điêu khắc, bó bột trong y học. Thành phần chính của thạch cao nung là
CaSO4.0,5H2O.
Ca(H2PO4)2.
CaCO3.
Ca(OH)2.
Có thể nhận biết dung dịch BaCl2 bằng dung dịch chất nào sau đây?
NaOH.
Na2CO3.
NaCl.
NaNO3.
Barium phản ứng với nước dễ dàng hơn so với magnesium ở điều kiện thường là do các nguyên nhân nào sau đây?
(1) Barium có tính khử mạnh hơn magnesium.
(2) Độ tan của barium hydroxide trong nước cao hơn nhiều so với magnesium hydroxide.
(3) Bọt khí hydrogen sinh ra bám trên bề mặt magnesium nhiều hơn, cản trở phản ứng tiếp diễn.
(1).
(1), (2) và (3).
(1) và (3).
(1) và (2).
Bình thuỷ dùng để đun nước lâu ngày bị đóng cặn, có thể dùng dung dịch nào sau đây để hoà tan lớp cặn?
Nước vôi.
Rượu uống.
Giấm ăn.
Muối ăn.
Đặc điểm chung cấu hình electron của nguyên tử kim loại chuyển tiếp dãy thứ nhất là
[Ne]3d1÷104s1÷2.
[Ar]3d1÷104s1÷2.
[Ar]3d1÷104s2.
[Ar]3d104s1÷2.
Kim loại nào sau đây thuộc dãy kim loại chuyển tiếp thứ nhất?
Ti.
Al.
Ba.
Na.
Phát biểu nào dưới đây là sai?
Nguyên tử trung tâm là cation kim loại hoặc nguyên tử kim loại có orbital trống đã nhận cặp electron chưa liên kết của phối tử.
Phối tử cho cặp electron chưa liên kết vào orbital trống của nguyên tử trung tâm.
Phức lập phương chỉ biết đối với các ion có kích thước rất lớn so với kích thước phối tử.
Phức chất luôn mang điện tích dương hoặc âm.
Nguyên tử trung tâm của phức [Co(NH3)6]3+ là ?
N.
Co.
Co3+.
NH3.
PHẦN II (4 điểm). Câu trắc nghiệm đúng sai. Thí sinh trả lời từ câu 1 đến câu 4. Trong mỗi ý a), b), c), d) ở mỗi câu, thí sinh chọn đúng hoặc sai. (Đ – S)
Điện phân MgCl2 nóng chảy. MgCl2 nóng chảy phân li thành các ion Mg2+ và ion Cl−.
Cation Mg2+ di chuyển về cực âm (cathode) và anion Cl− di chuyển về cực dương (anode) của bình điện phân.
Tại cathode xảy ra quá trình oxi hóa: Mg2+ + 2e ⟶ Mg.
Tại anode xảy ra quá trình khử: 2 Cl− ⟶ Cl2 + 2e.
Có thể điều chế Mg từ MgCl2 bằng phương pháp nhiệt luyện.
Công đoạn chính của công nghiệp chlorine – kiềm là điện phân dung dịch sodium chlorine bão hòa trong bể điện phân có màng ngăn xốp. Phương trình hóa học của quá trình điện là: 2NaCl + 2H2O 2NaOH + H2 + Cl2.
Anion Cl – bị khử thành khí chlorine tại anode.
Tại cathode, thu được đồng thời dung dịch bão hòa và tinh thể sodium hydroxide.
Nếu không có màng ngăn xốp, nước Javel được hình thành trong bể điện phân.
Hydrogen cũng là một sản phẩm có giá trị của công nghiệp chlorine – kiềm.
Magnesium \(({\rm{Mg}})\) là kim loại được ứng dụng để tạo các hợp kim nhẹ, bền, đặc biệt là cho ngành công nghiệp sản xuất ô tô và hàng không vũ trụ. Magnesium được sản xuất trong công nghiệp theo quá trình Pidgeon với nguyên liệu ban đầu là quặng dolomite. Quá trình được thực hiện qua các giai đoạn sau:
Giai đoạn 1. Nung quặng dolomite:
MgCO3⋅CaCO3(s)→t°MgO(s)+CaO(s)+2CO2( g)
Giai đoạn 2. Dùng Si trong ferrosilicon \(({\rm{Fe}},{\rm{Si}})\) làm chất khử trong điều kiện chân không:
2MgO(s)+2CaO(s)+Si(s)→t°2Mg(g)+Ca2SiO4(s)
Phản ứng chung của quá trình Pidgeon là:
2MgCO3.CaCO3(s)+Si(s)→t°2Mg(s)+Ca2SiO4(s)+2CO2(g) ΔrH298°~183 kJ
Quá trình Pidgeon là quá trình thu nhiệt.
Phản ứng ở giai đoạn (2) thuộc phương pháp nhiệt luyện.
Phản ứng ở giai đoạn (2) chứng tỏ MgO có tính oxi hoá mạnh hơn CaO.
Nếu hiệu suất của quá trình là 90% thì cứ 1 tấn quặng dolomite sẽ điều chế được 120 kg kim loại magnesium.
Một phức chất có công thức [Fe(H2O)6](NO3)3.
Nguyên tử trung tâm là cation Fe2+.
Phối tử là \[NO_3^ - \].
Trong phức chất trên nguyên tử Fe chiếm 16% về khối lượng.
Tỉ lệ khối lượng của phối tử và nguyên tử trung tâm là 14 : 27.
PHẦN III (1,5 điểm). Câu hỏi trắc nghiệm yêu cầu trả lời ngắn.Thí sinh trả lời từ câu 1 đến câu 6.
Cho các kim loại sau: Na, Ca, Fe, Al, Zn, Cu, Ag. Có bao nhiêu kim loại được điều chế trong công nghiệp bằng phương pháp điện phân hợp chất nóng chảy của chúng?
3
Tiến hành 2 thí nghiệm sau:
- Thí nghiệm 1: cho m gam bột Fe (dư) vào V1 lít dung dịch Cu(NO3)2 1M.
- Thí nghiệm 2: cho m gam bột Fe (dư) vào V2 lít dung dịch AgNO3 0,1M.
Sau khi các phản ứng xảy ra hoàn toàn, khối lượng chất rắn thu được ở hai thí nghiệm đều bằng nhau. Tỉ lệ \(\frac{{{V_1}}}{{{V_2}}}\) là?
1
Điện phân 2 lít dung dịch NaCl 0,5 M với điện cực trơ, màng ngăn xốp bằng dòng điện có cường độ không đổi 0,2 A. Sau 1930 giây thì dừng điện phân, thu được dung dịch X (giả thiết thể tích dung dịch không đổi). Dung dịch X có pH bằng bao nhiêu? (Làm tròn kết quả đến hàng phần mười).
11,3
Ở điều kiện thường, tinh thể Ca có D = 1,55 g/cm3. Giả thiết các nguyên tử Ca là những hình cầu chiếm 74% thể tích tinh thể, phần còn lại là khe rỗng.
Cho biết:
- Công thức tính thể tích hình cầu: V = \[\frac{4}{3}\].π.r3
- Số Avogadro NA= 6,023.1023 và số pi π = 3,1416.
Bán kính nguyên tử Ca là bao nhiêu pm? (Làm tròn kết quả đến hàng đơn vị).
196
Dung dịch iron(II) sulfate để lâu ngày bị oxi hóa một phần bởi oxygen của không khí tạo thành iron(III) sulfate (hỗn hợp X). Cho 30 mL dung dịch H2SO4 0,5M vào 10 mL hỗn hợp X thu được dung dịch Y.
• Thí nghiệm 1: Chuẩn độ 10,0 mL dung dịch Y bằng dung dịch KMnO4 0,05M cho đến khi xuất hiện màu hồng nhạt bền (phản ứng coi như vừa đủ) thì thấy hết 9,0 mL dung dịch KMnO4.
• Thí nghiệm 2: Ngâm một lá sắt dư vào 10,0 mL dung dịch Y, khuấy đều đến khi khử hoàn toàn sắt(III) thành Fe(II). Lấy lá sắt ra, rồi chuẩn độ bằng dung dịch KMnO4 0,05M. Khi màu hồng nhạt bền xuất hiện thì thấy hết 10,5 mL dung dịch KMnO4. Tỉ lệ iron (II) sulfate đã bị oxi hóa trong không khí là a%. Giá trị của a bằng bao nhiêu? (kết quả làm tròn đến hàng đơn vị).
10
Sắt là kim loại chuyển tiếp dãy thứ nhất, có khả năng tạo phức chất phong phú và có nhiều ứng dụng thực tiễn: [Fe(H2O)6]SO4; K4[Fe(CN)6]; [Fe(CO)5]; [Fe(H2O)6]Cl3. Có bao nhiêu phức chất trong đó nguyên tử trung tâm là Fe2+?
2








