Bộ 3 đề thi cuối kì 2 Hóa 10 Kết nối tri thức cấu trúc mới có đáp án - Đề 3
28 câu hỏi
PHẦN I. Câu trắc nghiệm nhiều phương án lựa chọn. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
Chất xúc tác là
chất làm giảm tốc độ phản ứng, nhưng không bị tiêu hao trong phản ứng.
chất làm tăng tốc độ phản ứng, nhưng bị tiêu hao trong phản ứng.
chất làm tăng tốc độ phản ứng nhưng không bị thay đổi cả lượng và chất sau khi phản ứng kết thúc.
chất làm thay đổi tốc độ phản ứng, nhưng bị tiêu hao không nhiều trong phản ứng.
Thông thường đối với các phản ứng có chất khí tham gia, khi tăng áp suất, tốc độ phản ứng
giảm.
không đổi.
tăng.
không xác định được.
Cho các phản ứng sau:
(1) Phản ứng than cháy trong không khí.
(2) Phản ứng tạo gỉ sắt.
(3) Phản ứng nổ của khí bình gas.
(4) Phản ứng lên men rượu.
Phản ứng xảy ra với tốc độ nhanh nhất là
(1).
(2).
(3).
(4).
Hình ảnh dưới đây minh họa ảnh hưởng của yếu tố nào tới tốc độ phản ứng: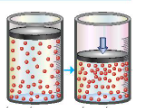
Áp suất.
Nhiệt độ.
Diện tích bề mặt tiếp xúc.
Chất xúc tác.
Cho phương trình phản ứng tổng quát sau: 2A + B → C.
Tốc độ phản ứng tại một thời điểm được tính bằng biểu thức:\[v = kC_A^2{C_B}\].
Hằng số tốc độ k phụ thuộc vào yếu tố nào sau đây?
Nồng độ của chất.
Nồng độ của chất B.
Nhiệt độ của phản ứng.
Thời gian xảy ra phản ứng.
Khí oxygen được điều chế trong phòng thí nghiệm bằng cách nhiệt phân potassium chlorate với xúc tác manganes dioxide. Để thí nghiệm thành công và rút ngắn thời gian tiến hành có thể dùng một số biện pháp sau:
(1) Trộn đều bột potassium chlorate và xúc tác.
(2) Nung ở nhiệt độ cao.
(3) Dùng phương pháp dời nước để thu khí oxygen.
(4) Nghiền nhỏ potassium chlorate.
Số biện pháp dùng để tăng tốc độ phản ứng là
2.
3.
4.
5.
Cho phản ứng đơn giản sau (xảy ra trong bình kín):
2NO(g) + O2(g) → 2NO2(g)
Ở nhiệt độ không đổi, nồng độ NO tăng hai lần, nồng độ O2 không đổi thì
tốc độ phản ứng không thay đổi.
tốc độ phản ứng tăng 2 lần.
tốc độ phản ứng tăng 4 lần.
tốc độ phản ứng giảm 2 lần.
Ở 35oC, phản ứng có tốc độ là 0,036 mol/ (L.h); ở 45oC, phản ứng có tốc độ là 0,09 mol/ (L.h). Hệ số nhiệt độ γ của phản ứng là
1,5.
2.
2,5.
3.
Trong bảng tuần hoàn các nguyên tố hóa học, các nguyên tố halogen thuộc nhóm
IA.
VIIA.
VA.
VIIIA.
Halogen nào được dùng trong sản xuất nhựa Teflon?
Fluorine.
Iodine.
Chlorine.
Bromine.
Cho các phản ứng hóa học sau, phản ứng nào chứng minh Cl2 có tính oxi hoá mạnh hơn Br2?
Br2 + 2NaCl → 2NaBr + Cl2.
Cl2 + 2NaOH → NaCl + NaClO + H2O.
Br2 + 2NaOH → NaBr + NaBrO + H2O.
Cl2 + 2NaBr → 2NaCl + Br2.
Nhỏ vài giọt dung dịch nào sau đây vào dung dịch AgNO3 thu được kết tủa màu vàng nhạt.
HCl.
NaBr.
NaCl.
HF.
Ở trạng thái lỏng, giữa các phân tử hydrogen halide nào sau đây tạo được liên kết hydrogen mạnh?
HCl.
HI.
HF.
HBr.
Hydrohalic acid thường được dùng để đánh sạch bề mặt kim loại trước khi sơn, hàn, mạ điện là
HBr.
HF.
HI.
HCl.
Nguyên nhân dẫn tới nhiệt độ nóng chảy, nhiệt độ sôi của các đơn chất halogen tăng từ fluorine đến iodine là do từ fluorine đến iodine,
khối lượng phân tử và tương tác van der Walls đều tăng.
tính phi kim giảm và tương tác van der Walls tăng.
khối lượng phân tử tăng và tương tác van der Walls giảm.
độ âm điện và tương tác van der Walls giảm.
Phát biểu nào sau đây không đúng?
Trong các hợp chất, ngoài số oxi hoá –1, fluorine còn có các số oxi hoá +1, +3, +5, +7.
Muối AgI không tan trong nước, muối AgF tan trong nước.
Fluorine có tính oxi hóa mạnh hơn chlorine.
Dung dịch HF hòa tan được SiO2.
Cho lượng dư dung dịch AgNO3 tác dụng với 100 ml dung dịch hỗn hợp NaF 0,05M và NaCl 0,1M. Khối lượng kết tủa thu được là
1,345 gam.
3,345 gam.
2,875 gam.
1,435 gam.
Cho 8,4 gam CaCO3 tác dụng hết với dung dịch HCl dư, thu được V lít khí CO2 (đkc). Giá trị của V là
2,24 L.
2,479 L.
3,36 L.
3,719 L.
PHẦN II. Câu trắc nghiệm đúng sai. Thí sinh trả lời từ câu 1 đến câu 4. Trong mỗi ý a), b), c), d) ở mỗi câu, thí sinh chọn đúng hoặc sai. (Đ – S)
Sản xuất gang trong công nghiệp bằng cách sử dụng khí CO khử Fe2O3 ở nhiệt độ cao theo phản ứng sau:
Fe2O3+3CO→t°2Fe+3CO2(*)
Trong các phát biểu sau, phát biểu sai là
Phản ứng (*) là phản ứng oxi hoá – khử.
CO đóng vai trò là chất khử trong phản ứng.
CO2 đóng vai trò là chất oxi hoá trong phản ứng.
Số oxi hoá của Fe giảm từ +2 xuống 0 sau phản ứng.
Phản ứng của 1 mol enthanol lỏng với oxygen xảy ra theo phương trình:
C2H5OH(l) + O2(g) → CO2(g) + H2O(l)
Những nhận định nào sau đây là đúng?
Đây là phản ứng tỏa nhiệt vì nó tạo ra khí CO2 và nước lỏng.
Đây là phải là phản ứng oxi hóa – khử với tổng số hệ số cân bằng trong phương trình phản ứng là 9.
Biến thiên enthalpy chuẩn của phản ứng sẽ thay đổi nếu nước tạo ra ở thể khí.
Sản phẩm của phản ứng chiếm một thể tích lớn hơn so với chất phản ứng.
Thí nghiệm nghiên cứu ảnh hưởng của diện tích bề mặt đến tốc độ phản ứng:
CaCO3 + 2HCl → CaCl2 + CO2 + H2O
Chuẩn bị: 2 bình tam giác, dung dịch HCl 0,5 M, đá vôi dạng viên, đá vôi đập nhỏ.
Tiến hành:
- Cho cùng một lượng (khoảng 2 g) đá vôi dạng viên vào bình tam giác (1) và đá vôi đập nhỏ vào bình tam giác (2).
- Rót 20 mL dung dịch HCl 0,5 M vào mỗi bình.
Phản ứng trong bình 1 có tốc độ thoát khí nhanh hơn.
Đá vôi dạng đập nhỏ có tổng diện tích bề mặt lớn hơn.
Diện tích bề mặt tiếp xúc càng lớn thì tốc độ phản ứng càng chậm.
Phản ứng trên thuộc loại phản ứng oxi hóa – khử.
Trong công nghiệp, dung dịch sodium chloride bão hoà được đem điện phân. Phản ứng điện phân xảy ra theo sơ đồ sau:
NaCl (aq) + H2O (l) → A (aq) + X (g) + Y (g) (*)
Biết khí Y làm quỳ tím chuyển sang màu đỏ sau đó mất màu.
Từ phản ứng giữa Y với dung dịch A sẽ sản xuất được hỗn hợp tẩy rửa phổ biến là nước Javel.
Từ phản ứng kết hợp giữa X và Y sẽ sản xuất được hydrogen chloride.
Công thức hóa học của A, X, Y lần lượt là Na(OH)2, Cl2, H2
Phương trình hóa học (*): 2NaCl (aq) + 2H2O (l) 2NaOH (aq) + H2 (g) + Cl2 (g)
Phần III. Câu hỏi trắc nghiệm yêu cầu trả lời ngắn. Thí sinh trả lời từ câu 1 đến câu 6.
Cho 2,7 gam kim loại R tác dụng hết với khí chlorine thu được 13,35 gam muối. Xác định kim loại R.
Hình vẽ dưới đây mô tả thí nghiệm điều chế và thu khí chlorine trong phòng thí nghiệm. Vai trò của bình chứa dung dịch NaCl và bông tẩm dung dịch NaOH lần lượt là?
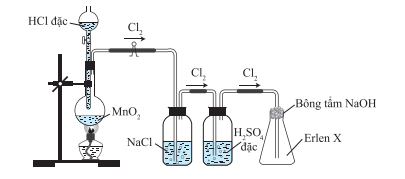
Viết 1 phương trình hoá học chứng minh chlorine vừa có tính oxi hoá, vừa có tính khử.
Cho từ từ đến hết 10 g dung dịch X gồm NaF 0,84% và NaCl 1,17%, vào dung dịch AgNO3 dư, thu được m gam kết tủa. Tính giá trị của m.
Cho m gam KClO3 tác dụng với HCl đến khi phản ứng xảy ra hoàn toàn thấy thoát ra V lít khí Cl2 ở đkc. Biết lượng Cl2 sinh ra phản ứng vừa đủ với 0,56 gam Fe. Xác định m và V.
Dẫn một lượng dư khí chlorine vào dung dịch chứa hỗn hợp muối NaBr và KBr sau phản ứng thu được hỗn hợp hai muối, đồng thời thấy khối lượng muối giảm 4,45 gam.
Tính số mol chlorine đã tham gia phản ứng.








