25 CÂU HỎI
Cho hình vẽ như sau. Cho biết hiện tượng xảy ra trong bình tam giác?



dd H2SO4 đặc
Na2SO3 tt
dd Br2
dd H2SO4 đặc
Na2SO3 tt
dd Br2
A. Không có hiện tượng gì xảy ra.
B. Có kết tủa màu vàng xuất hiện.
C. Dung dịch Br2bị mất màu, đồng thời xuất hiện kết tủa.
D. Dung dịch Br2bị mất màu nâu.
Đem 11,2 gam Fe để ngoài không khí, sau một thời gian thu được một hỗn hợp X gồm Fe và các oxit. Hòa tan hoàn toàn hỗn hợp đó trong dung dịch H2SO4đặc, nóng dư, thu được dung dịch Y và 3,36 lít khí SO2(đktc). Số mol H2SO4đã tham gia phản ứng là
A. 0,25.
B. 0,45.
C. 0,35.
D. 0,75.
Cho 2,24 lít SO2(đktc) hấp thụ hết vào 200 ml dung dịch NaOH 1M thu được dung dịch Y. Khối lượng muối có trong dung dịch Y là:
A. 25,2 gam.
B. 11,5 gam.
C. 12,6 gam.
D. 10,4gam.
Tại sao viên than tổ ong có nhiều lỗ?
A. Tăng nồng độ oxi khi quạt vào than.
B. Tăng nhiệt độ để nhanh chín thức ăn.
C. Tăng áp suất của phản ứng.
D. Tăng diện tích tiếp xúc của than với oxi.
Ở 25oC, kẽm ở dạng bột khi tác dụng với dung dịch HCl 1M, tốc độ phản ứng xảy ra nhanh hơn so với kẽm ở dạng hạt. Yếu tố ảnh hưởng đến tốc độ phản ứng trên là
A. Diện tích bề mặt tiếp xúc.
B. Áp suất.
C. Nhiệt độ.
D. Nồng độ.
Tìm câu sai: Tại thời điểm cân bằng hóa học thiết lập thì
A. Số mol các chất tham gia phản ứng không đổi.
B. Tốc độ phản ứng thuận bằng tốc độ phản ứng nghịch.
C. Số mol các sản phẩm không đổi.
D. Phản ứng không xảy ra nữa.
Thuốc thử đặc trưng để nhận biết ra hợp chất halogenua trong dung dịch là
A. Ba(OH)2.
B. NaOH.
C. AgNO3.
D. BaCl2.
Axit sufuric đặc, nguội có thể đựng trong bình chứa làm bằng
A. Ca.
B. Ag.
C. Cu.
D. Al.
Cho 7,84 lít hỗn hợp khí X (đktc) gồm Cl2và O2phản ứng vừa đủ với 11,1 gam hỗn hợp Y gồm Mg và Al, thu được 30,1 gam hỗn hợp Z. Phần trăm khối lượng của Al trong Y là
A. 51,35%.
B. 48,65%.
C. 75,68%.
D. 24,32%.
Cho phản ứng sau ở trang thái cân bằng: CO(k)+ H2O(k)→ CO2(k)+ H2(k)∆H < 0. Sự biến đổi nào sau đây không>làm chuyển dịch cân bằng hoá học?
A. Thay đổi nồng độ khí H2hoặc CO2.
B. Thay đổi nồng độ khí H2O.
C. Thay đổi nhiệt độ.
D. Thay đổi áp suất.
Oleum có công thức tổng quát là
A. H2SO4.nH2O.
B. H2SO4 đặc.
C. H2SO4.nSO3.
D. H2SO4.nSO2.
Cho hỗn hợp X gồm 3,2 gam Cu và 8,4 gam Fe tác dụng với dung dịch HCl dư thấy có V lit khí thoát ra (đktc). Giá trị của V là
A. 3,36 lit.
B. 2,24 lit.
C. 1,12 lit.
D. 4,48 lit.
Cho các phương trình phản ứng sau:
MnO2+ (A) → MnCl2+ (B)↑ + (C);
(B) + H2→ (A);
(A) + (D) → FeCl2+ H2.
Các chất (A), (B), (C), (D) lần lượt là:
A. NaCl, Cl2, H2O, FeO.
B. NaCl, Cl2, H2O, Fe(OH)2.
C. HCl, Cl2, H2O, Fe.
D. HCl, H2, H2O, Fe.
Khi cho axit sunfuric đặc vào NaCl (rắn) đun nóng. Chất khí sinh ra là
A. SO2.
B. H2S.
C. HCl.
D. Cl2.
Cần bao nhiêu gam nước để pha loãng 100g dung dịch H2SO4 50% (khối lượng riêng là 1,84g/ml) thành dung dịch mới có nồng độ 10%?
A. 100 gam.
B. 500 gam.
C. 200 gam.
D. 400 gam.
Nước clo hoặc khí clo ẩm có tính tẩy màu (tẩy trắng) vì nguyên nhân là
A. clo hấp thụ màu.
B. clo có tính oxi hóa mạnh.
C. nước clo chứa HClO có tính oxi hóa mạnh, tẩy màu.
D. clo tác dụng với nước tạo ra HCl có tính tẩy màu.
Cho cân bằng hóa học sau: PCl5(r)→ PCl3(k)+ Cl2(k), ∆H >0.
Cân bằng chuyển dịch theo chiều nghịch khi
A. Giảm nồng độ Cl2.
B. Giảm áp suất.
C. Thêm PCl5.
D. Giảm nhiệt độ.
Để phân biệt được 3 chất khí: CO2, SO2và O2đựng trong 3 bình mất nhãn riêng biệt, người ta dùng thuốc thử là
A. Nước vôi trong và dung dịch Br2.
B. Dung dịch Br2.
C. Nước vôi trong.
D. Dung dịch KMnO4.
Xét phản ứng phân hủy N2O5 trong dung môi CCl4 ở 45oC: 2N2O5 → 2N2O4 + O2. Ban đầu nồng độ của N2O5 là 4,66M, sau 368 giây nồng độ của N2O5 là 4,16M. Tốc độ trung bình của phản ứng tính theo N2O5 là
A. 6,80.10−4mol/(l.s).
B. 1,36.10−3mol/(l.s).
C. 2,72.10−3mol/(l.s).
D. 6,80.10−3mol/(l.s).
Đốt cháy hết 4,8 gam lưu huỳnh bột trong khí hiđro vừa đủ thu được V lít khí X. Hấp thụ hết khí X vào 500 ml dung dịch NaOH 0,5M, sau phản ứng thu được dung dịch Y. Cô cạn dung dịch Y thu được m gam rắn khan. Giá trị m là
A. 19,5.
B. 11,7.
C. 10,6.
D. 8,4.
Cho cân bằng hóa học sau: 2SO2(k)+ O2(k)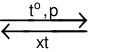 2SO3(k). Khi tăng nhiệt độ thì tỉ khối của hỗn hợp khí so với H2giảm đi. Phát biểu đúng khi nói về cân bằng này là
2SO3(k). Khi tăng nhiệt độ thì tỉ khối của hỗn hợp khí so với H2giảm đi. Phát biểu đúng khi nói về cân bằng này là
A. Phản ứng thuận tỏa nhiệt, cân bằng dịch chuyển theo chiều nghịch khi tăng nhiệt độ.
B. Phản ứng nghịch thu nhiệt, cân bằng dịch chuyển theo chiều thuận khi tăng nhiệt độ.
C. Phản ứng thuận thu nhiệt, cân bằng dịch chuyển theo chiều nghịch khi tăng nhiệt độ.
D. Phản ứng nghịch tỏa nhiệt, cân bằng dịch chuyển theo chiều thuận khi tăng nhiệt độ.
Cho 11,7 gam hỗn hợp bột Mg và Al tác dụng hết với dung dịch HCl dư thu được dung dịch Y và V lít khí H2(đktc). Cô cạn dung dịch Y thu được 54,3 gam muối clorua khan. Giá trị của V là
A. 10,08.
B. 6,72.
C. 13,44.
D. 26,88.
Cho 1,67 gam hỗn hợp gồm hai kim loại ở 2 chu kỳ liên tiếp thuộc nhóm IIA tác dụng hết với dung dịch HCl (dư), thoát ra 0,672 lít khí H2(ở đktc). Hai kim loại đó là
A. Sr và Ba.
B. Mg và Ca.
C. Be và Mg.
D. Ca và Sr.
Đơn chất halogen nào sau đây là chất rắn (ở điều kiện thường) và có tính thăng hoa?
A. I2.
B. Br2.
C. Cl2.
D. F2.
Cho các chất sau: H2S, S, O2, O3, SO2, H2SO4. Số chất vừa có tính oxi hóa, vừa có tính khử là
A. 1.
B. 3.
C. 2.
D. 4.


