42 CÂU HỎI
Trong các hợp chất sau đây, hợp chất nào có liên kết ion?
A. HCl.
B. H2O.
C. NH3.
D. NaCl.
Để đánh giá loại liên kết trong phân tử hợp chất, người ta có thể dựa vào hiệu độ âm điện. Khi hiệu độ âm điện của hai nguyên tử tham gia liên kết ³ 1,7 thì đó là liên kết
A. ion.
B. cộng hoá trị không cực.
C. cộng hoá trị có cực.
D. kim loại.
Trong các phản ứng hoá học, các nguyên tử kim loại có khuynh hướng
A. nhận thêm electron.
B. nhận hay nhường electron phụ thuộc vào từng phản ứng cụ thể.
C. nhường electron.
D. nhận hay nhường electron phụ thuộc vào từng kim loại cụ thể.
Cho 2 nguyên tử có cấu hình electron ở trạng thái cơ bản như sau: 1s22s1 và 1s22s22p5. Hai nguyên tử này kết hợp nhau bằng loại liên kết gì để tạo thành hợp chất?
A. Liên kết cộng họa trị có cực.
B. Liên kết ion.
C. Liên kết cộng hóa trị không cực.
D. Liên kết kim loại.
Ion X- có cấu hình electron là 1s22s22p6, nguyên tử Y có số electron ở các phân lớp s là 5. Liên kết giữa X và Y thuộc loại liên kết nào sau đây?
A. cộng hóa trị phân cực.
B. cho nhận.
C. ion.
D. cộng hóa trị.
Liên kết ion tạo thành giữa hai nguyên tử
A. kim loại điển hình.
B. phi kim điển hình.
C. kim loại và phi kim.
D. kim loại điển hình và phi kim điển hình.
Liên kết được tạo nên giữa hai nguyên tử bằng một hay nhiều cặp electron chung, gọi là
A. Liên kết ion.
B. Liên kết cộng hoá trị.
C. Liên kết kim loại.
D. Liên kết hydrogen.
Trong phân tử sẽ có liên kết cộng hoá trị phân cực nếu cặp electron chung có đặc điểm nào sau đây?
A. Ở giữa hai nguyên tử.
B. Lệch về một phía của một nguyên tử.
C. Chuyển hẳn về một nguyên tử.
D. Nhường hẳn về một nguyên tử.
Cho các phát biểu sau về hợp chất ion:
(1) Không dẫn điện khi nóng chảy.
(2) Dễ hòa tan trong các dung môi hữu cơ.
(3) Có nhiệt độ nóng chảy và nhiệt độ sôi cao.
(4) Khó tan trong nước.
Số phát biểu đúng là
A. 1.
B. 2.
C. 3.
D. 4.
Cho dãy các chất: N2, H2, NH3, NaCl, HCl, H2O. Số chất trong dãy mà phân tử chỉ chứa liên kết cộng hóa trị phân cực là
A. 3.
B. 6.
C. 5.
D. 4.
Hợp chất có liên kết ion trong phân tử là
A. CO2.
B. NH4Cl.
C. HCl.
D. H2O2.
Nguyên tử nguyên tố X có cấu hình electron 1s22s22p63s23p64s1, nguyên tử nguyên tố Y có cấu hình electron 1s22s22p5. Liên kết hoá học giữa nguyên tử X và nguyên tử Y thuộc loại liên kết
A. kim loại.
B. cộng hoá trị.
C. ion.
D. cho nhận.
Cho biết các giá trị độ âm điện của nguyên tử các nguyên tố sau: K (0,82); Al (1,61); H (2,20); O (3,44); S (2,58); Br (2,96) và Cl (3,16). Hợp chất nào sau đây có liên kết ion trong phân tử?
A. SO2
B. AlCl3
C. H2O
D. KBr
Phát biểu nào sau đây là sai khi nói về liên kết trong phân tử HCl?
A. Phân tử HCl là phân tử phân cực.
B. Các electron liên kết bị hút lệch về một phía nguyên tử chlorine.
C. Cặp electron dùng chung nằm chính giữa hai nguyên tử hydrogen và chlorine.
D. Nguyên tử hydrogen và chlorine liên kết với nhau bằng một liên kết đơn.
Liên kết hóa học trong đó cặp electron dùng chung bị hút lệch về phía nguyên tử có độ âm điện cao hơn được gọi là
A. liên kết cộng hóa trị có cực.
B. liên kết ion.
C. liên kết cộng hóa trị không cực
D. liên kết cộng hóa trị vô cực.
Nhận xét nào sau đây đúng khi nói về phân tử khí cacbonic (CO2), biết CO2 có cấu trúc thẳng:
A. Liên kết giữa C và O là cộng hóa trị không cực, CO2 là phân tử có cực.
B. Liên kết giữa C và O là cộng hóa trị có cực, CO2 là phân tử có cực.
C. Liên kết giữa C và O là cộng hóa trị không cực, CO2 là phân tử không cực.
D. Liên kết giữa C và O là cộng hóa trị có cực, CO2 là phân tử không cực.
Liên kết cộng hóa trị không phân cực thường là liên kết giữa:
A. Hai kim loại giống nhau.
B. Hai phi kim giống nhau.
C. Một kim loại mạnh và một phi kim mạnh.
D. Một kim loại yếu và một phi kim yếu.
Nhận định sai về hợp chất cộng hóa trị là
A. Các hợp chất cộng hóa trị tồn tại ở trạng thái rắn, lỏng hoặc khí.
B. Các hợp chất cộng hóa trị không cực tan tốt trong các dung môi không cực.
C. Các hợp chất cộng hóa trị tan tốt trong nước.
D. Các hợp chất cộng hóa trị không cực không dẫn điện ở mọi trạng thái.
Với phân tử NH3 phát biểu nào sau đây là đúng?
A. Liên kết trong phân tử là liên kết ion.
B. Liên kết trong phân tử là liên kết cộng hóa trị không phân cực.
C. Liên kết trong phân tử là liên kết cộng hóa trị phân cực.
D. Liên kết trong phân tử là liên kết cho – nhận.
Trong phân tử nitrogen, các nguyên tử liên kết với nhau bằng liên kết:
A. ion yếu.
B. ion mạnh.
C. cộng hóa trị không có cực.
D. cộng hóa trị phân cực.
Công thức electron nào sau đây là của phân tử H2O?
A. 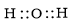
B. 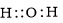
C.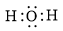
D.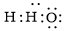
Công thức electron nào sau đây là của phân tử khí nitrogen?
A. 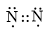
B. 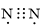
C. 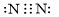
D. 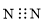
Công thức được viết dựa trên công thức electron, trong đó mỗi cặp electron chung được thay bằng một gạch nối “–” gọi là
A. công thức cấu tạo thu gọn.
B. công thức Lewis.
C. công thức phân tử.
D. công thức cấu tạo.
Công thức Lewis của CS2 là
A. 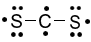
B. 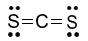
C. 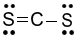
D. 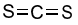
Công thức Lewis của H2O là
A. 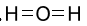
B. 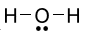
C. 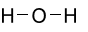
D. 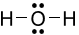
Số cặp electron không tham gia liên kết của nguyên tử N trong phân tử NCl3 là
A. 0.
B. 1.
C. 2.
D. 3.
Công thức Lewis nào sau đây viết sai?
A. 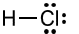
B. 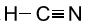
C. 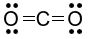
D. 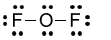
Nguyên tử nào sau đây khi hình thành ion có khuynh hướng nhường 1 electron?
A. Ca.
B. K.
C. Cu.
D. Fe.
Khi hình thành anion nguyên tử oxygen có xu hướng
A. nhường 1 electron.
B. nhận 2 electron.
C. nhận 1 electron.
D. nhường 2 electron.
Hợp chất nào sau đây có liên kết ion?
A. H2O.
B. CH4.
C. KBr.
D. Cl2.
Hợp chất nào sau đây có liên kết cộng hóa trị không phân cực?
A. O2.
B. KCl.
C. H2O.
D. HF.
Hợp chất nào sau đây không tạo được liên kết hydrogen liên phân tử?
A. H2O.
B. HF.
C. C2H5OH.
D. H2S.
Liên kết hydrogen xuất hiện giữa những phân tử cùng loại nào sau đây?
A. C2H6.
B. CH3OH.
C. CO2.
D. H2S.
Cho bảng số liệu sau về tên và công thức của các ion:
|
Tên ion |
Công thức ion |
|
Calcium |
Ca2+ |
|
Nitrate |
NO3- |
|
Phosphate |
PO43- |
Công thức của calcium nitrate là
A. Ca2NO3.
B. CaNO3.
C. Ca(NO3)2.
D. Ca3NO3.
Bảng sau cung cấp một số thông tin về các nguyên tố sodium và sulfur
|
Nguyên tố |
sodium (Na) |
sulfur (S) |
|
Số hiệu nguyên tử |
11 |
16 |
Sodium sulfide là một hợp chất ion. Phản ứng tạo thành sodium sulfide nào sau đây là đúng?
A.
B.
C.
D.
Potassium chloride là một hợp chất có thể tan trong nước lạnh và có nhiệt độ nóng chảy cao (801oC). Liên kết trong phân tử potassium chloride là gì?
A. Liên kết công hóa trị.
B. Liên kết hydrogen.
C. Liên kết ion.
D. Liên kết cho nhận.
Khí nitrogen (N2) rất bền, ở nhiệt độ thường N2 khá trơ về mặt hóa học nên trong một số trường hợp đặc biệt, khí nitrogen được dung để bơm lốp (vỏ) xe thay cho không khí có thể oxi hóa cao su theo thời gian. Vì sao nitrogen lại có đặc tính này?
A. phân tử N2 có liên kết ba bền vững, năng lượng liên kết lớn.
B. phân tử N2 có liên kết đơn bền vững, năng lượng liên kết nhỏ.
C. phân tử N2 có liên kết ba bền vững, năng lượng liên kết nhỏ.
D. phân tử N2 có liên kết đơn bền vững, năng lượng liên kết lớn.
Trong phân tử, các electron chuyển động không ngừng, khi các electron tập trung về một phía sẽ hình thành nên
A. một ion dương.
B. một ion âm.
C. một lưỡng cực tạm thời.
D. một lưỡng cực vĩnh viễn.
Vì sao HF có nhiệt độ sôi cao hơn hẳn so với HCl, HBr, HI?
A. HF có phân tử khối lớn nhất.
B. HF có liên kết hydrogen.
C. HF có tương tác van der Waals lớn nhất.
D. HF là hợp chất phân cực nhất.
Phát biểu nào sau đây là đúng?
A. Tương tác van der Waals mạnh hơn liên kết hydrogen.
B. Liên kết hydrogen mạnh hơn liên kết ion và liên kết cộng hóa trị.
C. Sự chuyển động không ngừng của các electron tạo nên các lưỡng cực vĩnh cửu.
D. Liên kết hydrogen giữa các phân tử H2O mạnh hơn liên kết hydrogen giữa các phân tử C2H5OH.
Trong dung dịch ethanol (C2H5OH) có bao nhiêu loại liên kết hydrogen được tạo thành?
A. 2.
B. 3.
C. 4.
D. 1.
Dãy các chất nào sau đây trong phân tử đều có liên kết ion?
A. O2, Cl2, HCl, F2.
B. K2O, NaCl, CaCl2, MgO.
C. HCl, H2S, N2O, NaCl.
D. CaO, HNO3, H2SO4, HCl.

