18 CÂU HỎI
Phần 1. Trắc nghiệm nhiều phương án lựa chọn
Cho phản ứng hóa học sau: Zn (s) + H2SO4 (aq, dư) → ZnSO4 (aq) + H2 (g)
Yếu tố nào sau đây không ảnh hưởng đến tốc độ phản ứng?
A. Diện tích bề mặt Zn.
B. Nồng độ dung dịch sulfuric acid.
C. Thể tích dung dịch sulfuric acid.
D. Nhiệt độ của dung dịch sulfuric acid.
Yếu tố nào dưới đây đã được sử dụng để làm tăng tốc độ của phản ứng rắc men vào tinh bột đã được nấu chín (cơm, ngô, khoai, sắn) để ủ rượu?
A. Nhiệt độ.
B. Nồng độ.
C. Chất xúc tác.
D. Áp suất.
Trong các cặp phản ứng sau, nếu lượng Fe trong các cặp đều được lấy bằng nhau và có kích thước như nhau thì cặp nào có tốc độ phản ứng lớn nhất?
A. Fe + dung dịch HCl 0,1 M.
B. Fe + dung dịch HCl 0,2 M.
C. Fe + dung dịch HCl 0,3 M.
D. Fe + dung dịch HCl 0,5 M.
Cho phương trình hóa học của phản ứng tổng hợp ammonia như sau:
![]()
Khi tăng nồng độ của hydrogen lên 2 lần, tốc độ phản ứng thuận
A. tăng lên 8 lần.
B. giảm đi 2 lần.
C. tăng lên 6 lần.
D. tăng lên 2 lần.
Đối với phản ứng: A + 3B ![]() 2C, phát biểu nào sau đây đúng?
2C, phát biểu nào sau đây đúng?
A. Tốc độ tiêu hao chất B bằng 3/2 tốc độ tạo thành chất C.
B. Tốc độ tiêu hao chất B bằng 2/3 tốc độ tạo thành chất C.
C. Tốc độ tiêu hao chất B bằng 3 tốc độ tạo thành chất C.
D. Tốc độ tiêu hao chất B bằng 1/3 tốc độ tạo thành chất C.
Cho ba mẫu đá vôi (100% ![]() ) có cùng khối lượng: mẫu 1 dạng khối, mẫu 2 dạng viên nhỏ, mẫu 3 dạng bột mịn vào ba cốc đựng cùng thể tích dung dịch HCl (dư, cùng nồng độ, ở điều kiện thường). Thời gian để đá vôi tan hết trong ba cốc tương ứng là
) có cùng khối lượng: mẫu 1 dạng khối, mẫu 2 dạng viên nhỏ, mẫu 3 dạng bột mịn vào ba cốc đựng cùng thể tích dung dịch HCl (dư, cùng nồng độ, ở điều kiện thường). Thời gian để đá vôi tan hết trong ba cốc tương ứng là ![]() giây. So sánh nào sau đây đúng?
giây. So sánh nào sau đây đúng?
A. 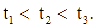
B. 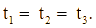
C. 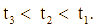
D. 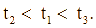
Xét phản ứng: A + 2B → 3C + D. Tốc độ trung bình của sự mất đi của B tương đương với biểu thức nào sau đây?
A. ![]()
B. ![]()
C. ![]()
D. ![]()
Thực hiện phản ứng sau:
![]()
Theo dõi thể tích ![]() thoát ra theo thời gian, thu được đồ thị như sau (thể tích khí được đo ở áp suất khí quyển và nhiệt độ phòng).
thoát ra theo thời gian, thu được đồ thị như sau (thể tích khí được đo ở áp suất khí quyển và nhiệt độ phòng).
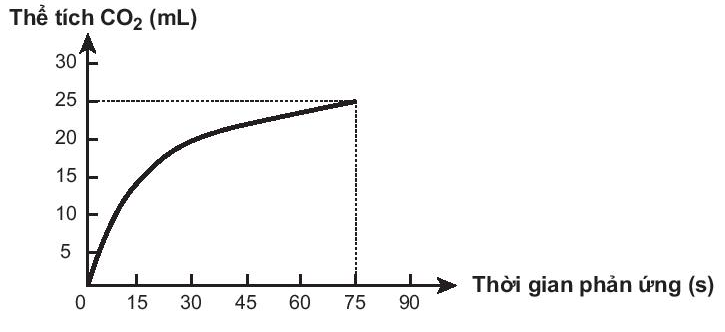
Trong các phát biểu sau, phát biểu nào không đúng?
A. Tốc độ trung bình của phản ứng trong các khoảng thời gian 15 giây là như nhau.
B. Tốc độ phản ứng giảm dần theo thời gian.
C. Tốc độ trung bình của phản ứng trong khoảng thời gian từ thời điểm đầu đến 75 giây là 0,33 mL/s.
D. Ở thời điểm 90 giây, tốc độ phản ứng bằng 0.
Cho phản ứng đơn giản: ![]()
Người ta thực hiện 3 thí nghiệm với nồng độ các chất đầu (![]() và
và ![]() ) được lấy khác nhau và xác định được tốc độ tạo thành HI trong 20 giây đầu tiên, kết quả cho trong bảng sau:
) được lấy khác nhau và xác định được tốc độ tạo thành HI trong 20 giây đầu tiên, kết quả cho trong bảng sau:
|
|
|
|
|
0,10 |
0,20 |
5,00 |
|
0,20 |
0,20 |
10,00 |
|
0,10 |
0,15 |
3,75 |
Biểu thức định luật tác dụng viết cho phản ứng trên là
A. ![]()
B. ![]()
C. ![]()
D. ![]()
Cho phản ứng điều chế khí oxygen trong phòng thí nghiệm bằng cách nhiệt phân muối potassium chlorate (![]() ):
):
![]()
Trong các biện pháp sau:
(a) Dùng chất xúc tác manganese dioxide (![]() ).
).
(b) Dùng phương pháp dời nước để thu khí oxygen.
(c) Nung hỗn hợp potassium chlorate và manganese dioxide ở nhiệt độ cao.
Những biện pháp được sử dụng để làm tăng tốc độ phản ứng là
A. a, c.
B. a, b.
C. b, c.
D. a, b, c.
Tốc độ phản ứng là
A. độ biến thiên nồng độ của một chất phản ứng trong một đơn vị thời gian.
B. độ biến thiên nồng độ của một sản phẩm phản ứng trong một đơn vị thời gian.
C. độ biến thiên nồng độ của một chất phản ứng hoặc sản phẩm phản ứng trong một đơn vị thời gian.
D. độ biến thiên nồng độ của các chất phản ứng trong một đơn vị thời gian.
Phát biểu nào sau đây là đúng?
A. Tốc độ của phản ứng hoá học có thể có giá trị âm hoặc dương.
B. Tốc độ của phản ứng hoá học là hiệu số nồng độ của một chất trong hỗn hợp phản ứng tại hai thời điểm khác nhau.
C. Trong cùng một phản ứng hoá học, tốc độ tiêu thụ các chất phản ứng khác nhau sẽ như nhau nếu chúng được lấy với cùng một nồng độ.
D. Trong cùng một phản ứng hoá học, tốc độ tạo thành của các chất sản phẩm khác nhau là khác nhau, tuỳ thuộc vào hệ số cân bằng của chúng trong phương trình hoá học.
Tốc độ trung bình ![]() của một phản ứng được viết theo biến thiên nồng độ các chất theo thời gian như sau:
của một phản ứng được viết theo biến thiên nồng độ các chất theo thời gian như sau:
![]()
Phản ứng đó là
A. 4A + B → 2C + 3D.
B. 4A + 2B → 2C + 3D.
C. ![]()
D. B + 4D → 2C + 3A.
Cho phản ứng sau: ![]()
Sau một thời gian đo được: ![]()
Tốc độ trung bình của phản ứng trên trong khoảng thời gian đó là
A. ![]()
B. ![]()
C. ![]()
D. ![]()
Cho phản ứng X + Y → Z. Khi bắt đầu phản ứng, nồng độ chất X là 0,024 mol/L. Sau 10s xảy ra phản ứng, nồng độ của X là 0,022 mol/L. Tốc độ phản ứng trong trường hợp này là
A. 0,0003 mol/L.s.
B. 0,00025 mol/L.s.
C. 0,00015 mol/L.s.
D. 0,0002 mol/L.s.
NOCl là chất khí độc, sinh ra do sự phân hủy nước cường toan (hỗn hợp ![]() và HCl có tỉ lệ 1 : 3). NOCl có tính oxi hóa mạnh, ở nhiệt độ cao bị phân hủy theo phản ứng hóa học sau: 2NOCl → 2NO + Cl2. Tốc độ phản ứng ở
và HCl có tỉ lệ 1 : 3). NOCl có tính oxi hóa mạnh, ở nhiệt độ cao bị phân hủy theo phản ứng hóa học sau: 2NOCl → 2NO + Cl2. Tốc độ phản ứng ở ![]() là
là ![]() mol/(L.s) và ở
mol/(L.s) và ở ![]() là
là ![]() mol/(L.s). Hệ số nhiệt độ
mol/(L.s). Hệ số nhiệt độ ![]() của phản ứng là
của phản ứng là
A. 2,25.
B. 2,5.
C. 3.
D. 1,75.
Khi nhiệt độ tăng lên 10 oC, tốc độ của một phản ứng hóa học tăng lên 3 lần. Hỏi tốc độ của phản ứng đó tăng lên bao nhiêu lần khi nâng nhiệt độ lên từ 30 oC đến 50 oC?
A. 3 lần.
B. 6 lần.
C. 9 lần.
D. 27 lần.
Cho phương trình hóa học của phản ứng: X + 2Y → Z + T. Ở thời điểm ban đầu, nồng độ của chất X là 0,01 mol/L. Sau 20 giây, nồng độ của chất X là 0,008 mol/L. Tốc độ trung bình của phản ứng tính theo chất Y trong khoảng thời gian trên là
A. 4,0.10−4 mol/(L.s).
B. 1,0.10−4 mol/(L.s).
C. 2.10−4 mol/(L.s).
D. 0,5.10−4 mol/(L.s).

